
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Второй закон термодинамики
|
|
|
|
Самопроизвольный процесс, происходящий без изменения энергетического запаса системы совершается только в направлении, при котором энтропия возрастает (S>О);
Австрийским физиком Больцманом было установлено
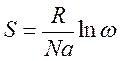
Энтропия - это логарифмическое выражение вероятности существования системы.
R - универсальная газовая постоянная = 8,314 Дж/моль К;
N - постоянная Авогадро (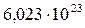 );
);
Следовательно, чем большим числом макрочастиц представлена рассматриваемая макросистема, тем больше вариантов распределение этих частиц, при которых может быть достигнуто макросостояние, тем выше значение энтропии.
1. С повышением температуры энтропия возрастает, так как усиливается неупорядоченность, хаос в системе, т.е.:
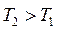 , то
, то 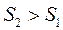
2. Энтропия скачкообразно увеличивается при переходе вещества (кристаллического) в жидкое, т.е. в процессе плавления:
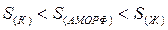
Для веществ в кристаллическом состоянии характерна упорядоченность частиц и наличие ближнего и дальнего порядка. Частицы расположены в строгой последовательности.
Зависимость энтропии от температуры t можно выразить графиком:
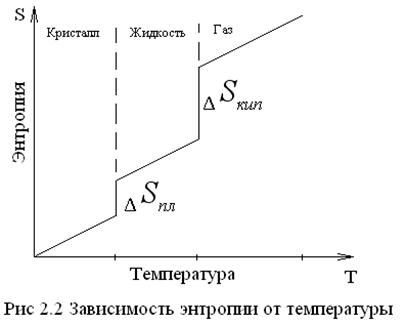
Здесь необходима различать постепенное изменение энтропии (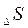 ) за счет изменения параметров состояния (Т) и скачкообразное – в результате фазовых переходов и химических реакций.
) за счет изменения параметров состояния (Т) и скачкообразное – в результате фазовых переходов и химических реакций.
3. Процессы — нагревания, кипения, диссоциации, вызывающие увеличение
беспорядка сопровождаются увеличением энтропии.
4. Кристаллизация, полимеризация связана с уменьшением объема, сопровождаются уменьшением энтропии.
5. Чем тверже вещество, тем меньше его энтропия, чем мягче, тем энтропия больше.
По группам сверху вниз наблюдается увеличение энтропии. В отличие от всех других термодинамических функций энтропия имеет абсолютное значение.
|
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 437; Нарушение авторских прав?; Мы поможем в написании вашей работы!