
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Свинцовый аккумулятор
|
|
|
|
Pb │H2SO4 │PbO2│ Pb
25 – 30 %
Анодный процесс:
Pb – 2e  Pb
Pb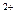
Образующиеся ионы Pb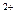 осаждаются на поверхности анода в виде малорастворимого PbSO4
осаждаются на поверхности анода в виде малорастворимого PbSO4
Катодный процесс:
PbO2 + 4H3O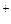 + 2e
+ 2e  Pb
Pb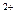 + 6H2O
+ 6H2O
Образующиеся ионы Pb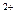 осаждаются на поверхности катода в виде
осаждаются на поверхности катода в виде
PbSO4
Тогда суммарная токообразующая реакция:
Pb + PbO2 + 2H2SO4  2 PbSO4 + 2H2O ЭДС = 2,1 В.
2 PbSO4 + 2H2O ЭДС = 2,1 В.
Сущность – более энергетически богатые Pb и PbO2 переходят в менее энергетически богатое вещество PbSO4.
Во внутренней цепи происходит перенос ионов. Ионы SO4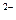 движутся к аноду, а ионы H
движутся к аноду, а ионы H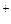 - катоду. У анода расходуются анионы, у катода – катионы. Раствор в целом остаётся электронейтральным.
- катоду. У анода расходуются анионы, у катода – катионы. Раствор в целом остаётся электронейтральным.
ЭДС зависит от конц. H2SO4 и для 25% конц. ~ 2 В. Так как H2SO4 при работе связывается, поэтому ЭДС уменьшается. По концентрации кислоты можно судить о степени разряда аккумулятора. На практике измеряется не сама концентрация., а плотность раствора H2SO4.
Недостаток – сравнительно небольшой.
1. Срок службы (из-за постоянной сульфатации электродов – неполное превращение PbSO4 в Pb и PbO2 при заряде)
(2 – 5 лет)
2. Малая удельная ёмкость/на единицу массы (кол-во электричества, которое отдаётся на единицу массы вещества).
3. Особенность электрохимических генераторов состоит в том, что электрохимически активные вещества не закладываются заранее, а подводятся по мере израсходования. Это обеспечивает непрерывность работы.
Свинцовой аккумулятор не должен сильно разряжаться. Если ЭДС падает до 1,8, то модно считать, что он полностью истощен. В его работе происходит испарение воды и частичное ее разложение, поэтому необходимо добавлять воду в дистиллированную. Всякие примеси снижают КПД. Для зарядки аккумулятора подключают к внешнему источнику тока. При этом ток протекает через аккумулятор в направлении обратном тому, в котором он проходил при зарядке аккумулятора. И электрохимические процессы на электродах обращаются.
Щелочной аккумулятор:
Значительное распространение имеют щелочные железо- или кадмий-никелевые аккумуляторы.
Fe │КОН │NiOOH │Ni ЭДС = 1,35 - 1,4 А
20%
Fe + 2NiOOH + H2O 2 Ni(OH) + Fe(OH)2
2 Ni(OH) + Fe(OH)2
Анодом служит Fe (или кадмиевая) пластина. Катод – никель.
Железо – никелевый аккумулятор.
Электролит 20% КОН.
ЭДС = 1,3 В
Обычно они выпускаются в продажу в виде батарей, состоящих из нескольких ячеек, включенных последовательно. В отличии от кислотных, щелочные аккумуляторы могут долго находиться в заряженном и разряженном состоянии. Щелочные дороже Pb аккумуляторов, но они не чувствительны к большим перегрузкам.
|
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 471; Нарушение авторских прав?; Мы поможем в написании вашей работы!