
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства. 1. красный оксид ртути получают при взаимодействии металла с кислородом при нагревании до 350 °С:
Получение
1. красный оксид ртути получают при взаимодействии металла с кислородом при нагревании до 350 °С:
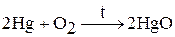
2. желтый оксид ртути при действии щелочей на растворы солей Hg2+:
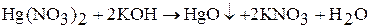
1. Оксид ртути не взаимодействует с водой;
2. Оксид ртути проявляют основные свойства. Оксид ртути взаимодействует с растворами кислот. Например:
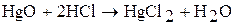
Оксид ртути (II) с растворами щелочей не взаимодействует.
В 1845 году французский химик Эжен Миллон обнаружил, что желтый оксид ртути (II) растворяется в растворе аммиака:
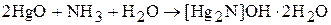
В результате реакции образуется кристаллическое вещество желтого цвета – основание Миллона (потому что гидроксогруппа может быть замещена на различные анионы). При нагревании до 110 °С вещество теряет одну молекулу кристаллизационной воды и превращается в моногидрат коричневого цвета.
Прим. Основание Миллона содержит ион [Hg2N]+, который можно рассматривать как ион NH4+, в котором четыре атома водорода заменены двумя атомами ртути. Молекулы воды расположены пустотах кристаллической решетки. Основание Миллона реагирует с кислотами, причем однозарядные анионы кислоты обычно занимают место иона ОН– и одной молекулы воды. Образующиеся соли имеют строение: 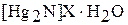 (где
(где  ).
).
Образование бурого осадка йодида основания Миллона при взаимодействии раствора тетрайодомеркурата (II) калия (реактив Несслера) с аммиаком служит качественной реакцией на аммиак и ионы аммония:
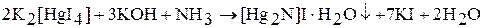
Основные свойства оксидов усиливаются в ряду ZnO – CdO – HgO. Окислительные свойства оксидов усиливаются в ряду ZnO – CdO – HgO, что подтверждается температурами их восстановления: оксид цинка восстанавливается углеродом при 900 °С, оксид кадмия – при 500 °С, оксид ртути (II) разлагается выше 400 °С без участия восстановителя.
|
|
Дата добавления: 2014-01-15; Просмотров: 1414; Нарушение авторских прав?; Мы поможем в написании вашей работы!