
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кислородные соединения азота
|
|
|
|
Известно шесть оксидов азота: N2O, NO, N2O3, NO2, N2O4, N2O5, а также неустойчивые оксиды N4O и NO3.
| Свойство | N2O | NO | N2O3 | NO2 | N2O4 | N2O5 |
| Степень окисления | +1 | +2 | +3 | +4 | +4 | +5 |
| Температура плавления, ºС | –90,7 | –163,7 | –101 | – | –11 | 32,4 (субл) |
| Температура кипения, ºС | –88,7 | –151,8 | 3,5 (разл) | – | 21,2 | – |
| Цвет | бесцв | бесцв | синий | бурый | бесцв | бесцв |
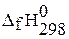 , кДж/моль , кДж/моль
| 90,2 | 50,3 (жидк) | 33,2 | –19,5 (жидк) | –41,3 (тв) | |
| Магнитные свойства | диа- | пара- | диа- | пара- | диа- | диа- |
Оксид азота (I) N2O (монооксид азота, закись азота) – бесцветный газ, без запаха, сладковатый на вкус, малорастворим в воде (при 0º С один объем газа растворяется в одном объеме воды). При вдыхании небольших количеств оксида азота (I) вызывается судорожных смех, поэтому его называют «веселящим газом».
Молекула N2O имеет линейное строение. Методом ВС строение молекулы оксида азота (I) описывается с помощью двух резонансных структур:
 ↔
↔ 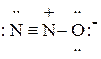
Наложением двух резонансных структур получаем: 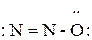
Длина связи N – N 113 пм, N – O 118 пм.
Получение N2O
1. термическим разложением нитрата аммония:
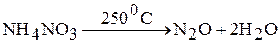
Образующийся газ может быть загрязнен азотом и оксидом азота (II). Нельзя допускать перегрева смеси, потому что оксид азота (I) разлагается со взрывом.
2. Чистый оксид азота (I) получают при взаимодействии нитрита (или азотистой кислоты) и соли гидразина или гидроксиламина:
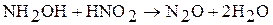
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 455; Нарушение авторских прав?; Мы поможем в написании вашей работы!