
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Улавливание абсорбентами на основе Na (содой и щелочью)
|
|
|
|
Использование щелочных вод и технических стоков
Схема, основанная на циркуляции раствора муравьиной кислоты
Основной раствор: Са(ОН)2+СаС12+НСООН (муравьиная кислота) для увеличения массообмена при абсорбции.
Основные стадии: абсорбция, окисление, нейтрализация, фильтрация.
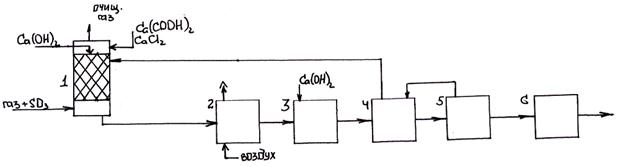
1 – абсорбер; 2 – сборник-реактор; 3 – смеситель; 4 – отстойник; 5 – фильтр; 6 – сушилка.
- газ очищают до содержания пыли не более 8 г/м3;
- раствор имеет наибольшую поглотительную способность при рН=4,5-5;
- после полного связывания формиат-ионов рН↓ до 4, что оптимально для окисления в (2), избыток воздуха – пятикратный. Суспензию с гипсом направляют в (3), где рН↑ путем добавки извести для оптимального отстоя в (4).
Далее 10-30%-ю суспензию гипса → вакуумный фильтр → гипс → на затаривание. Содержит около 0,5% СаSО3.
Недостаток схемы – необходимость такого дорогого реактива, как Са(ОН)2.
Для очистки газов от SО2 на ТЭС.
· Наиболее широко применяют воды золоуловителей, т.е. шлам, который легко перекачивается по трубам.
· Контактные аппараты – тарельчатого типа различной конструкции.
Сточная вода золоуловителя имеет рН=10,3-11,4. Её свободная щелочность достигает 21мг-экв/л, а карбонат-бикарбонатная щелочность 147 моль-экв/л
Дымовые газы – наоборот, всегда кислые: SО2 0,08-0,15%об.
СО2 5,6-9,7%об.
Абсорбция: 46-54оС при: Ж/Г=3,2 кг/кг (расход), при этом η=99% и рН=11,4 снижается → 7,0.
Особенности подобных схем:
· Химический состав золы изменяется в широких пределах в зависимости от исходного угольного топлива, его месторождения.
· Засоренность угля породой также влияет на состав золы.
· Технология сжигания влияет на долю неорганики, уносимой с потоком газа из топки.
|
|
|
Таблица - Обычный состав золы:
| SiО2 - 30-68% | А12О3 - 10-40% | Nа2О - 0,04-1,1% |
| СаО - 1,5-50% | Fе2О3 - 2-30% | К2О - 0,5-1,3 |
| МgО - 0,8-4,8% | SО3 - 0,2-1,6% | ТiО2 - 0,3-0,9% |
Щелочные оксиды дают с водой основные соединения Са(ОН)2, Мg(ОН)2, К Nа(ОН)2 и т.д. рН↑ в суспензии.
В щелочной среде протекают процессы гидролиза силикатов, алюминатов, ферритов:
хСаО·уSiО2· z Fе2О3·кА12О3 + (х+у+3z+3к)Н2О→уН2SiО3+2zFе(ОН)3 + 2кА1(ОН)3 +хСа2+ + 2хОН-
Характерно образование коллоидных форм продуктов гидролиза.
Коллоидная система – большая поверхность раздела фаз (десятки и сотни метров). Dчаст ≈ 1 мкм, хлопьевидные. Это положительный фактор.
В зависимости от соотношения щелочности в золе и SО2 в дымовых газах, поглощение SО2 может быть полным или неполным. При дефиците золы необходимо подщелачивать суспензию золы в (3), либо выброс SО2 растет.
Уравнения реакции могут быть составлены лишь в общем виде.

1 – циклон очистки дымовых газов; 2 – абсорбер; 3 – реактор гидролиза; 4 – нейтрализатор; 5 – реактор-окислитель; 6 – отстойник (сгуститель); 7 – емкость для оборотной воды; 8 – газоподогреватель (почему так назван?); 9 – центрифуга.
В реакторе с мешалкой (3) происходит смешивание частиц летучей золы с водой, образование гидроксидов Са и Мg при выщелачивании наиболее тонкодисперсных частиц (рН =3,5; 45-50оС).
В (4) поступает жидкость из абсорбера (2) насыщенная SО2 и СО2. Реакция происходит как в жидкой фазе, так и на поверхности коллоидных частиц гидроксидов.
Крупные частицы и нерастворимые частицы являются затравочными центрами образования осадка.
SО2+2 ОН-→SО32- +Н2О - основная реакция связывания SО2.
Но если щелочи мало, то: SО2+ ОН-→НSО3-
Реакции в нейтрализаторе (5) НSО3- +0,5О2→ НSО4-
Шлам – смесь сульфата кальция 2х водного и золы.
Варианты использования:
1) Добавки к цементу и получение гипсобетонных изделий сразу из суспензии.
2) Прокаливание при 250-400оС и получение гипсового вяжущего.
|
|
|
Примеры теоретического анализа, показывающие эффективность такого метода, исходя из состава отходов сжигания угля разных разрезов:
| Месторождение | Выход SО2 мг-экв/кг | СаО/SО2 моль/моль |
| Эстонское сланцевое | 3,95 | |
| Березовское | 1,35 | |
| Карагандинское | 0,05 |
Моль/моль ~ 1 ед. (СаО + SО2=СаSО3)
46.9 Магнезитовый метод улавливания SО2
Включает стадии абсорбции, хемосорбции, регенерации хемосорбента, утилизации концентрата SО2 в серную кислоту.
В упрощенном выражении: SО2 через стадию абсорбции водой, хемосорбируется оксид-гидроксидом магния - МgО· Мg(ОН)2.
Образующийся МgSО3 имеет ограниченную растворимость и выпадает в осадок в виде смеси: МgSО3·6Н2О, МgSО3·3Н2О.
Эту соль сушат и прокаливают. МgО – возвращают в цикл. SО2 – переводят в Н2SО4.
Реакции:
МgО+Н2О→ Мg(ОН)2
МgSО3+Н2О+SО2→Мg(НSО3)2
Мg(НSО3)2 + Мg(ОН)2 → 2 Мg SО3↓+2Н2О
Кислая соль слабое основание пересыщенный раствор

1 – абсорбер Вентури; 2 – нейтрализатор; 3 – центрифуга; 4 – сушилка; 5 – печь.
Орошение суспензией 1:10, где начальная рН = 6,8-7,5;
конечная рН=5,5-6,0
Состав суспензии:
МgО - 1,5%
МgSО3 - 6,7%
МgSО4 - 12,4%
Сульфат магния образуется в абсорбере, но его образование нежелательно (т.к. регенерация при tо=1200-1300, тогда МgО становится неактивным). Поэтому на стадии абсорбции - сокращают время контакта, а на стадии обжига в шихту вводят кокс для снижения температуры разложения МgSО4 или используют природный газ в печах-КС или во вращающихся печах.
На центрифугу подают лишь часть суспензии.
После сушилки получают продукт:
MgO – 2,6%;
MgSO3 – 65%;
MgSO4 – 12%.
После обжига во вращ. печах при 900ºС MgO с 8% MgSO4, возвращают в цикл, обжиговый газ после печи содержит SO2 с концентрацией 7-15%.
Схема требует пополнения MgO и доп. воды.
Достоинства метода:
- можно очищать горячие газы.
- продукт рекуперации – H2SO4 – проблемы сбыта – нет.
- доступность и дешевизна MgO
- высокая эффективность очистки
Недостатки метода:
- сложность схемы.
- неполное разложение MgSO4 и его потери.
- потери MgO при регенерации
46.10 Цинковый метод улавливания SО2
Абсорбент – суспензия ZnO
ZnO+ SО2 ® ZnSO3 – нерастворим, образует осадок, что проще отделять.
Обжиг – всего 350ºС.
Недостаток ZnSO4 – нерентабельно регенерировать – выводится из системы.
|
|
|
Na2CO3 + SO2 ® Na2SO4 + CO2
Na2SO3 + SO2 + H2O ® 2NaHSO3 и тоже самое с NaOH
Далее NaHSO3 + ZnO ® ZnSO3 ↓ + NaOH
т.е. цинковый метод с добавлением солей Na в раствор.
|
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 597; Нарушение авторских прав?; Мы поможем в написании вашей работы!