
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Второе начало термодинамики
|
|
|
|
Первый закон термодинамики не может отличить обратимые процессы от необратимых. Он просто требует от термодинамического процесса определенного энергетического баланса и ничего не говорит о том, возможен такой процесс или нет. Направление самопроизвольно протекающих процессов устанавливает второй закон термодинамики.
Формулировка Клаузиуса: Теплота самопроизвольно не может переходить от тела с меньшей температурой к телу с большей температурой.
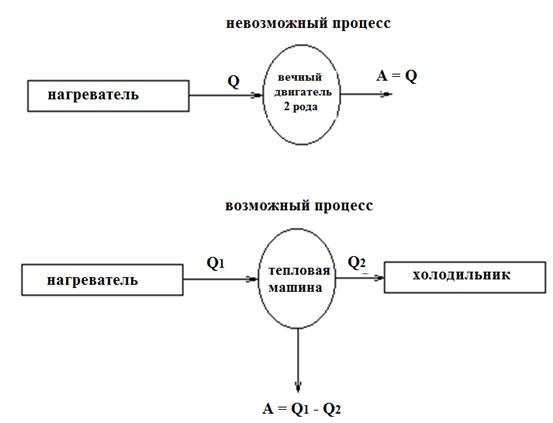
Формулировка Томсона: Невозможен вечный двигатель второго рода, т.е. такой периодический процесс, единственным результатом которого было бы превращение теплоты в работу следствие охлаждения тела.
Обратимым называется процесс1 – 2, если можно совершить обратный процесс 2 – 1 через все промежуточные состояния системы так, чтобы после возвращения системы в исходное состояние в окружающих телах не произошло ни каких-либо изменений. Такой процесс является физической абстракцией.
Необратимыми называются процессы, при которых возвращение системы в исходное состояние возможно лишь при условии затрат внешней энергии, что влечёт за собой определённые изменения в окружающей среде.
Все реальные процессы являются необратимыми (расширение газа в пустоту, теплообмен, диффузия).
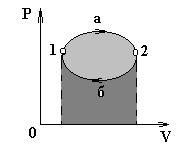 Круговым процессом (циклом) называется процесс, при котором система возвращается в исходное состояние.
Круговым процессом (циклом) называется процесс, при котором система возвращается в исходное состояние.
1) Цикл изображённый на рисунке прямой, соответствует тепловой работе, т.е. устройству, которое получает количество теплоты от некоторого теплоотдатчика (нагревателя), совершает работу и отдаёт часть этой теплоты теплоприёмнику (холодильнику).
Рабочее вещество в этом цикле – газ, который совершает положительную работу.
|
|
|
Коэффициент полезного действия тепловой машины (прямого цикла) называют отношение совершённой работы к количеству теплоты, полученному рабочим веществом от нагревателя:
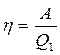 (1)
(1)
Так как работа тепловой машины совершается за счёт полученного количества теплоты, то DU = 0, значит из первого начала термодинамики, следует, что
А = Q1 + Q2,
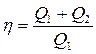 (2)
(2)
 2) Обратный цикл соответствует работе холодильной машины, т.е. такой системе, которая отбирает теплоту от холодильника и передаёт количество теплоты нагревателю. Исходя из второго начала термодинамики, такой процесс невозможен самопроизвольно. Он происходит за счёт работы внешних сил. При этом газ совершает отрицательную работу.
2) Обратный цикл соответствует работе холодильной машины, т.е. такой системе, которая отбирает теплоту от холодильника и передаёт количество теплоты нагревателю. Исходя из второго начала термодинамики, такой процесс невозможен самопроизвольно. Он происходит за счёт работы внешних сил. При этом газ совершает отрицательную работу.
Цикл Карно – это круговой процесс, состоящий из двух изотерм 1-2, 3-4 (Т1 > Т2) и двух адиабат 2-3, 4-1. Рабочее вещество – идеальный газ.
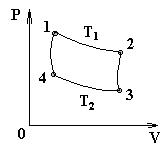 КПД обратимого цикла Карно:
КПД обратимого цикла Карно:
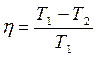 (3)
(3)
Положения Карно:
1. КПД всех обратимых (абстрактных) машин, работающих по циклу, состоящему из двух изотерм и адиабат, с нагревателем при температуре Т1 и холодильником при температуре Т2, равны между собой и не зависят от рабочего вещества и конструкции машины, совершающей цикл.
2. КПД необратимой (реальной) машины меньше КПД обратимой (абстрактной) машины:
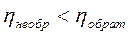 (4)
(4)
На основании этих положений можно записать количественную формулировку второго начала термодинамики:
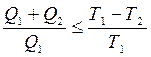 (5)
(5)
«=» -относится к обратимому циклу,
«<» - к необратимому.
Допустим, что происходит теплообмен между двумя телами без совершения работы А, значит 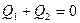 , тогда исходя из (5) Т1 – Т2 > 0 и Т1 > Т2, что соответствует первой формулировке Клаузиуса.
, тогда исходя из (5) Т1 – Т2 > 0 и Т1 > Т2, что соответствует первой формулировке Клаузиуса.
Если бы тепловая машина полностью затрачивала всю полученную при теплообмене энергию на совершение работы и не отдаёт энергию холодильнику т.е 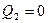 , тогда исходя из (5) будем иметь:
, тогда исходя из (5) будем иметь:
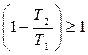 (6)
(6)
что невозможно, так как Т1, Т2 – положительны. Об этом говорит вторая формулировка Томсона о невозможности вечного двигателя второго рода. 
|
|
|
Алгебраической суммой приведённым количеством теплоты называют следующее отношение, полученное из (5):
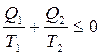
«=» -относится к обратимому циклу,
«<» - к необратимому.
Если состояние системы изменяется по некоторому произвольному циклу, который можно представить в виде совокупности достаточно малых циклов Карно, тогда (6), можно записать:
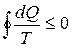
где 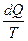 - элементарная приведённая теплота,
- элементарная приведённая теплота, 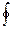 - означает, что интегрирование проводится по замкнутому контуру, т. е. по циклу.
- означает, что интегрирование проводится по замкнутому контуру, т. е. по циклу.
В 1865 г. Клаузиус вводит новую функцию S – э нтропию.
Энтропия есть функция состояния системы. Соответственно её можно представить в виде разности двух значений конечного и начального состояния системы, равного сумме приведённых количеств теплоты:

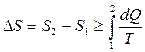 (7)
(7)
где знак «=» - относится к обратимому циклу, а«>» - к необратимому.
Если процесс протекает в изолированной системе (dQ = 0), тогда для обратимых процессов энтропия не изменяется, т.е. S = const и DS = 0, а для необратимых процессов энтропия возрастает, т.е. DS > 0.
Это увеличение энтропии не будет происходить беспредельно. Энтропия будет возрастать до тех пор, пока в системе не наступит равновесное состояние, следствии выравнивания параметров между телами системы.
Согласно молекулярно-кинетической теории, энтропию представляют как меру неупорядоченности расположения частиц системы.
Неупорядоченность состояния системы количественно характеризуется термодинамической вероятностью Wтер.
Термодинамическая вероятность Wтер - это число микросостояний, реализующих данное макросостояние.
По Больцману ВНТ является статистическим законом:
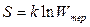
В заключении: ПЗТ содержит энергетический баланс процесса, а ВЗТ показывает его возможное направление.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 474; Нарушение авторских прав?; Мы поможем в написании вашей работы!