
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Водородная связь. Химическая связь, основанная на электростатическом притяжении ионов, называется ионной связью
Химическая связь, основанная на электростатическом притяжении ионов, называется ионной связью.
Ионные или электростатические взаимодействия.
Энергия связи - энергия, выделяющаяся при ее образовании, или необходимая для разъединения двух связанных атомов.
Энергия связи характеризует ее прочность. Энергия ковалентной связи составляет от 300 до 700 кДж/моль.
Различают неполярную и полярную ковалентную связь:
Неполярная (симметричная) ковалентная связь - связь между атомами с практически равной электроотрицательностью и, следовательно, равномерным распределением электронной плотности между ядрами атомов.
Например: H-H, Cl-Cl, C-C.
Полярная (несимметричная) ковалентная связь - связь между атомами с различной электроотрицательностью и несимметричным распределением общей электронной пары.
Электронная плотность такой связи смещена в сторону более электроотрицательного атома, что приводит к появлению на нем частичного отрицательного заряда d- («дельта минус»), а на менее электроотрицательном атоме - частичного положительного заряда δ+ («дельта плюс») и молекула становится диполем (молекула воды):
Cδ+ Cld-, Cd+ Od-, Cd+ Nd-
Примеры образования ковалентной связи в полипептидах и белках:
а) пептидная связь, она представляет собой сопряжённый тип связи (промежуточный вариант между одинарной и двойной связью);
б) внутри- и межмолекулярные -S-S- связи:
!!! Как мы увидим в дальнейшем, образование S–S-связей играет важную роль в организации третичной структуры белка.
!!! Помимо сильных ковалентных взаимодействий существуют еще и слабые нековалентные взаимодействия, которые стабилизируют пространственную структуру органических молекул.
К ним относятся: ионные, водородные, гидрофобные связи и
ван-дер-ваальсовые взаимодействия.
Такая связь возникает при большой разнице в электроотрицательностях связываемых атомов: когда менее электроотрицательный атом почти полностью отдает свои валентные электроны и превращается в катион; другой, более электроотрицательный атом, эти электроны присоединяет и становится анионом.
Атом Na (1 электрон на внешнем уровне) и атом Cl (7 внешних электронов) превращаются в ионы Na+ и Cl- с завершенными внешними электронными оболочками (по 8 электронов), между которыми возникает электростатическое притяжение, т.е. ионная связь.
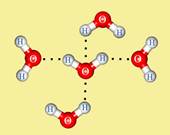
Структуру водородной связи мы с вами разберём на примере взаимодействия молекул воды между собой.
Молекула воды является диполем. Это объясняется тем, что атом водорода, связанный с более электроотрицательным элементом кислородом, имеющим неподелённую электронную пару, испытывает недостаток электронов и поэтому способен взаимодействовать с атомом кислорода другой молекулы воды.
В результате этого взаимодействия возникает водородная связь
(Рис. 2.1):
|
Дата добавления: 2014-01-20; Просмотров: 379; Нарушение авторских прав?; Мы поможем в написании вашей работы!