
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Белки, содержащие негемовое железо
|
|
|
|
Компоненты электрон-транспортной цепи
Компонентами электрон-транспортной цепи являются сложные ферменты и простые белки переносчики.
В переносе электронов от субстратов к молекулярному кислороду принимают участие:
1. НАД - зависимые дегидрогеназы;
2. ФАД- зависимые дегидрогеназы;
3. Убихинон (КоQ);
4. Цитохромы b, c, a +a3;
НАД-зависимые дегидрогеназы. В качестве кофермента содержат НАД и НАДФ. Пиридиновое кольцо никотинамида способно присоединять электроны и протоны водорода.
ФАД и ФМН-зависимые дегидрогеназы содержат в качестве кофермента фосфорный эфир витамина В2 (ФАД).
Убихинон или коэнзим Q (КоQ) играет роль промежуточного переносчика водородных атомов, т. е. электронов и протонов в митохондриальной мембране, окисляя восстановленную форму флавиновых ферментов и превращается при этом в гидрохинон КоQ∙H2 (рис. 8.3):
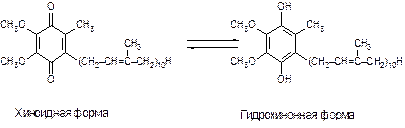
Рис. 8.3. Строение убихинона коэнзима Q (КоQ)
Цитохромы - белки хромопротеиды, способные присоединять электроны, благодаря наличию в своем составе в качестве простетических групп железопорфиринов.
Они принимают электрон от вещества, являющегося немного боле сильным восстановителем, и передают его более сильному окислителю.
Цитохромы разделяют на подгруппы а, b и с. К двум последним группам относят цитохромы, содержащие обычный гем (рис 8.4)
Цитохромы располагаются в митохондриальной цепи между убихиноном и кислородом. При этом цитохромы включаются в дыхательную цепь в определенной последовательности:
Цит. b → Цит. c 1 → Цит. c → Цит. aa 3
Цитохромы b, c и c 1 выполняют функцию промежуточных переносчиков электроновю
Комплекс цитохромов a и a1, называемый цитохромоксидазой, является терминальным дыхательным ферментом, непосредственно взаимодействующим с кислородом.
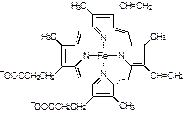
Рис. 8.4 Строение гема, входящего в состав цитохромов b и с
!!! В отличии от гема гемолгобина атом железа в цитохромах может обратимо переходить из двух в трехвалентное состояние это обеспечивает транспорт электронов.
Белки, содержащие негемовое железо. В этих белках атомы железа связаны с атомами серы цистеиновых остатков или прямо с атомами серы S2-, поэтому их часто называют железосерными белками и обозначают как Fe-S (рис. 8.5):
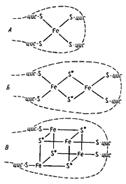
Рис. 8.5. Структура белков, содержащих негемовое железо (Fe-S-белки)
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 729; Нарушение авторских прав?; Мы поможем в написании вашей работы!