
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Колебание двухатомной молекулы
|
|
|
|
Предисловие.
КОЛЕБАТЕЛЬНАЯ СПЕКТРОМЕТРИЯ. ТЕОРИЯ КОЛЕБАНИЙ.
(исправил 5.05.12)
Колебательные спектры можно наблюдать двумя метдами:
1. Абсорбционная ИК-спектроскопия, базирующаяся на изменении интенсивности ИК-излучения, которое поглощается веществом, при изменении частоты (волнового числа);
2. Спектроскопия комбинационного рассеивания (Раман-спектроскопия).
Оба метода дают информацию о колебании атомов в молекуле. Прежде чем рассматривать эти виды спектроскопии, необходимо познакомиться с теорией колебания атомов в молекулах.
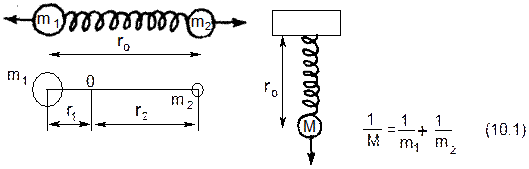 |
Рассмотрим самый простой случай колебания – это колебание двухатомной молекулы. Для молекулы типа ХУ возможен только одно колебательное движение, а именно вдоль оси связи между двумя атомами. Именно эту связь можно рассматривать как причину сопротивления растяжению или сжиманию молекулы. Тогда в качестве модели двухатомной молекулы можно взять два шара, связанные между собой пружиной или один шар с приведенной массой М, подвешенный на пружине:
Если пружину растянуть, то возникает колебание шара относительно положения равновесия. При растягивании пружины возникает обратная сила (поэтому знак «-», ибо растягивание и обратная сила направлены в противоположные стороны), пропорциональная смещению х (подчиняется закону Гука). Сила действия пружины на шар возникает за счет уменьшения потенциальной энергии V, поэтому перед производной dV/dx тоже ставится знак «-»:
F = - kx = - dV/dx, (10.2)
где х = r - ro, а k – силовая постоянная связи. Разделяя переменные величины и интегрируя от 0 до х, находим:
dV = kxdx, V = ò kxdx = ½×kx2 (квадратичная парабола). (10.3)
10.2.1. Классическое решение колебательной задачи.
|
|
|
Моменты вращения шаров (см. схему под двухшаровой моделью) равны:
m1r1 = m2r2, a r = r1 + r2.
При этом F = ma = m1¶2 r1/¶ t2 = m2 ¶2 r2/¶ t2 = - kx = -k(r -ro). Тогда:
¶2(r -ro)/¶ t2 = ¶2x/¶ t2 = ¶2r/¶ t2 = ¶2r1/¶ t2 + ¶2r2/¶ t2 = - k(1/m1 + 1/m2)(r – ro), или
М¶2x/¶ t2 = - kx
Классическое решение этого дифференциального уравнения:
r = ro + aCos2pnt,
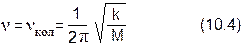 |
где а – амплитуда колебания, а частота n колебания атомов в молекуле определяется уравнением Гука:
10.2.2. Квантово-механическое решение колебательной задачи.
Решение находится при помощи уравнения Шрёдингера: Ĥc = Еc, где Ĥ – гамильтониан (оператор) энергии, c (хи) – колебательная волновая функция, Е – стационарные уровни колебательной энергии. С учетом выражения для гамильтониана это уравнение Шредингера для колебательной задачи записывается следующим образом:
-(h2/8π2M)(¶2χ/¶t2) + Vχ = Eχ.
 |
Решение уравнения Шредингера при V = ½×kx2 дает следующее выражение для колебательной волновой функции:
где Hv(x) – полином Чебышева-Эрмита, v – колебательное квантовое число, принимающее значение ряда чисел: 0, 1, 2, 3 и т.д., x (кси) – координата колебания (x = х/а), b = 2p2Мk/h2. Степенная часть колебательной волновой функции в уравнении (10.5) всегда четная (симметричная), поскольку x2, зато Hv(x) имеет разную четность в зависимости от v и четности самой x. При малых значениях v он определяется зависимостями:
| v | ||||
| Нv | 2x | 2(x2 – 1) | 4x(2x2 – 3) |
Из этой таблицы следует сделать вывод, что полином Чебышева-Эрмита, как и вся колебательная волновая функция, при четных значениях колебательного квантового числа v всегда четный (симметричный), при нечетных же значениях v имеет ту четность (тип симметрии), что и координата колебания x.
Решение уравнения Шредингера дает следующее выражение для стационарных уровней колебательной энергии:
Ev=hνкол(v +1/2), (10.6)
| v | Ev | E(v + 1) - Ev |
| ½ hνкол | ||
| 3/2 hνкол | hνкол | |
| 5/2 hνкол | hνкол | |
| 7/2 hνкол | hνкол |
 Из представленной выше таблицы вытекает, что стационарные уровни колебательной энергии строго квантованы, а для гармонического осцилятора разница между соседними уровнями одна и та же. Чтобы молекула перешла с нижнего уровня на верхний, например, при переходе 0 1, она должна извне получить квант энергии инфракрасного излучения DЕ = hnизл, который должен быть равным разнице энергии между колебательными уровнями, т.е. hnизл= hnкол. Отсюда выплывает требование, при котором излучение поглощается:
Из представленной выше таблицы вытекает, что стационарные уровни колебательной энергии строго квантованы, а для гармонического осцилятора разница между соседними уровнями одна и та же. Чтобы молекула перешла с нижнего уровня на верхний, например, при переходе 0 1, она должна извне получить квант энергии инфракрасного излучения DЕ = hnизл, который должен быть равным разнице энергии между колебательными уровнями, т.е. hnизл= hnкол. Отсюда выплывает требование, при котором излучение поглощается:
|
|
|
nизл= nкол.
10.3. Модель колебания – ангармонический осцилятор.

Потенциальная энергия колебания реальной молекулы существенно отличается от энергии, описываемой квадратичной параболой:
Кроме того, для реальной молекулы расстояние между колебательными уровнями энергии не является постоянным, а немного уменьшается при увеличении колебательного квантового числа v. Таким образом, модель гармонического осцилятора – плохая модель.
Поэтому берут модель ангармонического осцилятора, значительно лучше описывающую колебание реальной молекулы. Это достигается введением в уравнение потенциальной энергии дополнительного кубического члена:
V=(1/2)kx2 – k’x3,
где k’ – постоянная ангармоничности силовой постоянной (k’<<k). Решение уравнения Шредингера:
Еv = hνкол(v + ½) – y hνкол(v + ½)2 – z hνкол(v + ½)3 +...
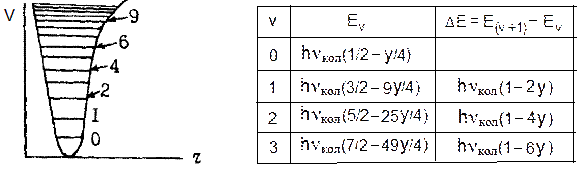 |
Здесь y (у<<1) та (z<<y) z – постоянные ангармоничности энергии. Грубое приближение - пренебрежение членами с (v + ½)n, где n > 2 дает следующие результаты:
Из этих данных видно, что в соответствии с моделью ангармонического осцилятора расстояния между энергетическими уровнями действительно уменьшаются по мере возрастания колебательного квантового числа.
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 2763; Нарушение авторских прав?; Мы поможем в написании вашей работы!