
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Метод иодометрии
|
|
|
|
Метод иодометрии основан на ОВ реакциях, связанных с превращением I2 в I‾ и обратно:
I2 + 2 ē ↔ 2 I‾
Ох Red

Данная реакция обратима, поэтому иодометрия применяется и для определения Ох и Red.
Рабочие растворы – стандартизированы раствор I2 – окислитель метода и Na2S2O3 – восстановитель метода.
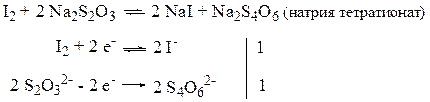
В качестве индикатора в иодометрии используют водный раствор крахмала, который образует с йодом йодкрахмальное соединение синего цвета.
При титровании йода рабочим раствором Na2S2O3 точка эквивалентности определяется по исчезновению синей окраски, причем крахмал необходимо добавлять в конце титрования, чтобы исключить погрешность. Высокая чувствительность крахмала к йоду и резкое изменение окраски раствора в точке эквивалентности позволяют использовать рабочие растворы I2 и Na2S2O3 меньшей концентрации, чем в других методах (от 0,01 н. до 0,05 н.).
Йодометрию необходимо проводить:
1) на холоде (т.к. I2 – летучее соединение, и при нагревании чувствительность крахмала к йоду уменьшается);
2) рН не должен превышать 9, т.к. в щелочной среде возможна реакция:

Йодометрическое определение восстановителей осуществляют по методу прямого или обратного титрования окислителей – косвенным титрованием.
Прямое титрование рабочим раствором I2 – определение соединений As(III), Sb(III), Sn(II), сульфидов, сульфитов, аскорбиновой кислоты:

Если титрование осложнено (восстановитель летучий, или реакция протекает медленно), используют обратное титрование; при этом нужны 2 рабочих раствора - I2 и Na2S2O3. К восстановителю добавляют точный избыток раствора I2, а остаток его титруют Na2S2O3.
Например,
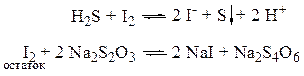
Для определения окислителей – к анализируемому раствору добавляют избыток KI в H2SO4 разб., и выделившийся I2 титруют Na2S2O3. Этим методом определяют Cl2, Br2, KMnO4, KClO3, CaOCl2, нитриты, Н2О2, Fe(III), Cu(II), As(V).
|
|
|
Растворы I2 и Na2S2O3 – вторичные стандартные растворы, т.к. не удовлетворяют всем требованиям. В качестве первичного стандарта используют K2Cr2O7 или KIO3:


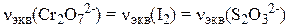
Методами оксидиметрии в клинических и биохимических исследованиях определяют содержание ферментов каталазы, пероксидазы, аскорбиновой кислоты, сахара в крови, мочевой кислоты в моче, ионов Са2+ в сыворотке крови.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 677; Нарушение авторских прав?; Мы поможем в написании вашей работы!