
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства брома и йода
|
|
|
|
Физические свойства брома и йода
Бром был открыт в 1825 г. Балларом при обработке соляного рассола бромида калия смесью пиролюзита и серной кислоты.
В 1811 году из золы морских водорослей Бернаром Куртуа был получен йод.
Бром – темно-красная жидкость, а ее пар – желто-бурого цвета с резким раздражающим запахом. Бром плохо растворим в воде, а также во многих органических растворителях (спирт, бензол, эфир, сероуглерод и т.д.).
Йод – черно-серое твердое вещество с металлическим блеском. Йод легко возгоняется, образуя фиолетовые пары. Йод плохо растворяется в воде, хорошо в растворах йодидов металлов и органических растворителях. Вдыхание паров йода и особенно брома разрушающе действует на дыхательные пути и поэтому очень опасно.
Химическая активность брома меньше, чем хлора.
1. Бром реагирует с металлами и неметаллами (за исключением О2, N2, He, Ne, Ar, благородных газов) с образованием бромидов. Например:
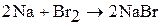
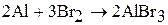
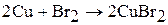
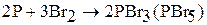
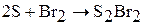
2. Йод реагирует с металлами и неметаллами (за исключением О2, S, N2, He, Ne, Ar, благородных газов) с образованием йодидов. Химическая активность йода наименьшая в ряду галогенов. Со многими элементами йод непосредственно не взаимодействует, а с некоторыми реагирует при повышенных температурах.
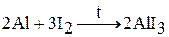
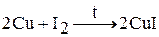
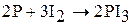
2. Бром и йод взаимодействует с водородом по цепному радикальному механизму. Реакция с бромом протекает медленно, а с йодом идет при нагревании и не доходит до конца – обратимый процесс:
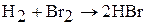

3. Растворение брома и йода в воде сопровождается диспропорционированием:


По сравнению с хлором равновесие реакции смещено еще больше влево, поэтому бром и йод присутствуют в водном растворе в виде I2 и Br2.
В щелочных растворах бром и йод диспропорционируют подобно хлору, но скорость процесса увеличивается:
|
|
|


Скорость диспропорционирования иона IO3– велика, поэтому в растворах он не существует.
4. Для йода характерны восстановительные свойства. Йод окисляется концентрированной азотной кислотой (хлором, бромом, пероксидом водорода) в водной среде до йодноватой кислоты:
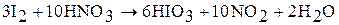
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 10737; Нарушение авторских прав?; Мы поможем в написании вашей работы!