
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные понятия. 7.2. Испарение и конденсация
|
|
|
|
ФАЗОВЫЕ РАВНОВЕСИЯ И ПРЕВРАЩЕНИЯ
Лекция 9
7.1. Основные понятия
7.2. Испарение и конденсация
7.3. Равновесие жидкости и насыщенного пара
7.4. Критическое состояние
7.5. Пересыщенный пар и перегретая жидкость
7.6. Плавление и кристаллизация
7.7. Уравнение Клапейрона — Клаузиуса
7.8. Тройная точка. Диаграмма состояния
В термодинамике фазой называется совокупность однородных, одинаковых по своим свойствам частей системы. Поясним понятие фазы на следующих примерах:
В закрытом сосуде находится вода и над ней смесь воздуха и паров воды. В этом случае мы имеем дело с системой, состоящей из двух фаз: одну фазу образует вода, вторую — смесь воздуха и паров воды. Если в воду добавить несколько кусочков льда, то все эти кусочки образуют третью фазу. Различные кристаллические модификации какого-либо вещества также представляют собой разные фазы. Так, например, алмаз и графит являются различными твердыми фазами углерода.
При определенных условиях разные фазы одного и того же вещества могут находиться в равновесии друг с другом, соприкасаясь между собой. Равновесие двух фаз может иметь место лишь в определенном интервале температур, причем каждому значению температуры Т соответствует вполне определенное давление р, при котором возможно равновесие.
Таким образом, состояния равновесия двух фаз изобразятся на диаграмме (р, Т) линией
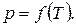
Три фазы одного и того же вещества (твердая, жидкая и газообразная, или жидкая и две твердые) могут находиться в равновесии только при единственных значениях температуры и давления, которым на диаграмме (р, Т) соответствует точка, называемая тройной. Эта точка лежит на пересечении кривых равновесия фаз, взятых попарно.
|
|
|
В термодинамике доказывается в согласии с опытом, что равновесие более чем трех фаз одного и того же вещества невозможно.
Переход из одной фазы в другую обычно сопровождается поглощением или выделением некоторого количества тепла, которое называется скрытой теплотой перехода, или просто теплотой перехода. Такие переходы называются фазовыми переходами первого рода.
Существуют переходы из одной кристаллической модификации в другую, которые не связаны с поглощением или выделением тепла. Такие переходы называются фазовыми переходами второго рода. Фазовые переходы второго рода не исчерпываются переходами между различными кристаллическими модификациями. К их числу принадлежит переход в сверхпроводящее состояние, совершаемый в отсутствие магнитного поля, а также переход между двумя жидкими фазами гелия, называемыми гелием-I и гелием-II. Мы ограничимся рассмотрением только переходов первого рода.
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 252; Нарушение авторских прав?; Мы поможем в написании вашей работы!