
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Физико-химические особенности обратимого процесса
|
|
|
|
Особенности обратимого процесса рассмотрим на примере процесса, который происходит при передаче тепла к молю идеального газа, который находится в цилиндре с поршнем (рис. 3). Цилиндр погружен в термостат с водой температуру которой можно очень плавно, без резких скачков повышать или понижать, используя нагревательное или охладительное устройства.
 | |||
 | |||





Рис. 3 К процессу производства работы расширения и сжатия газа:
а) исходное состояние; б) конечное состояние
Предположим, что на поршне с массой m1, находится тело с массой m2. Кроме того поршень контактирует с атмосферой и на него действует атмосферное давление Ратм. Примем, что поршень двигается в поршне без трения (в последующем это ограничение снимем). На поршень действует суммарная сила тяжести в виде веса и атмосферного давления (m1g + m2g + Pатм), которую можно уравновесить давлением газа Рг, имеющего температуру Т1 при давлении V1.
Давление Рг как физическую силу (Н/м2) при Т1 и V1, которая уравновешивает внешние силы, можно рассчитать из условия
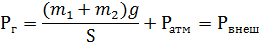
где Рвнеш – внешнее давление, против которого совершается работа расширения; S – площадь поршня (м2).
Источник тепла и холодильное устройство должны давать возможность точно определять количество теплоты, которой система (газ + вода в термостате) обменивается с окружающей средой. Вода в термостате постоянно перемешивается мешалкой, чтобы полностью исключить перепады температуры в разных частях термостата. Только в этом случае температура Т1 будет иметь смысл физического параметра в целом для воды в термостате и для газа в цилиндре. В этом случае говорят, что газ находится в тепловом равновесии с водой в термостате и с источником теплоты.
|
|
|
С помощью теплоисточника будем медленно нагревать воду в термостате так, чтобы разность температур между теплоисточником и водой и между водой и газом была чрезвычайно небольшой (в пределе бесконечно малой). Через некоторый промежуток времени, пусть очень длительный, температура газа повысится с Т1 до Т2. Объем газа увеличится с V1 до V2, при этом будет произведена работа по преодолению внешних сил W = Pвнеш (V2 – V1). На каждом этапе процесса система (газ + вода) и окружающая среда в виде источника теплоты практически находятся в состоянии теплового равновесия, а внешние объекты, на которые направлена работа (грузы + атмосфера), в состоянии механического равновесия с газом Рвнеш = Рг (для того, чтобы исключить влияние температуры газа на атмосферное давление наложим условие, что поршень нетеплопроводен). Из приведенного рассмотрения следует, что в пределе процесс совершается через последовательность состояний термического и механического равновесий.
На каждом этапе движущая сила (давление газа) и сила (Рвнеш), на преодоление которой направлена работа, уравновешены.
Процесс, который совершается через непрерывную последовательность состояний, предельно близких к равновесию, называется равновесным*.
Увеличение внешних сил (Рвнеш) по отношению к внутренним силам (Рг) на исчезающее малую величину, позволяет на каждом этапе направить процесс в обратном направлении (работа совершается внешней средой над системой). Если равновесный 1→2 процесс провести в обратном направлении он пройдет через последовательность тех же состояний, которые имели место в прямом направлении. В этом смысле равновесный процесс термодинамически обратим. В результате циклического равновесного процесса в исходное состояние возвращается как среда, так и система.
|
|
|
В дальнейшем термодинамически обратимый и равновесный процесс будем рассматривать как равнозначные.
Равновесный процесс в строгом смысле этого слова сугубо теоретический идеальный процесс, поскольку к нему предъявляются взаимоисключающие требования – быть равновесием и быть процессом. Состояние термического, механического, химического и прочих равновесий – статическое состояние и оно в практическом смысле не может быть элементом процесса. Но при интерпретации равновесного процесса допускается незначительное, исчезающее малое различие сил системы и окружающей среды на каждом этапе его протекания. Другими словами его представляют в виде скачкообразного пути между близко расположенными смежными состояниями равновесия. По этой причине равновесный процесс называют также квазистатическим. Идеальный процесс в отличие от естественного, поддается точному физико-математическому описанию, и в силу того, что изменения функций состояния не зависят от пути процесса его закономерности можно распространить и на реальные процессы.
_____________________
* Состояние равновесия в данном процессе следует отличать от состояния термодинамического равновесия, например в химической реакции. В состоянии термодинамического равновесия движущие силы процесса полностью исчерпаны (об этом речь пойдет ниже). В равновесном процессе на всем его протяжении они не равны нулю, но они уравновешены силами окружающей среды.
Кроме того при анализе равновесных процессов удается выявить такие закономерности, которые очень трудно или невозможно установить, изучая реальный процесс. Классическим примером в этом смысле является проблема, каким образом можно повысить коэффициент полезного действия тепловых машин. По этому поводу выдвигались разные идеи, например, использовать вместо водяного пара атмосферный воздух. Карно, анализируя предложенный им термодинамически обратимый цикл (цикл Карно) на основе которого в принципе может работать тепловая машина, установил, что КПД тепловых машин зависит только от разности температур источника тепла Т1 и холодильного устройства Т2 (в качестве которого может выступать прилегающая к цилиндру атмосфера) и не зависит от природы рабочего газа
|
|
|
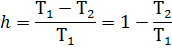
Из уравнения видно, что КПД тепловых машин увеличивается с увеличением разности температур Т1 и Т2 (при Т1→0,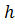 →1). И это открытие определило магистральное направление на пути развития теплоэнергетически.
→1). И это открытие определило магистральное направление на пути развития теплоэнергетически.
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 298; Нарушение авторских прав?; Мы поможем в написании вашей работы!