
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Потенціометричне титрування
|
|
|
|
На відміну від звичайного титрування, в якому точку кінця титрування встановлюють візуально, в потенціометричному титруванні його здійснюють інструментально – за зміною величини потенціалу індикаторного електрода в процесі титрування. Його перевагами є:
- можливість аналізувати забарвлені та каламутні розчини;
- більша точність;
- документальність (будують криві титрування);
- можливість аналізу суміші речовин (HCl + CH3COOH).
При цьому використовують ті ж самі типи реакцій:
· осадження: Ag+ + Cl- =AgCl↓;
· комплексоутворення: Al3++ H2Y2- ↔ AlY- + 2H+;
· кислотно-основної взаємодії: H2CrO4 + 2OH- = CrO42- + 2H2O;
· окиснення-відновлення: Fe2+ + Cr2O72- + H+ = Fe3+ + Cr3+ + H2O.
При цьому будують криву титрування – графічну залежність потенціалу індикаторного електрода (чи іншого показника, пропорційного йому) від об’єму доданого титр анта.
Криві титрування сильної кислоти сильною основою, що описується рівнянням
HCl + NaOH = NaCl + H2O
Н++ ОН- = Н2О
наведені на рис. 4.1.



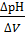 , мл-1
, мл-1


 рН
рН


 VNaOH, мл VNaOH, мл
VNaOH, мл VNaOH, мл
т. е. т. е.






 VNaOH, мл
VNaOH, мл
т. е.
Рис 4.1. Криві титрування сильної кислоти сильною основою:
а – інтегральна, б – диференційна, в – метод Грана.
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 895; Нарушение авторских прав?; Мы поможем в написании вашей работы!