
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основні класи ферментів
|
|
|
|
| Клас | Здійснювана реакція |
| Оксидоредуктази | Окислювально-відновні реакції всіх типів |
| Трансферази | Перенос окремих груп атомів від донорної молекули до акцепторної |
| Ізормерази | Взаємоперетворення різних ізомерів |
| Гідролази | Гідролітичне (за участю молекули води) розщеплення зв'язків |
| Ліази | Негідролітичне й неокислювальне розщеплення зв'язків |
| Лігази (синтетази) | Утворення зв'язків у реакції конденсації двох різних сполук |
Кожен фермент має субстратну специфічність, тобто може каталізувати перетворення лише деяких подібних субстратів, і специфічність дії, тобто каталізує тільки одну певну реакцію, наприклад окислювання-відновлення або гідролітичне розщеплення.
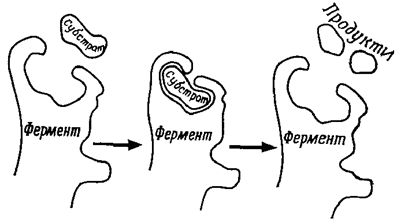
Субстратна специфічність базується на зв'язуванні субстрату з ферментом (рис. 4.2). Безпосередньо діюча ділянка ферменту, де субстрат приєднується й піддається перетворенню, називають каталітичним центром. У побудові цього центра бере участь до 20 амінокислотних залишків. Субстрат "підходить" до каталітичного центра, як ключ до замка (точніше як рукавичка до руки), відносно просторової конфігурації й розподілу зарядів, атомних груп і т.д. При зв'язуванні субстрату змінюється конформація ферменту (індукована проміжна форма).
Специфічність дії пов'язана з набором амінокислотних залишків, об'єднаних у каталітичному центрі й взаємодіючих із субстратом під час реакції. Субстратна специфічність і специфічність дії залежать від первинної структури й конформації молекули ферменту.
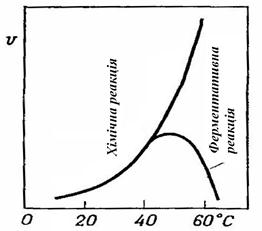
Тому що ферменти - білки, при підвищеній температурі вони денатуруються, Температурна залежність ферментативної реакції являє собою криву з оптимумом (областю найбільшої активності) при 40-600С (рис. 4.2, Б). При кип'ятінні більшість ферментів незворотньо втрачає активність.
|
|
|
| 
|
| А | Б |
| |
| В |
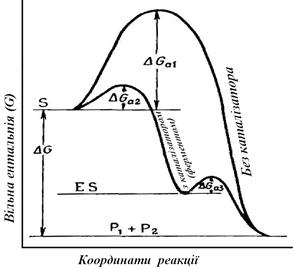
Рис. 4.2. Дія ферментів. А. Зниження енергії активації (DGа1) для екзергонічної реакції S ® P1+P2 завдяки каталізатору (ферменту). DGа1 > DGa2 + DGa3. Б. Залежність швидкості реакції v від температури при хімічній реакції без каталізатора й у присутності ферменту (Lіbbert). В. Модель ферментативного розщеплення молекули субстрату при короткочасній зміні конформації під час зв'язування субстрату з ферментом
Багато ферментів діють тільки в сполученні з низькомолекулярною органічною активною групою - коферментом. У цьому випадку ферментний білок називають апоферментом, а комплекс із апоферменту й коферменту - голоферментом. Кофермент пов'язаний з ферментом або постійно, у якості простетичної групи, або тимчасово, як косубстрат. Багато гетеротрофних організмів можуть синтезувати не всі необхідні коферменти, тому вони повинні одержувати з їжею попередники коферментів або готові коферменти у формі вітамінів (табл. 4.2).
Таблиця 4.2
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 4116; Нарушение авторских прав?; Мы поможем в написании вашей работы!