
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теоретичні основи скловаріння
|
|
|
|
ОСНОВИ ТЕХНОЛОГІЇ СКЛА
Лекція №3
У реальних виробничих умовах окремі етапи процесу скловаріння відокремити складно. Однак для розуміння самого процесу в цілому-знання елементів із якого він складається, необхідне і важливе.
Процес скловаріння складається із п'яти стадій.
Перша стадія - силікатоутворення - характеризується тим, що при її закінченні основні хімічні реакції у твердому стані між компонентами шихти закінчені, у шихті не залишається окремих складових її компонентів (піску, соди сульфату, крейди тощо), більшість газоподібних із шихти видаляється.
Для звичайного натрійкальційового скла дана стадія завершується при 800-900С.
Друга стадія - склоутворення - характеризується тим. що при її закінченні маса стає прозорою, тобто в ній відсутні не проварені частинки шихти, однак вона пронизана великою кількістю бульбашок та свилів, іншими словами неоднорідна. Для звичайного скла дана стадія завершується при 1150-1200С.
Третя стадія - дегазація - характеризується тим, що при її завершенні скломаса звільнюється від видимих газових включень, а також тим що встановлюється рівноважний стан між скломасою (рідкою фазою) та газами що залишилися у самій скломасі (газова фаза). Для звичайного скла даний етап завершується при 1400-1500С. В'язкість скломаси складає близько 10 Н . с/м2.
Четверта стадія - гомогенізація - характеризується тим, що при її завершенні скломаса звільнюється від свилів і стає однорідною. Коливання в показниках переломлення окремих частин скломаси мінімальні. У оптичному склі вказані коливання не перевищують ±0,0005.
Для звичайного скла дана стадія може бути завершена при температурах більш низьких, ніж це необхідно для завершення етапу дегазації.
|
|
|
П ' ята стадія - остудження - характеризується тим, що температура скломаси знижується на 200-300С для створення необхідної робочої в'язкості
Кожна із п'яти перерахованих стадій має свої особливості, і для проведенню кожної з них існують свої оптимальні умови. Шляхи, згідно з якими необхідно проводити практичне скловаріння, повинні базуватися на теорії скло утворення що враховує наступні явища та фактори;
1) явища фізичного, хімічного та фізико-хімічного порядку, що відбуваються у
процесі скло утворення, а саме: ' "
а) хімічні реакції, що протікають при нагріванні в окремих скло твірних
компонентах та їх сумішах;
б) термофізику процесів, тобто фізичний стан окремих скло твірних
компонент та сумішей при їх нагріванні;
в) фізико-хімічну взаємодію в скломасі, а також між скломасою та газовим
середовищем печі та між скломасою та вогнетривом;
г) термодинамічні фактори;
д)структурні особливості скла.
2) вплив різних факторів, що прискорюють процес скло утворення на окремих його етапах та вцілому.
Усі явища, що відбуваються в процесі скло утворення, класифікують наступним чином (В. Тернер 1920):
Фізичні зміни:
1) випаровування вологи;
2) нагрівання шихти;
3) плавлення окремих компонентів шихти;
4) розчинення речовин у твердому або рідкому стані в рідині, що утворилась;
5) зміна кристалічної форми;
6) випаровування деяких складових частин. Хімічні реакції:
1) розщеплення гідратів;
2) видалення фізично зв'язаної води;
3) розкладання карбонатів, сульфатів, нітратів тощо;
4) взаємодія різних компонентів та утворення силікатів. Фізико-хімічні процеси:
1) взаємодія між рідкою скломасою та газоподібними компонентами пічного простору;
2) взаємодія між скломасою та включеними у неї газами;
3) взаємодія між газовою фазою скломаси та газовою фазою бульбашок, що включені у скломасу;
|
|
|
4) взаємодія між газами печі та газами, що включені у скломасу та бульбашки, що пронизують її;
5) взаємодія між скломасою та вогнетривом.
2. Силікатоутворення та склоутворення
2.1. Реакції та поліморфні перетворення при нагріванні окремих компонентів шихти
Кварцовий пісок. При нагріванні кварцового піску у кремнеземі відбуваються наступні поліморфні перетворення.
(β-кварц < 573: > α-кварц < 870с" > α-тридиміт <- 1470- > кристобаліт.
Кальціонована сода. Температура плавлення Na2СОз - 852С. При нагріванні до 400С помічається втрата ваги, що рівна 0,33%. Пружність дисоціації Na2СОз ↔ Nа20+С02 досягає 760 мм. рт. ст. при температурі близько 1750С.
Поташ (чистий) К2СОз плавиться при температурі 897С.
Сульфат натрію. При температурі 239С Ыаг804 переходить із ромбічної у моноклінну модифікацію. Дисоціація починається при температурі 1200-1220С і посилюється при 1350С. У відновлювальному середовищі (водень) дисоціація починається при 530-590С і посилюється при 900С.
Крейда або вапняк (кальцит). Швидкість хімічної дисоціації залежить від величини зерна вказаних карбонатів. Кальцит із величиною зерна менш за 0,06 мм при нагріванні протягом 60 год при 6 З ОС втрачає 36% своєї ваги, в той час як кальцит з величиною зерна 0,09 мм при тих же умовах втрачає 22%.
Повна дисоціація кальциту з величиною зерна 0,06 мм відбувається при температурі 915С, кальциту з величиною зерна 0,02 мм - близько 902С.
Доломіт, температура дисоціації СаМg(С03)2 близько 700С.
Натрієва селітра. NaNOз плавиться при 318С, і при подальшому підвищенні температури (вище 350С), дисоціює з виділенням кисню.
Азотисто натрієва сіль, що утворилась, NaNO2 при підвищенні температури розкладається із виділенням азоту та кисню.
Калієва селітра. KN03 плавиться при 336С і при температурі 500С розкладається на азотисто калієву сіль та кисень, а при температурі вище 500С остання розкладається на азот, кисень та окис калію.
2.2. Леткість компонентів шихти при нагріванні
Із компонентів шихти найбільшу леткість при нагріванню мають борна кислота та її солі, окис свинцю, сполуки миш'яку, окис сурми, селен та деякі його сполуки, а також хлориди.
Леткість борної кислоти залежить від її кількості у шихті, складу шихти та умов її нагрівання.
|
|
|
Леткість, розрахована на 1% вмісту окислу у склі, складає для окремих окислів у % (за літературними даними):
Nа20 (через соду)............................................ 0,032
Nа20 (через сульфат).................................0,06
К20 (через поташ)............................................ 0,12
В203.................................................................. 0,15
ZnO...............................................................0,04
РЬО (50%)........................................................ 0,14
СаF2.................................................................. до 50
Sе...................................................................... до 90
Нагрівання кремнезему до 1400С не визиває втрат на леткість. Миш'яковистий ангідрид Аз2Оз легко випаровується, якою знаходиться у вільному стані. Під час плавлення шихти втрати миш'яковистого ангідриду при вмісті його менше 0,1% незначні. При змісті більше 0,25% його втрати складають близько 40%. Із шихти селенового рубіну випаровується до 90% металічного селену від заданої у шихті кількості. Менш леткі сполуки селену. У бор силікатних та свинцевих скломасах внаслідок леткості В203 та РЬО їх вміст у поверхневих шарах менше ніж у глибинних. З підвищенням температури варки скла леткість деяких компонентів, у першу чергу лужних окислів, різко зростає.
При підвищенні температури з 1450 до 1600С леткість Ка20 зростає від 0,5 до 1,3%. У сульфатній шихті, леткість якої вище, при підвищенні температури вона зростає від!,] до 1,9%.
2.3. Взаємна розчинність компонентів шихти та їх сполук при нагріванні Випадки обмеженої розчинності досить часті у практиці скловаріння.
Утворення так званих "щолоків" при варці сульфатного скла визвано обмеженою розчинністю деяких сульфатів у силікатних, сплавах. Окис хрому, введена у якості фарбника, розчиняється у розплаві лише до певної кількості (приблизно до 3%).
Розчинність компонентів шихти залежить від температури, тривалості нагрівання та кількісного співвідношення компонент.
Сульфат натрію у розплавленому стані легко розчинне карбонати і хлориди натрію, калію, кальцію та барію, а карбонати натрію та калію розчиняють ті ж хлориди. У розплавленому стані вуглекислий натрій та вуглекислий калій взаємно розчинні; в струмені вуглекислоти той та інший розчиняють вуглекислий кальцій із утворенням подвійних солей, якщо дані солі знаходяться у еквімолекулярних співвідношеннях. Сульфат натрію розчиняє азотнокислий натрій та сірчанокислий калій. Азотнокислий натрій розчиняє вуглекислий натрій та азотнокислий калій.
|
|
|
Як правило, одне силікатне скло легко розчиняє інші. Однак існує ряд бор силікатних скол без свилів та інших неоднорідностей, які представляють собою дві незмішані фази, що здатні, при певній хімічній обробці, виділити одну менш хімічно стійку фазу, зберігаючи при цьому свій склоподібний стан.
Властивості даного класу бор силікатного скла використовуються у техніці для отримання термостійких та хімічно стійких високо кремнеземистих виробів, що містять до 96% SiO2.
2.4. Склоутворення
Наступна за силікатоутворенням стадія скло утворення характеризується тим, що після завершення основних хімічних реакцій у шихті та утворення силікатів натрію, силікатів кальцію та складних силікатів у результаті подальшого підвищення температури, і відповідно, підвищення рухливості атомів і молекул різко зростає швидкість дифузійних процесів і швидкість розчинення кремнезему та силікатів. Завдяки дифузійним процесам, що протікають у розплаві, вирівнюються концентрації розчинів силікатів на різних ділянках, і у першому наближенні утворюється відносно однорідна скломаса.
Швидкість дифузії визначається за формулою:
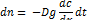
Де dn - кількість речовини, що проходить через площадку q за час dt; D - коефіцієнт дифузії, що дорівнює R*T/(6π*r*N); R - газова стала; Т — абсолютна температура; r-радіус молекули; N - число Авогадро; dc/dх - градієнт концентрації у напрямку координатної вісі, тобто зміна dс концентрації на довжині dх.
Коефіцієнт дифузії залежить від природи дифундуючої речовини та середовища, у якій протікає дифузія, від температури і, в меншій мірі, від концентрації та тиску.
При розчиненні зерен кварцового піску у силікатному розплаві спочатку зурно розчиняється з поверхні а потім відбувається дифузія розчиненої речовини у об'єм розчину. Обидва процеси мають різні швидкості, і кінетика розчинення залежить від співвідношення даних швидкостей.
Якщо швидкість розчинення визначається швидкістю дифузії речовини, що розчиняється, через пограничний шар, тоді
v = (С0-С),
(С0-С),
де v - швидкість розчинення; 8 - товщина пограничного шару розчину; С0 -концентрація насичення у твердій поверхні; С - концентрація в об'ємі розчину.
Величина перехідного шару 8 складає у деяких випадках від 0,02 до 0,05 мм.
Швидкість розчинення зростає з інтенсивністю розміщування.
Підсумовуючи результати великої кількості досліджень по силікато- та скло утворенню, можна зробити наступні висновки:
1. Процеси силікатоутворення у сульфатних шихтах протікають значно складніше, ніж у содових, внаслідок утворення великої кількості стабільних та метастабільних проміжних продуктів.
Важливо, однак, відмітити, що процес силікатоутворен ня у сульфатній шихті можна вважати вдало завершеним, якщо вдалося відновити сульфат натрію до сульфіду і звести до мінімуму залишкову кількість нерозкладеного сульфату натрію.
2. Стадія скло утворення, яку слід розглядати як продовження стадії силікатоутворення, відрізняється від останньої тим, що дифузійні процеси в ній протікають з максимальною інтенсивністю. Процеси розчинення надлишкового кремнезему у силікатах, що утворилися, а також взаємне розчинення силікатів один у одному повинні бути завершені до ступеня, що забезпечує постійність концентрації розчину силікатів в усіх ділянках сплаву. Однорідність останнього може бути порушена лише деякою кількістю газів, що не змогли виділитися із розплаву внаслідок його високої в'язкості.
3. Математичного виразу кінетики процесу скло утворення у повному вигляді поки не знайдено.
Формула для розрахунку швидкості дифузії, а також спеціальні формули, запропоновані для розрахунку швидкості розчинення силікату кальцію у силікаті натрію та для розрахунку швидкості розчинення в залежності від в'язкості розплав), недостатні для розрахунку процесу скло утворення.
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 2708; Нарушение авторских прав?; Мы поможем в написании вашей работы!