
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Железо и его соединение с углеродом
|
|
|
|
Железо – основной компонент сталей и чугунов, важнейших металлических сплавов современной техники. Не случайно наш XX–й век остается веком железным.
20 лет назад – карикатура в газетах: могучий конь (надпись на боку ”химия„ и старая костлявая кляча – „металлургия”). Но жизнь преподала серьезный урок – недооценка роли и значения металлов в н.т.р., что по словам академика Б.Патона спустя годы обернулось досадными просчетами и диспропорциями.
Героические усилия последних лет – и у нас 151млн.т. (1/5 мирового производства, больше, чем где). Но – проблема – экономия. В отходы у нас 20 млн. тонн стали – ежегодно (из них 8 млн. тонн – в стружки).
Техническое железо: ~ 99,8÷99,8% Fe + 0,1÷0,2% примесей (~0,02%С + ~0,1%Cu). Температура плавления технического железа 1539°С. Имеет α и γ полиморфных состояния (см. выше рисунок 11). Στ=250 Мпа, σв=250 Мпа, δ=50%, ψ=85%, HB 80, ρFe=7,86 г/см3.
С углеродом Fe может образовать:
1) твердые растворы
- в α- Fe растворяется 0,02%C (поры кристаллической решетки имеют размер 0,62 A°).
Твердый раствор углерода и других элементов в α- Fe – феррит.
- в γ-Fe – до 2,14%C (поры – 1,02 А°).
Твердый раствор углеродав γ- Fe – аустенит.
2) химическое соединение Fe и C – цементит Fe 3 C (карбид железа). Сложная решетка из октаэдров t °пл. Fe3C=1250°C, %C – 6,67, НВ=800. О Цементит при длительном нагреве может распадаться с образованием свободного C (графита).
2.1 Диаграмма состояния Fe – цементит (метастабильная)
Представлена на рисунке.
ABCD – ликвидус
AHJЕCF – солидус
Фазы: жидкость, Ц – цементит, Ф – феррит, А – аустенит
Таблица – Координаты точек
| точка | t | % C | точка | t | % C |
| А | F | 6.67 | |||
| H | 0.1 | G | |||
| J | 0.16 | P | 0.02 | ||
| B | 0.5 | S | 0.8 | ||
| N | K | 6.67 | |||
| E | 2.14 | Q | 0.01 | ||
| C | 4.3 |
|
|
|
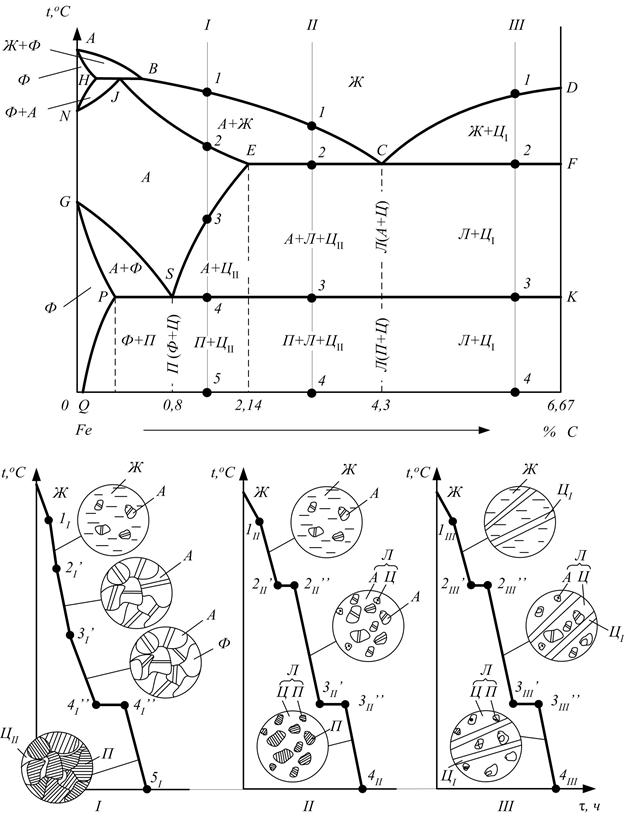
Рисунок 31 – Диаграмма состояния железо – цементит
Остановимся на более детальном рассмотрении диаграммы состояния Fe – C, а точнее диаграмма состояния Fe – Fe 3 C. Fe 3 C (Ц) – цементит это химическое соединение с постоянным составом.
Линия ABCD выше, которой все Fe - C сплавы находятся в жидком состоянии – линия ликвидус (от лат. Liguidus – жидкий, расплавленный).
Линия AHIECF – являющаяся геометрическим местом точек конца затвердевания или кристаллизации Fe - C сплавов, – линия солидус (от лат. Solidus – плотный, твердый). Ниже линии солидус все сплавы находятся в твердом состоянии.
Кроме того, что Fe образует химическое соединение Fe 3 C, оно может существовать в 2-х аллотропических модификациях α и γ (полиморфизм Fe).
Поэтому в системе Fe – Fe 3 C кроме названных выше жидкой фазы и цементита могут существовать такие фазы:
Феррит (Ф) – представляющий собой твердый раствор углерода в α- Fe. Зачастую Ф обозначают α. Ферритной является область GPQ.
Аустенит (А) – твердый раствор углерода в γ-Fe. Может быть обозначен γ. Аустенитная область – GSEA.
В А содержится гораздо больше углерода, чем в феррите – предельно 2,14% и минимум – 0,02% соответственно.
В областях, прилегающих к линии цементита DFKL несомненно будет, имеется цементит (Ц).
В промежуточных областях ACE и GSP используя правила отрезков.
Для всех Fe – C сплавов, содержащих от 2,14 до 6,67 %C, т.е. тех при охлаждении которых пересекаем линию ECF, при t °=1147°C протекает эвтектическая реакция:
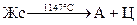 (3)
(3)
Полученную мелкую механическую смесь А и Ц называют эвтектикой (Э) или ледебуритом (Л).
При температуре 727°C все Fe – C сплавы, содержащие 0,02-6,67 %C, т.е. при охлаждении пересекающие линию PSK, претерпевают аналогичное превращение:
 (4)
(4)
Однако, поскольку жидкая фаза отсутствует в этом превращении, а протекает оно в уже затвердевших сплавах, данное превращение называют не эвтектическим, а эвтектоидным. Тонкую механическую смесь Ф + Ц, полученную при 727°C называют эвтектоидом или перлитом (П), т.к. имеет вид перламутра.
|
|
|
Сплавы, содержащие 0 – 0,02%C – техническое железо
0,02 – 2,14%C – стали
2,14 – 6,67%C – чугуны
Стали делятся на до- и заэвтэктоидные; чугуны делятся на до- и заэвтектические.
Следует отметить еще линии СД, SE и PQ.
Линия СД – геометрическое место точек выделения из жидких Fe – C сплавов кристаллов цементита. Поскольку это первые кристаллы цементита, выделяющиеся из жидкости их обозначают Ц I. При дальнейшем охлаждении в интервале температур 1147-727 из А по линии SE выделяются кристаллы Ц II, благодаря падению растворимости углерода в аустените. Аналогично при охлаждении ниже 727°C из феррита выделяются кристаллы Ц III.
На примере сплава Fe – C, допустим заэвтектического чугуна содержащего 5 %C и 95 %Fe, рассмотрим происходящие с ним при охлаждении превращения.
Как правило, превращения, происходящие со сплавом отражают в виде графической зависимости t ° – τ. Суть ее построения – измерение t ° во времени.
- отмечаем сплав I, II, III;
- отмечаем характерные точки пересечения его с линиями диаграммы 1, 2, 3, 4, 5 и переносим их на график t ° – τ;
- проводим кривую охлаждения.
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 758; Нарушение авторских прав?; Мы поможем в написании вашей работы!