
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ион - дипольное взаимодействие. Механизмы образования растворов
Наиболее распространенным в природе растворителем является вода. Она обладает высокой диэлектрической проницаемостью, ε = 83. Диэлектрическая проницаемость - это отношение напряженности электрического поля в вакууме к напряженности поля в однородной изотропной среде при неизменных зарядах, создающих поле. Она показывает, во сколько раз уменьшается сила взаимодействия электрических зарядов при переносе их из вакуума в однородную изотропную среду, если расстояние между зарядами остается неизменным.
Например для эфира ε = 4,3,что существенно ниже, чем в случае воды, т.е. при переносе заряда из вакуума в среду (воду), сила взаимодействия уменьшается в 83 раза, а из вакуума в эфир лишь – в 4,3 раза.
Именно высокая диэлектрическая проницаемость воды является причиной разложения на ионы. При диссоциации происходит химическая реакция взаимодействия иона с молекулой растворителя (воды). Этот процесс называется сольватацией (гидратацией). Если при растворении в воде или другом растворителе энергия гидратации (сольватации) окажется равной или близкой к энергии связей кристаллической решетки, то в этом случае произойдет разрушение кристаллической решетки вещества и начнется процесс растворения и образования гидратированных (сольватированных) ионов.
Схематически это можно выразить следующим образом:

Рис. 4.2 Гидратация иона меди.
С другой стороны, например, в случае с хлористым водородом происходит его взаимодействие с молекулой воды с образованием соляной кислоты и дальнейшей диссоциацией на ионы:
HCl + H 2 O 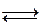 H 3 O + + Cl - (4.з)
H 3 O + + Cl - (4.з)
Таким образом, возможны два механизма образования растворов с одновременной диссоциацией на ионы:
1. если ионы существуют в кристаллической решетке, тогда при растворении в воде (растворителе) гидратная (сольватная) оболочка, стабилизирует существование ионов в растворе (рис. 4.2);
2. если в веществе, находящемся в газообразном, жидком или твердом состоянии ионы отсутствуют, гидратация обеспечивает их диссоциацию и последующую стабилизацию ионов (реакция 4.з).
Подобный механизм образования ионов позволяет утверждать, что они образуются не под действием электрического тока, а уже при растворении. Рассмотренный механизм объясняет их устойчивость в растворах электролитов (см. рис. 4.2).
Теория С.Аррениуса вместе с теорией гидратации (сольватации), разработанной Д.И. Менделеевым, достаточно хорошо описывала поведение растворов электролитов, но только для разбавленных растворов. Как следует из всего вышеизложенного, она основана на ион - дипольном взаимодействии. Именно ион - дипольное взаимодействие объясняет механизм образования растворов и их устойчивость. Учет ион - дипольного взаимодействия позволил существенно развить теорию С.Аррениуса, однако для концентрированных растворов электролитов это оказалось недостаточным.
Для описании их поведения было введено понятие об активности ионов. Активность - это кажущаяся (эффективная) концентрация ионов, которая меньше их концентрации, определенной в растворе
ai = fi Ci, (4.13)
где C i – концентрация иона, ai – его активность; fi – коэффициент активности (безразмерная величина) fi < 1.
Активность зависит от общей ионной силы раствора:
 (4.14)
(4.14)
где Ci – концентрация иона, а Zi – его заряд.
При постоянной ионной силе раствора коэффициенты активности равны. Был введен средний коэффициент активности:
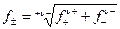 , (4.15)
, (4.15)
 - число катионов и анионов, образующихся при диссоциации электролита.
- число катионов и анионов, образующихся при диссоциации электролита.
Введение коэффициента активности связано с необходимостью создания теории электролитов для концентрированных растворов.
|
|
Дата добавления: 2014-01-13; Просмотров: 1773; Нарушение авторских прав?; Мы поможем в написании вашей работы!