
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гетерогенные равновесия
Термодинамическую систему, все свойства которой во всех точках одинаковы, либо плавно изменяются от точки к точке, называют гомогенной.
Гомогенная система может состоять из нескольких веществ, называемых компонентами. Гомогенными системами являются, например, водные растворы хорошо растворимых солей (NaCl, KCl, Ca(NO3)2) и органических соединений (этилового спирта, уксусной кислоты).
Термодинамическую систему, свойства которой от точки к точке изменяются скачкообразно, называют гетерогенной. Такая система состоит из нескольких гомогенных частей. Гомогенную часть гетеро-генной системы называют фазой. Каждая фаза характеризуется массой, геометрическими размерами, и, главное, наличием границы раздела, отделяющей ее от других фаз.
Гетерогенными системами являются, например, жидкость-пар, твердый осадок-насыщенный раствор, твердое тело-газ.
Равновесия, которые устанавливаются на границе раздела фаз, называют гетерогенными равновесиями.
Произведение растворимости (ПР)
Рассмотрим процессы, возникающие при взаимодействии твердого вещества KtnAnm ионного типа с водой. Под действием растворителя ионы Ktm+ и Аnn- будут переходить в жидкую фазу и одновременно, за счет электростатического притяжения, часть перешедших в раствор ионов вновь будет осаждаться на твердой фазе. Спустя некоторое время в системе установится равновесие, кинетическим условием которого является равенство скоростей процессов растворения и осаждения, а термодинамическим - постоянство свободной энергии Гиббса (DG = 0).
Раствор, находящийся в равновесии с твердой фазой, называют насыщенным.
В водных растворах растворенная часть вещества-электролита, в большинстве случаев, полностью диссоциирует на ионы. Поэтому в системе твердое вещество – насыщенный раствор устанавливается равновесие между осадком и ионами, образовавшимися при диссоциации растворенной части вещества:
|
|
Применив к этому равновесию закон действующих масс, получим выражение для константы равновесия:
 .
.
Таким образом:
В насыщенном растворе малорастворимого сильного электролита при данной температуре произведение молярных концентраций его ионов, возведенных в степени их стехиометрических коэффициентов, есть величина постоянная и называется константой или произведением растворимости.
Произведение растворимости ПР (или 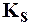 ) количественно харак-теризует растворимость данного вещества при данной температуре:
) количественно харак-теризует растворимость данного вещества при данной температуре:

Величина ПР зависит от природы электролита, растворителя и температуры. С ростом температуры ПР обычно увеличивается, так как при нагревании раствора для большинства твердых веществ характерно увеличение растворимости.
Величина ПР малорастворимого сильного электролита связана с его растворимостью, которую в данном случае выражают как молярную концентрацию электролита в насыщенном растворе:

n, m - стехиометрические коэффициенты т.е. число катионов и анионов.
В некоторых случаях растворимость выражают в г/л. Пересчет можно выполнить при помощи соотношения:

|
|
Дата добавления: 2014-11-06; Просмотров: 408; Нарушение авторских прав?; Мы поможем в написании вашей работы!