
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Правила работы с титрованными растворами
|
|
|
|
– Вся посуда, используемая при работе с титрованными растворами, должна быть безукоризненно чистой;
– бюретку перед заполнением титрованным раствором предварительно нужно промыть дистиллированной водой, а затем два раза ополоснуть титрованным раствором;
– необходимо следить, чтобы в носике бюретки не было пузырьков воздуха или кристаллов вещества;
– титрование из бюретки всегда надо начинать от какого-нибудь определенного деления, лучше всего от нуля;
– во всех измерительных сосудах отсчет проводят по нижней точке мениска при нахождении глаза наблюдателя на одном уровне с краем мениска;
– для более четкого наблюдения мениска к противоположной от наблюдателя стенке сосуда прикладывают белую бумагу;
– при титровании титрант добавляют по каплям, причем носик бюретки должен быть настолько узким, чтобы объем одной капли не превышал 0,03 мл;
– емкость измерительных сосудов от нагревания изменяется, поэтому их необходимо держать вдали от источников тепла;
– при титровании пипеткой для наполнения титрованным раствором пипетку держат большим и средним пальцами за верхний конец. Указательный палец закрывает верхнее отверстие пипетки. Объем отмеривают следующим образом. Набирают в пипетку жидкость выше метки, кончик ее вытирают кусочками фильтровальной бумаги или чистой тряпочкой, доводят уровень жидкости до метки и, прислонив кончик пипетки к стенке конической колбы, промытой дистиллированной водой, дают жидкости стечь. Затем считают до десяти и после этого отводят кончик пипетки от стенки колбы.
Приготовленные титрованные растворы используют для количественного определения фармацевтических субстанций (лекарственных веществ) титриметрическими методами.
|
|
|
Химические реакции, используемые для количественного определения лекарственных средств, должны удовлетворять следующим основным требованиям:
– протекать количественно, т.е. константа равновесия реакции должна быть достаточно велика;
– протекать с большой скоростью;
– не должны осложняться протеканием побочных реакций;
– должны иметь способ индикации окончания реакции.
Для расчета содержания лекарственных веществ по результатам титрования применяют титр титранта по определяемому веществу ( условный титр рабочего раствора; титр рабочего раствора по определяемому веществу; титр-соответствие ).
Титр титранта по определяемому веществу (ТВ/А, мг/мл) показывает массу титруемого ЛВ в милиграммах, которая эквивалентна 1 мл титрованного раствора соответствующей концентрации. Условный титр (ТВ/А) рассчитывают по формуле:
 (9);
(9);
или
 (10)
(10)
где M(В); N(В) – соответственно концентрация титрованного раствора, выраженная в М (моль/л); н. (грамм-эквивалент/л); моль/л УЧ; Mr (А) – молярная масса определяемой фармацевтической субстанции; Э(А) – эквивалентная масса определяемой фармацевтической субстанции, г/моль; Моль(УЧ)А – моль-масса условной частицы (УЧ) титруемой фармацевтической субстанции, г/моль; К(А); К(В) – соответственно стехиометрические коэффициенты определяемой фармацевтической субстанции (ЛВ) и титранта в уравнении реакции количественного определения; 1000 – объем титрованного раствора, содержащего моль; грамм-эквивалент; моль соответствующей УЧ, мл; 1000 – для пересчета массы в мг.
ПРИМЕР: Рассчитайте титр 0,1 М раствора серебра нитрата по натрия бромиду (Мr 102,90).
РЕШЕНИЕ: 

или
fэкв(NaBr) = 1
Э(NаВr) = fэкв∙Мr(A) = 1· 102,9 = 102,9 (г/моль)

ЗАКЛЮЧЕНИЕ: Титр 0,1 М раствора серебра нитрата по натрия бромиду равен 10,29 мг/мл.
ПРИМЕР: Рассчитайте титр 0,1 М раствора серебра нитрата по кальция хлориду (Мr 219,08).
|
|
|
РЕШЕНИЕ:
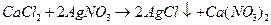

или
fэкв(CaCl2) = 1/2
Э(CaCl2) = fэкв∙Мr(A) = 1/2· 219,08 = 109,54 (г/моль)

ЗАКЛЮЧЕНИЕ: Титр 0,1 М раствора серебра нитрата по кальция хлориду равен 10,95 мг/мл.
Приведенные выше примеры показывают, что титр одного и того же титранта по определяемому веществу является величиной постоянной, но зависящей от молярной массы определяемого вещества. Кроме того, титр титранта по определяемому веществу зависит от типа реакции (реакции замещения, окисления и др.), в которой участвуют определяемое лекарственное вещество и титрант.
В некоторых органических фармацевтических субстанциях, получаемых из ЛРС (например, соли алкалоидов производных тропана: атропина сульфат – (C17H23NО3)2·H2SO4· H2O; морфинана: апоморфина гидрохлорид – C17H17NО2·HCl·3/4H2O; кодеина фосфат – C18H21NО3·H3PO4·1,5H2O и др.), допускается содержание определенного количества остаточной влаги.
В то же время количественное содержание действующего вещества в фармацевтической субстанции согласно ФС нормируется в пересчете на сухой (если определяется потеря в массе при высушивании) или безводный (если определяется содержание воды по методу К.Фишера) анализируемый образец.
При необходимости расчета титра по определяемому веществу (ТВ/А) в пересчете на сухое/безводное вещество используют формулу:
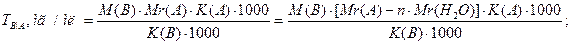 (11)
(11)
или

где Мr (А) – молярная масса фармацевтической субстанции, г/моль; n – количество молекул воды в анализируемой фармацевтической субстанции согласно брутто–формуле; Мr (H2O) – молярная масса воды, г/моль.
ПРИМЕР: Рассчитайте титр 0,1 М раствора хлорной кислоты по морфина гидрохлориду (Mr C17H19NО3·HCl·3H2O 375,85; Mr H2O 18,0) в пересчете на безводное вещество.
РЕШЕНИЕ:
2(C17H19NО3·HCl·3H2O) +2HClO4 +Hg(CH3COO)2 → HgCl2+
A B
+2CH3COOH+2(C17H19NО3·HClO4·3H2O)

|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 3863; Нарушение авторских прав?; Мы поможем в написании вашей работы!