
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гематологическая картина ЖДА
Железодефицитные анемии (ЖДА)
Дисгемопоэтические анемии
Острая постгеморрагическая анемия (ОПГА)
Острая постгеморрагическая анемияявляется осложнением массивных кровотечений 2 - 3 степени тяжести (кровопотеря 20 - 30%) и проявляется обычно на 4 - 5 сутки. К этому времени в крови нарастает содержание клеток физиологической регенерации эритроцитов – ретикулоцитов (>1%). По этой причине анемию относят к гиперрегенераторной. Цветовой показатель, обычно, не снижается и ее считают нормохромной. В отдельных случаях она может носить гипохромный характер. Общее количество лейкоцитов и тромбоцитов в единице объема крови сниженается из-за компенсаторной гемодилюции.
Принципые терапии ОПГА заключаются в срочном восстановлении ОЦК плазмозаменителями, поддержании деятельности сердечнососудистой системы и переливании цельной одногруппной крови или эритроцитарной массы для устранения гипоксии. Эритропоэз стимулируют эритропоэтином, препаратами железа, пиридоксином, цианокобаламином, аскорбиновой кислотой.
Этиология ЖДА. На долю ЖДА приходится 80% всех зарегистрированных случаев малокровия, что составляет примерно 300 млн. человек (ВОЗ). В 80-90% случаев она возникает при повторных необильных, скрытых кровотечениях и носит название хроническая постгеморрагическая ЖДА. Наиболее частыми причинами подобных кровотечений являются геморрой, эрозии слизистой пищевода, язвенная болезнь желудка и двенадцатиперстной кишки. У женщин в этиологии доминируют дисфункциональные маточные кровотечения - метроррагии, а у девочек в подростковом периоде - появление менструальных кровотечений и угнетение синтеза гема возросшей продукцией эстрогенов. Из-за интенсивного истощения депо железа, не восполняемого извне, ЖДА обнаруживается у 90% женщин к концу беременности. Она развивается также при наследственном или приобретенном дефиците плазменного транспортера железа – трансферрина. При отсутствии железа в пище или его невсасывание по причине ахлоргидрии или резекции проксимальных отделов ЖКТ, развивается ее алиментарный вариант. Некоторые продукты питания ухудшают всасывание железа из-за образования с ним нерастворимых комплексов. Так альбумины молока образуют альбуминаты железа, а таннин чая – его таннаты. К таким же последствиям может привести бесконтрольное пероральное применение некоторых лекарственных средств: дубящих, адсорбирующих, обволакивающих, препаратов кальция, фосфатов, тетрациклина и др.
Патогенез ЖДА. По мере истощения лабильного депо железа в гепатоцитах, все более угнетается синтеза гема в гемоглобине. Одновременно снижается активность большой группы железосодержащих внутриклеточных ферментов: дегидрогеназ, цитохромов, каталаз и пероксидаз, что ухудшает эффективность клеточного дыхания, сопряженного с ним синтеза макроэргов и антиоксидантную защиту клеток. Эти факторы подавляют эритропоэз и осмотическую резистентность эритроцитов, которые, повышенно разрушаясь, усугубляют патологию. В результате эритропоэз становится неэффективным, гипорегенераторным: в периферической крови уменьшается количество нормоцитов, и появляются дегенеративные эритроциты: пойкило - и анизоциты с доминированием микроцитоза (Рис. 21) и гипохромии (Ц.п. < 0,86).
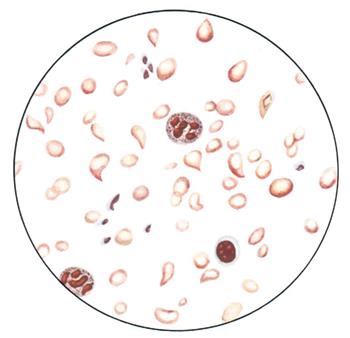
Рис.21. Видны резкие дегенеративные изменения эритроцитов; гипохромия; анизо - и пойкилоцитоз, шизоцитоз - мелкие обрывки.
Если содержание гемоглобина в крови снижается до 6,8 - 6,6 ммоль/л, то ЖДА считают легкой степени тяжести, а менее 4,3 ммоль/л – тяжелой.
Тяжелая ЖДА сопровождаются ухудшением всего гемопоэза и проявляется дегенеративной панцитопенией. Ей часто сопутствует иммунодефициты, обусловленные незавершенным фагоцитозом, снижением синтеза иммуноглобулинов и падением активности факторов неспецифической антибактериальной защиты – лизоцима и β-лизина. На их фоне легко возникают и тяжело протекают инфекционные заболевания.
ЖДА формирует гемическую, а затем и тканевую гипоксию, которые усугубляют неэффективность гемопоэза, и вызывают значительные обменные и функциональные расстройства в высокоаэробозависимых клетках эпителия слизистых, кардиомиоцитах, нейронах.
Течение ЖДА - рецидивирующее. Периоды обострений проявляются бледностью кожи, слабостью, быстрой физической утомляемостью. Часты головокружения, шум в ушах. Возможны обмороки. Дыхание частое, поверхностное. Обнаруживается тахикардия и признаки левожелудочковой гипертрофии. В ротовой полости возникают воспалительно-дистрофические изменения. Больные обращают внимание на ломкость и искривление ногтей, выпадение волос. Эти явления связаны не только с дефицитом железа, но и с дефицитом витаминов: пиридоксина и цианокобаламина, потребление которых в ходе компенсаторно возросшего эритропоэза увеличивается. Для анемии специфично извращение вкуса, пристрастие к мелу, известке.
Принципы терапии ЖДАзаключаются в устранении основного заболевания, вызвавшего железодефицит. В качестве патогенетической терапии используются препараты железа, стимуляторы эритро - и гемопоэза, витамины группы В. Лучшему усвоению железа способствует приём желудочного сока, разведенной хлороводородной кислоты, углекислых минеральных вод (Ессентуки-17, Пятигорские источники 14, 17). При тяжёлой гипоксии показана гемотрансфузия. Для нормализации сердечной деятельности применяют сердечные гликозиды.
17.2.3.2. В12 и фолиево-дефицитная (мегалобластная) анемия
Этиологией мегалобластной, пернициозной (злокачественной) анемии Аддисона-Бирмера(ПА)является дефицит цианокобаламина, обусловленный отсутствием фактора Кэстла, необходимого для всасывания витамина. Наиболее часто дефицит этого гастромукопротеина возникает после резекции желудка и хроническом аутоиммунном атрофическом гастрите (более чем у 90% пациентов с ПА в сыворотке крови обнаруживаются антитела класса IgG к париетальным клеткам и у 60% - к гастромукопротеиду). В редких случаях возникновение ПА связано с наследственной недостаточностью транскобаламина-2, транспортирующего витамин В12 в печень и костный мозг. Причиной мегалобластной анемии может быть также дефицит фолиевой кислоты, развивающийся в течение трех недель после прекращения ее поступления в организм с пищей. Как правило, это происходит с алкоголиками, наркоманами и пожилыми людьми по причине низкого потребления свежих фруктов и овощей. Дефицит фолата возникает также при повышенной в нем потребности при беременности и потерях - при гемодиализе. Ряд лекарственных препаратов - антагонистовфолацина: пентамидин, триметоприм, триамтерен и др. и ингибиторовсинтеза ДНК: азатиоприн, 6-меркаптопурин, 5-фторурацил, цитозин и др. – способны вызвать этот вид анемии.
Патогенез. При всем многообразии причин мегалобластной анемии основу ее патогенезасоставляет нарушение превращения неактивной фолиевой кислоты в ее активный метаболит - тетрагидрофолиевую (фолиниевую) кислоту. Этот процесс осуществляется группой В12-зависимых внутриклеточных ферментов. Далее тетрагидрофолат используется всеми клетками организма для синтеза пуриновых и пиримидиновых нуклеотидов. Таким образом, оба витамина являются синергистами и их нехватка результирует одни и теже последствия - замедление синтеза ДНК с частичной заменой тиминовых нуклеотидов на уридиновые. Образующаяся при этом нестабильная и дефектная ДНК способна лишь к частичной репликации в S-фазе клеточного цикла и поэтому тормозит завершение митоза. Клетки как бы «застревают» в интерфазе. В ходе эритропоэза эта аномалия препятствует нормальной пролиферации и дифференциации эритроидных клеток–предшественниц. В них развивается я дерно-цитоплазматическая асинхрония, проявляющаяся замедлением образования нормоцитов и повышением образования мегалобластов и мегалоцитов – крупных клеток, насыщенных незрелым гемоглобином (Рис. 22, 23).
|
|
Дата добавления: 2014-11-06; Просмотров: 435; Нарушение авторских прав?; Мы поможем в написании вашей работы!