
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ізохоричний процес
139. Яка із формул характеризує ізохоричний процес? Дайте його визначення.
а) 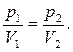 б)
б) 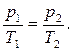 в)
в) 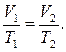 г)
г) 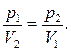 д)
д) 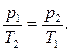
140. Закон Шарля для ізохоричного процесу має такий вигляд:
а) 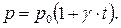 б)
б)  в) V=V 0×(1+ α×t). г)
в) V=V 0×(1+ α×t). г) 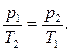 д)
д) 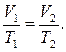
141. До якої температури t 20С треба охолодити повітря, яке міститься у герметичній посудині при температурі t 1 = 210С, щоб тиск газу р зменшився вдвічі?
а) t 2=-840С. б) t2 =-420С. в) t 2=-210С. г) t 2=-1260С. д) t 2=-630С.
142. В балоні при температурі t 1=7°С знаходився газ під тиском p 1=100 кПа. Балон охолодили, і тиск зменшився до p 2=80 кПа. На скільки градусів D T знизилась температура газу?
а) D T =92 К. б) D T =128 К. в) D T =56 К. г) D T =164 К. д) D T =212 К.
143. Балон містить газ під тиском р 1=0,1 МПа при температурі Т 1=250 К. На скільки збільшиться тиск у балоні D р, якщо температуру підвищити на D Т= 100 К?
а)D р =100 кПа. б)D р =60 кПа. в)D р =120 кПа. г)D р =80 кПа. д)D р =40 кПа.
144. В балоні міститься газ при температурі Т 1=280 К. Його нагрівають на D Т =70 К, і його тиск збільшується на D р =600 кПа. Визначити початковий тиск газу р 1.
А) р 1=1,2 МПа б) р 1=2,4 МПа в) р 1=3,6 МПа г) р 1=4,8 МПа д) р 1=6,0 МПа
145. При якій температурі t 10C знаходився газ у закритій посудині, якщо при його нагріванні на D t= 140°C тиск р 1 в посудині зросте у 1,5 рази?
а) t 1 = 7°С. б) t 1 = 21°С. в) t 1 = 14°С. г) t 1 = 35°С. д) t 1 = 28°С.
146. У замкнутій посудині знаходиться ідеальний газ. При температурі t 1=0°С його тиск p 1 становив 10 Па. Яким стане його тиск р 2 при температурі t 2=273°С?
а) р 2=35 Па. б) р 2=30 Па. в) р 2=25 Па. г) р 2=20 Па. д) р 2=15 Па.
147. До якої температури Т 2 нагріли балон із газом, якщо його тиск р збільшився вдвічі, а початкова температура газу t 1 дорівнювала 240С?
а) Т 2=467 К. б) Т 2=376 К. в) Т 2=594 К. г) Т 2=48 К. д) Т 2=282 К.
148. У замкнутій посудині знаходиться ідеальний газ при температурі t 1=00С і тиску p 1=200 Па. Яким буде тиск газу p 2 при температурі t 2 = 2730С?
а) р 2=700 Па. б) р 2=400 Па. в) р 2=500 Па. г) р 2=300 Па. д) р 2=600 Па.
149. Тиск газу p 1 усередині закритої пляшки при температурі T 1=273 К дорівнював 320 Па. При нагріванні її до температури T 2 = 450 К пробка із пляшки вилетіла. Визначте, при якому тиску p 2 це відбулось?
а) p 2=712 Па. б) p 2=476 Па. в) p 2=384 Па. г) p 2=638 Па. д) p 2=527 Па.
150. До якої температури Т 2 треба нагріти повітря, яке міститься у герметичній посудині при температурі t 1 0 =200С, щоб тиск газу р 1 збільшився втричі?
а) Т 2=254 К. б) Т 2=879 К. в) Т 2=646 К. г) Т 2=60 К. д) Т 2=487 К.
151. У замкнутій посудині сталого об'єму знаходиться ідеальний газ. При температурі t 1=50°С його тиск p 1 дорівнював 100 Па. Яким стане його тиск р 2 при температурі t 2=323°С?
а) p 2=186 Па. б) p 2=279 Па. в) p 2=311 Па. г) p 2=234 Па. д) p 2=142 Па.
152. Тиск газу p 1 усередині закритої пляшки при температурі T 1=290 К становив 145 Па. При нагріванні до температури T 2=320 К пробка із пляшки вилетіла. Визначити, при якому тиску p 2 це сталося.
а) p 2=170 Па. б) p 2=190 Па. в) p 2=150 Па. г) p 2=160 Па. д) p 2=180 Па.
Ідеальний газ
153. Яка властивість газу міститься у терміні “ ідеальний газ ”?
а) газ, у якому відсутнє внутрішнє тертя. г) газ при кімнатній температурі.
б) газ, у якому присутнє внутрішнє тертя. д) газ при дуже високому тиску.
в) газ при температурах близьких до абсолютного нуля.
154. Який газ називають “ ідеальним ”?
а) газ, який знаходиться при не дуже низькій температурі..
б) зіткнення молекул якого та зі стінками посудини абсолютно пружні.
в) розмірами молекул якого і силами взаємодії між ними можна знехтувати.
г) газ, який знаходиться при дуже високому тиску.
д) газ, який знаходиться при сталому об‘ємі.
155. Який вислів на вашу думку є правильним?
а) Об’єм газу завжди менший за об’єм посудини, в якій він знаходиться.
б) Об’єм газу, не завжди співпадає iз об’ємом своєї посудини.
в) Об’єм газу завжди більший за об’єм посудини, в якій він знаходиться.
г) Об’єм газу завжди співпадає із об’ємом посудини, в якій він знаходиться.
д) Немає правильної відповіді.
156. Який вигляд має закон Клайперона-Менделєєва? Поясніть його зміст.
а) р 1 ×V 1 =р 2 ×V 2. б) 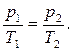 в)
в) 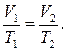 г)
г)  д)
д) 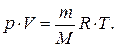
157. Яка із приведених формул є рівнянням стану ідеального газу для кількості одного його моля?
а) 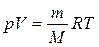 . б)
. б)  . в)
. в) 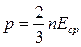 . г)
. г) 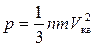 . д) p=n×k×T.
. д) p=n×k×T.
158. Яка із приведених формул є рівнянням стану ідеального газу для кількості одного його кіломоля?
а) 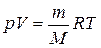 . б)
. б) 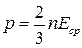 . в)
. в)  . г)
. г)  . д)
. д)  .
.
159. Яка із формул є рівнянням стану ідеального газу для довільної його кількості?
а) 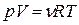 . б)
. б) 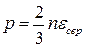 . в)
. в) 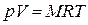 . г)
. г) 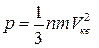 . д)
. д) 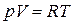 .
.
160. Газ нагрівається при сталому тиску. Як змінюється при цьому його густина r від температури Т? Поясніть.
а) r~T. б) r~ 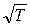 . в) r= const. г) r~Т 2. д) r~
. в) r= const. г) r~Т 2. д) r~ 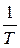 .
.
161. Яка із формул є рівнянням стану ідеального газу для будь-якої довільноїйого кількості? Поясніть його зміст.
а) 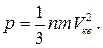 б)
б)  в)
в) 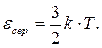 г)
г) 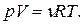 д)
д) 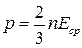 .
.
162. Укажіть розмірність універсальної газової сталої R.
а) 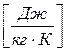 . б)
. б) 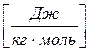 . в)
. в) 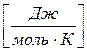 . г)
. г) 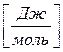 . д)
. д) 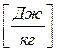 .
.
163. Яка із наведених формул висловлює закон Дальтона? Сформулюйте його.
а) р=∑рі. б) ν=N/NA. в) 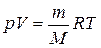 . г)
. г) 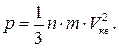 д)
д) 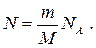
164. Закон Дальтона має вигляд: (Сформулюйте його).
а) 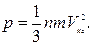 б) р=р 1 +р 2 +...+рn. в)
б) р=р 1 +р 2 +...+рn. в) 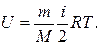 г)
г) 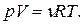 д)
д) 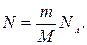
165. Укажіть невірну розмірність для універсальної газової сталої R:
а) 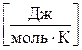 . б)
. б) 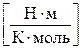 . в)
. в) 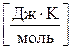 . г)
. г) 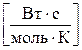 . д)
. д) 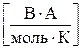 .
.
166. Укажіть вірну розмірність універсальної газової сталої R.
а) 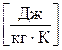 . б)
. б) 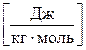 . в)
. в) 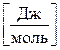 . г)
. г) 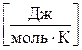 . д)
. д) 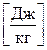 .
.
167. Укажіть невірну розмірність для універсальної газової сталої R.
а) 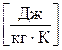 . б)
. б) 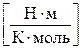 . в)
. в) 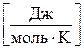 . г)
. г)  . д)
. д) 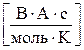 .
.
168. Укажіть вірну розмірність для сталої Больцмана k.
а) 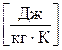 . б)
. б) 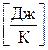 . в)
. в) 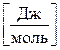 . г)
. г) 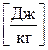 . д)
. д) 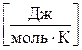 .
.
169. Укажіть невірну розмірність для сталої Больцмана k.
а) 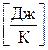 . б)
. б) 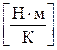 . в)
. в) 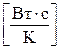 . г)
. г) 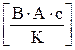 . д)
. д) 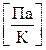 .
.
170. Який із приведених газів має найбільшу густину r при однакових тиску р і температурі Т?
а) Водень. б) Азот. в) Метан. г) Кисень. д) Гелій.
171. Який із перелічених газів має найменшу густину r, якщо температура Т і тиск р газів однакові?
а) Кисень. б) Метан. в) Азот. г) Вуглекислий газ. д) Водень.
172. Чому дорівнює концентрація молекул ідеального газу n, якщо його температура t =270С, а тиск p= 1 Па? (Стала Больцмана k= 1,38×10-23 Дж/К).
а) n =4,3×1021 м-3. б) n =2,4×1020 м-3. в) n =1,5×1018 м-3. г) n =6,4×1017 м-3. д) n =8,1×1019 м-3.
173. Визначте концентрацію молекул ідеального газу n, якщо його температура t= 780С, а тиск p =12 Па. (Стала Больцмана k= 1,38×10-23 Дж/К).
а) n =4,3×1020 м-3. б) n =5,4×1018 м-3. в) n =2,5×1021 м-3. г) n =7,2×1017 м-3. д) n =9,6×1019 м-3.
174. Визначте концентрацію молекул ідеального газу n при температурі t= 90С і тиску p= 0,2 Па. (Стала Больцмана k= 1,38×10-23 Дж/К).
а) n =5,1×1019 м-3. б) n =1,8×1021 м-3. в) n =3,2×1020 м-3. г) n =6,3×1018 м-3. д) n =7,6×1017 м-3.
175. Тиск ідеального газу р =2×10-3 Па, а концентрація його молекул n =2×1016 м-3. Визначити температуру газу Т. (Стала Больцмана k= 1,38×10-23 Дж/К).
а) Т= 5178 К. б) Т= 3894 К. в) Т= 6732 К. г) Т= 4245 К. д) Т= 7246 К.
176. Який із приведених газів має найменшу густину r при однакових температурі Т і тиску р?
а) Кисень. б) Азот. в) Метан. г) Водень. д) Гелій.
177. Який із перелічених газів має найбільшу густину r при однакових тиску р та температурі Т?
а) Вуглекислий газ. б) Аргон. в) Вуглець. г) Аміак. д) Водень.
178. Газ нагрівається при сталому тиску. Як змінюється густина газу r зі зміною його температури Т?
а) r~Т. б) r~ 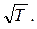 в) r~
в) r~ 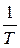 . г) r= const. д) r~Т 2.
. г) r= const. д) r~Т 2.
179. Визначте концентрацію молекул ідеального газу n при температурі t =1270С і тиску p =10 Па. (Стала Больцмана k= 1,38×10-23 Дж/К).
а) n =2,4×1020 м-3. б) n =1,8×1021 м-3. в) n =7,2×1019 м-3. г) n =4,6×1022 м-3. д) n =9,3×1018 м-3.
180. Чому дорівнює концентрація молекул ідеального газу n, якщо його температура t= 540С, а тиск p= 4 Па? (Стала Больцмана k= 1,38×10-23 Дж/К).
а) n =4,2×1021 м-3. б) n =2,7×1022 м-3. в) n =1,8×1018 м-3. г) n =6,5×1019 м-3. д) n =8,9×1020 м-3.
181. Визначте концентрацію молекул ідеального газу n при температурі t =640С і тиску p= 16 Па. (Стала Больцмана k= 1,38×10-23 Дж/К).
а) n =3,4×1021 м-3. б) n =1,6×1018 м-3. в) n =5,4×1020 м-3. г) n =4,8×1022 м-3. д) n =7,2×1019 м-3.
182. Визначте концентрацію молекул ідеального газу n при температурі t= 870С і тиску p= 0,6 Па. (Стала Больцмана k= 1,38×10-23 Дж/К).
а) n =2,4×1019 м-3. б) n =8,7×1018 м-3. в) n =3,9×1021 м-3. г) n =1,2×1020 м-3. д) n =5,6×1022 м-3.
183. Тиск ідеального газу р =6×10-2 Па, а концентрація його молекул n =4×1018 м-3. Визначити температуру цього газу Т. (Стала Больцмана k= 1,38×10-23 Дж/К).
а) Т= 2148 К. б) Т= 1087 К. в) Т= 967 К. г) Т= 2452 К. д) Т= 1746 К.
184. У балоні міститься газ при температурі Т =200 К, а концентрація його молекул n =25 моль/м3. Визначте тиск газу р. (Стала Больцмана k= 1,38×10-23 Дж/К).
а) р= 1,4 103 Па. б) р= 5,6 105 Па. в) р= 4,2 104 Па. г) р= 8,7 103 Па. д) р= 9,8 104 Па.
185. Яким буде тиск ідеального газу р 2 при одночасному збільшенні його об'єму V і абсолютної температури T у 2 рази, якщо початковий тиск був р 1 = 100 Па?
а) р 2=100 Па. б) р 2=50 Па. в) р 2=250 Па. г) р 2=200 Па. д) р 2=150 Па.
186. Визначте густину кисню r, який знаходиться під тиском р =250 кПа та температурі Т =250 К. (Молярна маса кисню М =32×10-3 кг/моль).
а) r =1,42 кг/м3. б) r =2,54 кг/м3. в) r =1,96 кг/м3. г) r =4,78 кг/м3. д) r =3,85 кг/м3.
187. На деякій висоті тиск повітря р становить 83,1 кПа, а температура Т =290 К. Яка густина повітря r на цій висоті, якщо його молярна маса М =29×10-3 кг/моль?
а) r =0,1 кг/м3. б) r =0,5 кг/м3. в) r =1,0 кг/м3. г) r =1,5 кг/м3. д) r =2,0 кг/м3.
188. Знайти густину r азоту при температурі t =770С та тиску p =166 кПа, якщо його молярна маса М =28×10-3 кг/моль.
а) r =0,8 кг/м3. б) r =1,6 кг/м3. в) r =2,4 кг/м3. г) r =2,0 кг/м3. д) r =1,2 кг/м3.
189. Визначити температуру аміаку t масою m =3 кг, який утримується у балоні об'ємом V =0,83 м3 під тиском p =4,8×105 Па. Відповідь надати у °С. (Молярна маса аміаку М =17×10-3 кг/моль).
а) t =-10°С. б) t =+1°С. в) t =0°С. г) t =-1°С. д) t =+10°С.
190. У посудині об'ємом V= 8,3 л знаходиться газ при температурі t =27°С. Внаслідок витікання газу, тиск в посудині знизився на D p= 600 кПа. Скільки молів газу D n вийшло при цьому із посудини? Температуру вважати незмінною.
а) D n =8 моль. б) D n =2 моль. в) D n =4 моль. г) D n =1 моль. д) D n =6 моль.
191. Визначити температуру t азоту у °С, якщо при тиску р =0,2 МПа його густина r =2,41 кг/м3. Відповідь заокруглити до цілого числа. (М =28×10-3 кг/моль).
а) t= 7°С. б) t= 21°С. в) t= 35°С. г) t= 14°С. д) t= 28°С.
192. Визначити густину ртутної пари r при температурі t =527°С та тиску p =831 Па. Молярна маса ртутної пари М =0,2 кг/моль.
а) r =125 г/м3. б) r =50 г/м3. в) r =25 г/м3. г) r =100 г/м3. д) r =75 г/м3.
193. Знайти тиск p кількості n= 1 кмоль газу, якщо при температурі t= 28°С його об'єм V становив 1 м3.
а) р= 0,5 МПа. б) р= 3,0 МПа. в) р= 1,5 МПа. г) р= 2,5 МПа. д) р= 2,0 МПа.
194. Газ, який має тиск р 1=810 кПа і температуру t 1=12°С, займає об'єм V 1=855 л. Яким буде тиск газу p 2, якщо така сама його маса m при температурі T 2=320 К займе об'єм V 2=800 л?
а) p 2=675 кПа б) p 2=763 кПа в) p 2=854 кПа г) p 2=598 кПа д) p 2=972 кПа
195. У відкачаному об'ємі між скляними стінками термосу тиск р становить 10-2 Па. Скільки молекул газу n міститься у 1 см3 при вказаному тиску і температурі t =27°С? (Стала Больцмана k= 1,38×10-23 Дж/К).
а) n =1,2·1013 см-3. б) n =2,4·1012 см-3. в) n =4,8·1014 см-3. г) n =7,2·1016 см-3. д) n =3,6·1015 см-3.
196. Скільки молекул повітря N міститься в кімнаті розмірами V =8´6´4 м3 при температурі t =220С та тиску p =100 кПа? (Стала Больцмана k= 1,38×10-23 Дж/К).
а) N =3,8·1015. б) N =8,1·1016. в) N =4,7·1014. г) N =6,3·1018. д) 2,4·1017.
197. У міжзоряному просторі міститься приблизно N= 1 атом водню у об¢ємі V= 1 см3, а температура газу T становить 125 К. Визначте тиск p міжзоряного газу.
а) р= 1,7·10-15 Па. б) р= 4,6·10-13 Па. в) р= 3,5·10-16 Па. г) р= 2,8·10-12 Па. д) р= 6,4·10-14 Па.
198. Який тиск p здійснює газ на стінки посудини, якщо у об¢ємі V= 1 см3 його міститься N= 106 молекул, а температура газу t =870С? (k= 1,38×10-23 Дж/К).
а) р= 1,9·10-17 Па. б) р= 7,4·10-12 Па. в) р= 2,7·10-15 Па. г) р= 5,3·10-13 Па. д) р= 8,6·10-14 Па.
199. Вважаючи повітря ідеальним газом, визначте концентрацію n його молекул при нормальних умовах (p 0 = 1,01×105 Па і T 0 = 273 К). (k= 1,38×10-23 Дж/К).
а) n =5,4·1013 м-3. б) n =2,7·1015 м-3. в) n =1,3·1017 м-3. г) n =8,2·1014 м-3. д) n =4,6·1016 м-3.
200. Визначити густину r двохатомного кисню при тиску p =5 МПа і температурі T =296 К. (Молярна маса кисню М =32×10-3 кг/моль).
а) r =95 кг/м3. б) r =80 кг/м3. в) r =35 кг/м3. г) r =50 кг/м3. д) r =65 кг/м3.
201. На деякій висоті над поверхнею Землі атмосферний тиск повітря p =83 кПа, а його температура T =250 К. Обчисліть густину повітря r на цій висоті, якщо його молярна маса М =29×10-3 кг/моль.
а) r =1,2 кг/м3. б) r =3,6 кг/м3. в) r =6,0 кг/м3. г) r =2,4 кг/м3. д) r =4,8 кг/м3.
202. Тиск азоту у посудині р =4 МПа, а його густина складає при цьому r =45 кг/м3. Визначте, якою була його температура Т? (Молярна маса азоту М =28×10-3 кг/моль).
а) Т= 325 К. б) Т= 250 К. в) Т= 300 К. г) Т= 275 К. д) Т= 350 К.
203. Визначте тиск р, який здійснює на стінки посудини кількість n =4 кмоль ідеального газу, якщо його температура T =300 К, а об¢єм V =4 м3.
а) р= 3,0 МПа. б) р= 2,5 МПа. в) р= 4,0 МПа. г) р= 3,5 МПа. д) р= 5,0 МПа.
204. Визначте тиск р, який здійснює на стінки посудини двохатомний водень при температурі t= 270С, якщо його густина при цьому r =4,8 кг/м3, а молярна маса М =2×10-3 кг/моль.
а) р= 3,5 МПа. б) р= 5,0 МПа. в) р= 4,5 МПа. г) р= 6,0 МПа. д) р= 5,5 МПа.
205. У балоні об¢ємом V= 10 л знаходиться сухе повітря під тиском p 1 = 100 кПа і при температурі T 1 = 273 К. У нього заливають воду масою m= 3 г і нагрівають до температури T 2 = 373 К. Визначте загальний тиск суміші pсум, що установиться у балоні. Молярні маси повітря М 1=29×10-3кг/моль, водяної пари М 2=18×10-3кг/моль.
а) pсум =137 кПа. б) pсум =211 кПа. в) pсум =94 кПа. г) pсум =152 кПа. д) pсум =189 кПа.
206. Визначте масу азоту m, який знаходиться у балоні об¢ємом V =56 л під тиском p =3 МПа при температурі t= 130С. (Молярна маса азоту М =28×10-3 кг/моль).
а) m =2,0 кг. б) m =1,5 кг. в) m =3,0 кг. г) m =2,5 кг. д) m =1,0 кг.
207. Густина неону r у балоні неонової лампи дорівнює 0,05 кг/м3 при тиску p =5 кПа. Визначте температуру неону T, молярна маса якого М =20×10-3 кг/моль.
а) Т= 287 К. б) Т= 241 К. в) Т= 273 К. г) Т= 304 К. д) Т= 326 К.
208. Визначити найменший об¢єм балону V, який містить масу m= 6,5 кг кисню, якщо його стінки при температурі t= 200С витримують максимальний тиск p =17 МПа. Молярна маса кисню М =32×10-3 кг/моль.
а) V =16 л. б) V =42 л. в) V =29 л. г) V =34 л. д) V =23 л.
209. Під яким тиском p знаходиться вуглекислий газ у балоні об¢ємом V =2 л при температурі t =370С, якщо до заповнення балон мав масу m 1 = 4,2 кг, а після нього m 2 = 5,6 кг? (Молярна маса вуглекислого газу М =44×10-3 кг/моль).
а) р= 22 МПа. б) р= 35 МПа. в) р= 16 МПа. г) р= 28 МПа. д) р= 41 МПа.
210. При температурі t 1 = 150С і тиску p 1 = 13,3 кПа газ займав об¢єм V 1 = 2 л. Яким стане його тиск p 2, якщо температуру підвищити до t 2 = 300С, а об¢єм зменшити до V 2 = 1,5 л?
а) p 2=26,4 кПа. б) p 2=35,5 кПа. в) p 2=11,6 кПа. г) p 2=18,7 кПа. д) p 2=42,1 кПа.
211. У балоні міститься газ при температурі T =20 К, а концентрація його молекул n =5×1023 м-3. Визначте тиск цього газу р. Стала Больцмана k= 1,38×10-23 Дж/К.
а) р= 214 Па. б) р= 138 Па. в) р= 89 Па. г) р= 176 Па. д) р= 63 Па.
212. Під тиском р 1 = 250 кПа і при температурі Т 1 = 250 К кисень займав об'єм V 1 = = 1,66 м3. Якою стане густина кисню r, якщо його об'єм збільшиться до V 2 = 8 м3? Молярна маса кисню М =32×10-3 кг/моль.
а) r =0,8 кг/м3. б) r =1,6 кг/м3. в) r =3,9 кг/м3. г) r =2,7 кг/м3. д) r =0,4 кг/м3.
213. На деякій висоті над поверхнею Землі тиск повітря р =78 кПа, а його температура Т= 265 К. Визначте густину повітря r на цій висоті. (М =29×10-3 кг/моль).
а) r =1,76 кг/м3. б) r =0,92 кг/м3. в) r =1,54 кг/м3. г) r =1,03 кг/м3. д) r =2,11 кг/м3.
214. Визначити густину водню r при температурі t= 54°С та тиску p =0,2 МПа. Молярна маса водню М =2×10-3 кг/моль. Молярна газова стала R =8,31 Дж/моль∙К.
а) r =0,25 кг/м3. б) r =0,3 кг/м3. в) r =0,15 кг/м3. г) r =0,2 кг/м3. д) r =0,1 кг/м3.
215. Визначте температуру T метану масою m= 1,5 кг, який утримується у балоні об'ємом V= 80 л під тиском p= 5,4 МПа. Молярна маса метану М =16×10-3 кг/моль.
а) Т= 347 К. б) Т= 619 К. в) Т= 286 К. г) Т= 194 К. д) Т= 555 К.
216. Визначте густину ртутної пари r при температурі Т= 384 К і тиску p =1 кПа. Молярна маса ртутної пари M =0,24 кг/моль. (Газова стала R =8,31 Дж/моль∙К).
а) r =150 г/м3. б) r =75 г/м3. в) r =50 г/м3. г) r =125 г/м3. д) r =100 г/м3.
217. Визначте температуру кисню Т, якщо при тиску p= 236 кПа його густина r= =1,98 кг/м3. (Молярна маса кисню М =32×10-3 кг/моль, R =8,31 Дж/моль∙К).
а) Т= 459 К. б) Т= 287 К. в) Т= 194 К. г) Т= 368 К. д) Т= 512 К.
218. Знайти тиск p кількості n= 4 кмоль ідеального газу, якщо при температурі T = =328 К, його об'єм V становить 2 м3. (Молярна газова стала R =8,31 Дж/моль×К).
а) р= 2,79 кПа. б) р= 4,28 кПа. в) р= 1,63 кПа. г) р= 5,45 кПа. д) р= 3,84 кПа.
219. У посудині об'ємом V= 100 см3 міститься газ при температурі t= 27°С. Визначте, на скільки знизиться тиск газу в посудині D p внаслідок витікання iз неї D N= 1020 молекул газу.
а)D p =5,6 кПа. б)D p =3,4 кПа. в)D p =1,9 кПа. г)D p =2,7 кПа. д)D p =4,1 кПа.
220. Газ, який мав тиск p 1 = 540 кПа і температуру t 1 = 24°С, займав об'єм V 1 = 72 л. Яким стане його тиск p 2, якщо та сама маса газу при температурі T 2 = 328 К зай-ме об'єм V 2 = 64 л?
а) p 2=484 кПа. б) p 2=296 кПа. в) p 2=671кПа. г) p 2=319 кПа. д) p 2=568 кПа.
221. Скільки молекул повітря N міститься в аудиторії, об¢ємом V= 6´4´3 м3, при температурі T= 300 К і тиску p= 978 кПа? (Стала Больцмана k= 1,38×10-23 Дж/К).
а) N =6,5×1026. б) N =1,7×1028. в) N =4,2×1025. г) N =8,4×1027. д) N =3,8×1024.
222. У балоні містилась маса m 1 = 4 кг газу при температурі T 1 = 270 К. Яку масу газу D m потрібно видалити із балону, щоб при його нагріванні до температури Т 2 = 300 К тиск p залишився початковим?
а) D m =0,4 кг. б) D m =1,2 кг. в) D m =2,4 кг. г) D m =1,8 кг. д) D m =0,8 кг.
223. У відкачаному об'ємі між скляними стінками термосу тиск р становить 5× ×10-3 Па. Визначити концентрацію молекул повітря n при цьому тиску і температурі t =20°С. (Стала Больцмана k= 1,38×10-23 Дж/К).
а) n =6,4×1019 м-3. б) n =3,6×1021 м-3. в) n =8,1×1022 м-3. г) n =4,8×1020 м-3. д) n =1,2×1018м-3.
224. Діаметр молекули азоту d= 0,3 нм. Вважаючи, що молекули мають сферичну форму, визначте, яка частина заповненого газом об'єму V, припадає (у відсотках) на об'єм самих молекул V 0 за нормальних умов (Т 0 = 273 К, р 0 = 100 кПа).
а) V 0 /V =0,02%. б) V 0 /V =0,12%. в) V 0 /V =0,08%. г) V 0 /V =0,04%. д) V 0 /V =0,16%.
225. В посудині об'ємом V= 4,2 л знаходився газ при температурі t= 18°С. Внаслідок витікання газу, тиск в посудині знизився на D p= 800 кПа. Скільки молів газу D n вийшло із посудини? Температуру газу вважати незмінною.
а)D n =2,8 моль. б)D n =1,4 моль. в)D n =0,7 моль. г)D n =2,1 моль. д)D n =3,5 моль.
226. Із балону зі стисненим газом, частина його витекла. При цьому тиск у бало-ні знизився від р 1 = 100 Н/см2 до р 2 = 80 Н/см2. Яка частина газу у відсотках до по-чаткової його маси D m/m 1 витекла із балону?
а)D m/m 1=10%. б)D m/m 1=5%. в)D m/m 1=20%. г)D m/m 1=15%. д)D m/m 1=25%.
227. Яка частина газу відносно початкової його маси D m/m 1 витекла із балону, якщо тиск у ньому зменшився від початкового р 1 = 10 МПа до р 2 = 8 МПа?
а) D m/m 1=0,2. б) D m/m 1=0,4. в) D m/m 1=0,1. г) D m/m 1=0,5. д) D m/m 1=0,3.
228. Із балону зі стиснутим воднем об¢ємом V =10 л витікає газ. При температурі t 1=70С манометр показував тиск p= 5 МПа. Через деякий час при температурі t 2= =170С манометр показував такий самий тиск. Визначте, яка кількість газу за масою D m витекла із балону? (Молярна маса водню М= 2×10-3 кг/моль).
а) D m= 3,0 г. б) D m= 2,5 г. в) D m= 1,0 г. г) D m= 1,5 г. д) D m= 2,0 г.
229. У балоні знаходилась маса m 1 = 2,5 кг газу при температурі T 1 = 283 К. Яку кі-лькість газу за масою D m потрібно видалити із балону, щоб при нагріванні його до температури T 2 = 323 К тиск газу залишився таким самим?
а) D m= 360 г. б) D m= 270 г. в) D m= 180 г. г) D m= 220 г. д) D m= 310 г.
230. Дві посудини об¢ємами V 1 = 7 та V 2 = 12 м3, з'єднані тонкою трубкою і містять газ при температурі t 1 = 00С. До якої температури t 2 треба нагріти другу посудину, щоб в ній залишилась третина від загальної кількості газу m? Температуру першої посудини t 1 вважати сталою.
а) t 2=9360С. б) t 2=7840С. в) t 2=6630С. г) t 2=8290С. д) t 2=5480С.
231. Суміш газів складається із азоту об¢ємом V 1 = 30 м3 молярної маси М 1 = 28×10-3 кг/моль і деякого об¢єму V 2 вуглекислого газу (М 2 = 44×10-3 кг/моль). Молярна маса суміші Мс =32×10-3 кг/моль. Визначте об¢єм вуглекислого газу у суміші V 2.
а) V 2 = 15 м3. б) V 2 = 10 м3. в) V 2 = 25 м3. г) V 2 = 20 м3. д) V 2 = 5 м3.
232. Циліндр довжиною L= 85 см розділений на дві частини рухомим поршнем. Ліва частина заповнена киснем (молярна маса М 1 = 32×10-3 кг/моль), а права – воднем (М 2 = 2×10-3 кг/моль). Як розташований поршень відносно лівого краю циліндру D l, якщо тиск р у обох частинах циліндру однаковий? Температури Т та маси газів m у обох частинах циліндру також однакові.
а) D l= 5 см. б) D l= 20 см. в) D l= 25 см. г) D l= 10 см. д) D l= 15 см.
|
|
Дата добавления: 2014-11-07; Просмотров: 4986; Нарушение авторских прав?; Мы поможем в написании вашей работы!