
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Внутрішня енергія
|
|
|
|
Основи термодинаміки
244. Замкнутою називають термодинамічну систему, яка:
а) Не обмінюється із зовнішнім середовищем тільки речовиною.
б) Обмінюється із зовнішнім середовищем енергією.
в) Не обмінюється із зовнішнім середовищем речовиною.
г) Обмінюється із зовнішнім середовищем тільки енергією.
д) Не обмінюється із зовнішнім середовищем ні енергією, ні речовиною.
245. Ступенями свободи молекули і називають:
а) незалежні координати, які визначають положення молекули у просторі.
б) кількість атомів, які входять до складу молекули.
в) середню відстань, яку проходить молекула за одну секунду.
г) середню відстань між двома послідовними зіткненнями.
д) кількість зіткнень молекули за секунду.
246. Скільки ступенів свободи і мають молекули одноатомного газу?
а) і= 1. б) і= 2. в) і= 3. г) і= 4. д) і= 5.
247. Скільки ступенів свободи і мають молекули двохатомного газу?
а) і= 1. б) і= 2. в) і= 3. г) і= 4. д) і= 5.
248. Скільки ступенів свободи і мають молекули трьохатомного газу?
а) і= 2. б) і= 6. в) і= 3. г) і= 4. д) і= 5.
249. Скільки ступенів свободи і мають молекули багатоатомного газу із жорсткими зв’язками?
а) і= 4. б) і= 2. в) і= 3. г) і= 6. д) і= 5.
250. Скільки ступенів свободи і мають молекули двохатомного азоту (N 2)?
а) Одну. б) Дві. в) Три. г) Чотири. д) П¢ять.
251. Яка кінетична енергія eсер в середньому припадає на кожну поступальну або обертальну ступені свободи?
а) eсер =  б) eсер =
б) eсер = 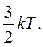 в) eсер =
в) eсер =  г) eсер = kT. д) eсер =
г) eсер = kT. д) eсер = 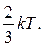
252. Яка кінетична енергія eсер в середньому припадає на кожну коливальну ступінь свободи?
а) eсер = 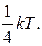 б) eсер =
б) eсер = 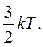 в) eсер =
в) eсер = 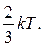 г) eсер = kT. д) eсер =
г) eсер = kT. д) eсер = 
253. Чому дорівнює відношення середньої кінетичної енергії поступального руху Еп молекул двохатомного кисню (О 2) до середньої кінетичної енергії їхнього обертального руху Еоб?
|
|
|
а) 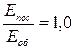 . б)
. б)  . в)
. в) 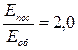 . г)
. г) 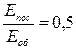 . д)
. д) 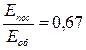 .
.
254. Чому дорівнює відношення середньої кінетичної енергії поступального руху Еп молекул метану (СН 4) до середньої кінетичної енергії їхнього обертального руху Еоб?
а) 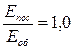 . б)
. б)  . в)
. в)  . г)
. г) 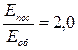 . д)
. д) 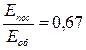 .
.
255. Укажіть, яка частина повної енергії Е молекул аміаку NН 3 припадає на енергію поступального руху Еп при помірних температурах?
а) Еп/Е= 0,66. б) Еп/Е= 0,33. в) Еп/Е= 0,75. г) Еп/Е= 0,50. д) Еп/Е= 0,25.
256. Чому дорівнює відношення середньої кінетичної енергії поступального руху Еп молекул двохатомного азоту N 2 до середньої кінетичної енергії їхнього обертального руху Еоб?
а) Еп / Еоб =0,5. б) Еп / Еоб =0,67. в) Еп / Еоб =1,0. г) Еп / Еоб =2,0. д) Еп / Еоб =1,5.
257. Чому дорівнює відношення середньої кінетичної енергії поступального руху Еп молекул двохатомного водню (Н2) до середньої кінетичної енергії їхнього обертального руху Еоб?
а) Еп / Еоб =1,0. б) Еп / Еоб =2,0. в) Еп / Еоб =1,5. г) Еп / Еоб =0,5. д) Еп / Еоб =0,67.
258. Як залежить внутрішня енергія ідеального газу U від його температури Т?
а) U~T 2. б) U~T. в) U~ 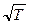 . г) U ~
. г) U ~ 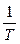 . д) U= const.
. д) U= const.
259. Як залежить внутрішня енергія ідеального газу U від концентрації його молекул n?
а) U~n 2. б) U~n. в) U~  . г) U ~
. г) U ~ 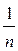 . д) U= const.
. д) U= const.
260. При якому із процесів внутрішня енергія системи U не змінюється?
а) При ізобарному. б) При ізохорному. в) При ізотермічному.
г) При адіабатному. д) При довільному.
261. Чому дорівнює зміна внутрішньої енергії D U двохатомного азоту (N 2) при ізобарному процесі?
а) 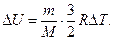 б)
б) 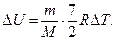 в)
в)  г)
г) 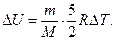 д)
д) 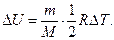
262. Чому дорівнює зміна внутрішньої енергії D U двохатомного водню (Н 2) при ізотермічному процесі?
а)D U =0. б) 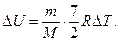 в)
в) 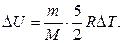 г)
г) 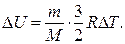 д)
д) 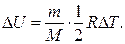
263. Чому дорівнює зміна внутрішньої енергії D U двохатомного кисню (О 2) при ізохорному процесі?
а) 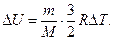 б)
б) 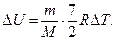 в)
в) 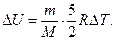 г)
г)  д)
д) 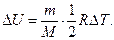
|
|
|
264. Тиск ідеального газу р= 2×10-3 Па, а концентрація його молекул n= 2×1016 м-3. Визначте середню кінетичну енергію eсер поступального руху молекул газу.
а) eсер =7,8×10-16 Дж. б) eсер =1,5×10-19 Дж. в) eсер =6,3×10-18 Дж.
г) eсер =2,7×10-17 Дж. д) eсер =4,2×10-20 Дж.
265. Тиск ідеального газу р =8×10-4 Па, а концентрація його молекул n =6×1018 м-3. Визначити середню кінетичну енергію eсер поступального руху молекул газу.
а) eсер =9×10-20 Дж. б) eсер =3×10-18 Дж. в) eсер =5×10-21 Дж.
г) eсер =7×10-19 Дж. д) eсер =2×10-22 Дж.
266. Балон містить двохатомний водень масою m =0,01 кг при температурі Т =280 К. Визначте кінетичну енергію eп поступального руху його молекул. (Молярна маса водню М =2×10-3 кг/моль, стала Авогадро NA =6,02·1023 моль-1).
а) eп =36 кДж. б) eп =81 кДж. в) eп =64×кДж. г) eп =49 кДж. д) eп =28 кДж.
267. Балон містить двохатомний кисень масою m= 0,6 кг при температурі Т= 300 К. Визначити повну кінетичну енергію Ек всіх його молекул. (Молярна маса кисню М =32×10-3 кг/моль, стала Авогадро NA =6,02·1023 моль-1).
а) Ек =120 кДж. б) Ек =180×кДж. в) Ек =90 Дж. г) Ек =210 кДж. д) Ек =150 кДж.
268. Знайти внутрішню енергію U одноатомного ідеального газу масою m= 80 г, молярна маса якого М =4×10-3 кг/моль, при температурі t= 27°С. (Молярна газова стала R =8,31 Дж/моль·К).
а) U =150 кДж. б) U =75 кДж. в) U =50 кДж. г) U =25 кДж. д) U =100 кДж.
269. Яка внутрішня енергія U кількості n= 1 моль одноатомного ідеального газу при температурі t= 27°С? (Молярна газова стала R =8,31 Дж/моль·К).
а) U =2,4 кДж. б) U =5,6 кДж. в) U =3,7 кДж. г) U =1,9 кДж. д) U =4,8 кДж.
270. Визначити внутрішню енергію U кількості n= 0,5 моль одноатомного ідеального газу при температурі t=- 73°С. (Молярна газова стала R =8,31 Дж/моль·К).
а) U =1,75 кДж б) U =1,0 кДж в) U =1,5 кДж г) U =2,0 кДж д) U =1,25 кДж
271. Визначте внутрішню енергію U кількості n= 5 моль одноатомного ідеального газу при температурі t= 1000С. (Молярна газова стала R =8,31 Дж/моль·К).
а) U =23 кДж. б) U =68 кДж. в) U =46 кДж. г) U =54 кДж. д) U =32 кДж.
272. Знайти зміну внутрішньої енергії D U кількості n= 1 моль одноатомного ідеального газу, якщо він ізобарично розширився при тиску р= 500 кПа від об¢єму V 1 = 10 л до об¢єму V 2 = 20 л. (Молярна газова стала R =8,31 Дж/моль·К).
а)D U =10 кДж. б)D U =7,5 кДж. в)D U =5 кДж. г)D U =2,5 кДж. д)D U =15 кДж.
|
|
|
273. Знайти внутрішню енергію U двохатомного ідеального газу, масою m= 20 г, молярна маса якого М= 4×10-3 кг/моль, при температурі Т= 273 К. (Молярна газова стала R =8,31 Дж/моль·К).
а) U =54 кДж. б) U =28 кДж. в) U =42 кДж. г) U =35 кДж. д) U =21 кДж.
274. Визначте внутрішню енергію U кількості n= 10 моль двохатомного ідеального газу при температурі t= 540С. (Молярна газова стала R =8,31 Дж/моль·К).
а) U =51 кДж. б) U =75 кДж. в) U =46 кДж. г) U =68 кДж. д) U =34 кДж.
275. Визначити внутрішню енергію U кількості n= 2,5 моль трьохатомного ідеального газу при температурі t=- 18°С. (Молярна газова стала R =8,31 Дж/моль·К).
а) U =24 кДж. б) U =28 кДж. в) U =12 кДж. г) U =20 кДж. д) U =16 кДж.
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 703; Нарушение авторских прав?; Мы поможем в написании вашей работы!