
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Определение электрохимического эквивалента меди
|
|
|
|
ЛАБОРАТОРНАЯ РАБОТА № 9.
Цель работы: определить электрохимическийэквивалент меди.
Теория. Молекулы солей, кислот, щелочей, при растворении этих веществ, например в воде, распадаются на заряженные частицы - ионы. Процесс называется электролитической диссоциацией.
Если в раствор, содержащий ионы, опустить пластины, соединенные с зажимами источника постоянного тока, то в образовавшемся электролитическом поле положительные ионы металла или водорода будут двигаться к отрицательной пластине (катоду) и выделятся на нем в виде твердого осадка (металл) или пузырьков газа (водород). Отрицательные ионы будут выделяться на положительной пластине (аноде). Этот процесс сопровождающий протекание тока через раствор, называется электролизом.
Масса выделившихся ионов m прямо пропорциональна количеству перенесённого ионами электричества q или силе тока I и времени его прохождения t:
m=k I t
Коэффициент пропорциональности k является для каждого вещества величиной постоянной и называется электрохимическим эквивалентом вещества. Он показывает какова масса вещества, выделяющегося на электроде при прохождении через электролит единицы количества электричества.
Приборы и принадлежности: аккумулятор, электролитическая ванна с раствором медного купороса, 2 медных электрода, амперметр постоянного тока, реостат, рубильник, провода, весы, разновесы до 0,01 г, секундомер, электрическая плитка, сосуд с водой.
Порядок выполнения работы:
1. Работа с электрической цепью.
1.1. Собрать цепь, как показано на схеме (рисунок 1.1);
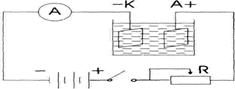
Рисунок 1.1
1.2. Замкнуть цепь и с помощью реостата R установить силу тока около 0,5А; 1.3. Разомкнуть цепь;
|
|
|
2. Вынуть катод, просушить над электрической плиткой, очистить его наждачной бумагой.
2.1. Промыть в воде катод и повторно просушить его над электрической плиткой;
3. Уравновесить весы.
3.1. Взвесить катод и определить массу(m 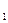 ) с точностью до 10 мг;
) с точностью до 10 мг;
3.2. Поместить катод в электролитическую ванну, замкнуть цепь и одновременно пустить в ход секундомер;
3.3. Во время опыта, который длится 15-20 минут, необходимо следить за тем, чтобы сила тока была неизменной. (0,5 А);
4. Разомкнуть цепь и засечь время в секундах (t,c).
4.1. Извлечь катод из ванны, осторожно промыть в воде, просушить над электрической плиткой;
4.2. Повторно взвесив, определить массу (m  );
);
5. Вычислить электрохимический эквивалент меди по формуле, зная I(А), t(с), m 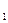 (кг), m
(кг), m  (кг):
(кг): 
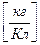
6. Повторить опыт, используя пункты 1.2.-5 лабораторной работы.
7. Найти среднее значение электрохимического эквивалента 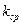 , используя данные 2-х опытов.
, используя данные 2-х опытов.
8. Зная, что табличное значение 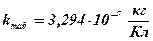 , определить относительную погрешность по формуле:
, определить относительную погрешность по формуле:
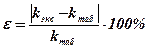 , где k
, где k  = k
= k  .
.
9. Результаты измерений и вычислений записать в таблицу 9.1.:
Таблица 9.1.
| № п\п | m 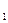 ,
(кг) ,
(кг)
| m  ,
(кг) ,
(кг)
| m  m m 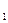 (кг)
(кг) 
| I, (А) | t, (с) | k, (кг/Кл) | k  ,
(кг/Кл) ,
(кг/Кл)
| 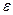 ,
% ,
%
|
10. Сделать вывод о проделанной работе.
11. Ответить на контрольные вопросы.
Контрольные вопросы:
3. Почему молекулы соли, кислоты и щёлочи в воде распадаются на ионы?
4. Почему с повышением температуры сопротивление электролита уменьшается?
5. При каких условиях концентрация электролита в процессе электролиза остаётся постоянной? меняется?
6. Как следует поступить, если по ошибке при выполнении опыта взвешенная пластинка была соединена с положительным полюсом источника тока?
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 6137; Нарушение авторских прав?; Мы поможем в написании вашей работы!