
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электродные потенциалы. Гальванические элементы
Химические источники электричества.
Пример 1. Напишите уравнения анодного и катодного процессов, суммарные ионно-молекулярное и молекулярное уравнения этих процессов, протекающих в гальваническом элементе, схема которого:
Ni │ NiSO4 ║ CoSO4 │ Co
(0,001 M) (1 M)
(В скобках приведены молярные концентрации растворов соответствующих солей). Вычислите величину электродвижущей силы (ЭДС) гальванического элемента.
Решение. Рассчитаем величины электродных потенциалов по уравнению Нернста:
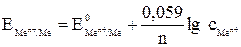 ,
,
где 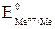 – стандартный электродный потенциал (см. в Приложении: табл. 6;
– стандартный электродный потенциал (см. в Приложении: табл. 6; 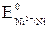 = –0,25 В;
= –0,25 В;  = –0,28 В).
= –0,28 В).
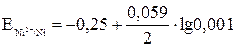 = –0,25 +
= –0,25 + 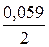 ·(–3) = –0,34 В.
·(–3) = –0,34 В.
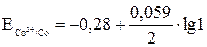 = –0,28 +
= –0,28 + 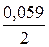 ·0 = –0,28 В.
·0 = –0,28 В.
На электроде, имеющем меньший потенциал, происходит отдача электронов, т. е. окисление. Этот электрод называется анодом. Поскольку 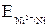 <
< 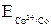 , анодом является никелевый электрод.
, анодом является никелевый электрод.
На электроде, имеющем больший потенциал, происходит принятие электронов, т. е. восстановление. Этот электрод называется катодом. Им является кобальтовый электрод.
Процессы, протекающие в гальваническом элементе:
Анод Ni – 2  = Ni2+
= Ni2+
Катод Co2+ + 2  = Co
= Co
Ионно-молекулярное уравнение: Ni + Co2+ = Ni2+ + Co
Молекулярное уравнение: Ni + CoSO4 = NiSO4 + Co
ЭДС = E(к) – E(а) = –0,28 – (–0,34) = 0,06 В.
Пример 2. В каком направлении может самопроизвольно протекать реакция
2Bi + 3CdCl2  2BiCl3 + 3Cd
2BiCl3 + 3Cd
Составьте схему гальванического элемента, в котором протекает эта реакция. Напишите уравнения анодного и катодного процессов, а также суммарное ионно-молекулярное уравнение. Определите ЭДС при концентрациях потенциалообразующих ионов в анодном и катодном пространстве, равных 1 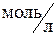 .
.
Решение. Окислительно-восстановительная реакция возможна, если потенциал предполагаемого окислителя больше потенциала предполагаемого восстановителя: Eокисл > Eвосст. Для прямой реакции
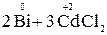

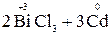
окислителем должен являться ион Cd2+, а восстановителем – металлический висмут 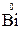 . Однако соотношение их электродных потенциалов:
. Однако соотношение их электродных потенциалов: 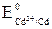 = –0,40 В <
= –0,40 В < 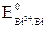 = +0,22 В, т.е. электродный потенциал предполагаемого окислителя оказывается меньше потенциала предполагаемого восстановителя: Eокисл < Eвосст. Прямая реакция невозможна.
= +0,22 В, т.е. электродный потенциал предполагаемого окислителя оказывается меньше потенциала предполагаемого восстановителя: Eокисл < Eвосст. Прямая реакция невозможна.
Для обратной реакции окислителем оказывается ион Bi3+, а восстановителем – металлический кадмий 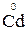 , т.е. Eокисл > Eвосст. Возможно самопроизвольное протекание обратной реакции
, т.е. Eокисл > Eвосст. Возможно самопроизвольное протекание обратной реакции
2BiCl3 + 3Cd = 2Bi + 3CdCl2
В гальваническом элементе на аноде (Cd) протекает процесс окисления кадмия, а на катоде (Bi) – процесс восстановления ионов Bi3+:
Анод Cd – 2 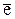 = Cd2+ │ 3
= Cd2+ │ 3
Катод Bi3+ + 3 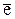 = Bi │ 2
= Bi │ 2
2Bi3+ + 3Cd = 2Bi + 3Cd2+
Схема гальванического элемента:
(А) Cd │ CdCl2 ║ BiCl3 │ Bi (К)
ЭДС = E(к) – E(а) = 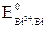 –
– 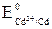 = +0,22 – (–0,40) = 0,62 В.
= +0,22 – (–0,40) = 0,62 В.
Задания
141-150. Напишите уравнения анодного и катодного процессов, Суммарные ионно-молекулярное и молекулярное уравнения этих процессов, протекающих в гальваническом элементе. Вычислите величину электродвижущей силы (ЭДС) гальванического элемента при указанных молярных концентрациях растворов соответствующих солей.
| Номер задачи | Схема гальванического элемента |
| Cu | CuSO4 || AgNO3 | Ag (1 M) (0,1 M) | |
| Bi | Bi(NO3)3 || Cu(NO3)2 | Cu (0,001 M) (1 M) | |
| Fe | FeSO4 || CdSO4 | Cd (0,001 M) (1 M) | |
| Ni | NiSO4 || CuSO4 | Cu (1 M) (0,01 M) | |
| Cd | CdSO4 || NiSO4 | Ni (0,01 M) (1 M) | |
| Zn | ZnSO4 || AgNO3 | Ag (1 M) (0,01 M) | |
| Cd | CdSO4 || CdSO4 | Cd (0,01 M) (1 M) | |
| Co | CoSO4 || CuSO4 | Cu (1 M) (0,01 M) | |
| Ni | NiSO4 || Bi(NO3)3 | Bi (0,1 M) (1 M) | |
| Pb | Pb(NO3)2 || AgNO3 | Ag (1 M) (0,01 M) |
151-160. Дайте обоснованный ответ, в каком направлении может самопроизвольно протекать заданная реакция? Составьте схему гальванического элемента, в котором протекает эта реакция. Напишите уравнения анодного и катодного процессов, а также суммарное ионно-молекулярное уравнение. Определите ЭДС при концентрациях потенциалообразующих ионов в анодном и катодном пространстве, равных 1 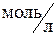 .
.
| Номер задачи | Схема реакции |
Cu + HgCl2  CuCl2 + Hg CuCl2 + Hg
| |
Cu + NiCl2  CuCl2 + Ni CuCl2 + Ni
| |
Pb + Co(NO3)2  Pb(NO3)2 + Co Pb(NO3)2 + Co
| |
| Номер задачи | Схема реакции |
Zn + NiSO4  ZnSO4 + Ni ZnSO4 + Ni
| |
Cu(NO3)2 + 2Ag  2AgNO3 + Cu 2AgNO3 + Cu
| |
CuSO4 + Co  CoSO4 + Cu CoSO4 + Cu
| |
2Bi + 3Ni(NO3)2  2Bi(NO3)3 + 3Ni 2Bi(NO3)3 + 3Ni
| |
2Ag + Co(NO3)2  2AgNO3 + Co 2AgNO3 + Co
| |
Bi + 3AgNO3  Bi(NO3)3 + 3Ag Bi(NO3)3 + 3Ag
| |
HgCl2 + Ni  Hg + NiCl2 Hg + NiCl2
|
|
|
Дата добавления: 2014-11-07; Просмотров: 4148; Нарушение авторских прав?; Мы поможем в написании вашей работы!