
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры образования ионов за счет отдачи или присоединения электронов атомами
 |
Na0 – e- = Na+
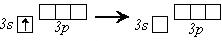 [He]3s1→[He] 3s0
[He]3s1→[He] 3s0
| F0 + e- = F-
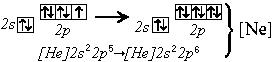
|
Ba0 – 2e- = Ba2+
 [He]6s2→[He] 6s0
[He]6s2→[He] 6s0
| O0 + 2e- = O2-
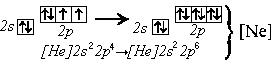
|
Al0 – 3e- = Al3+
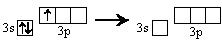 [Ne]3s2 3p1→[Ne] 3s03p0
[Ne]3s2 3p1→[Ne] 3s03p0
| I0 + e- = I-
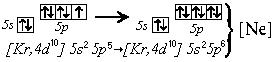
|
Mn0 – 2e- = Mn2+
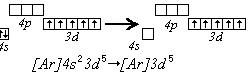
| N0 + 3e- = N3-
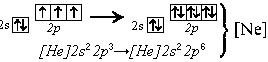
|
КОНТРОЛЬНЫЕ ЗАДАНИЯ
31. Определите количество протонов и нейтронов в ядре атома платины.
32. При бомбардировке нейтронами изотопов 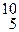 B и
B и 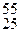 Mn выделяется a-частица и образуются изотопы
Mn выделяется a-частица и образуются изотопы 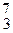 Li и
Li и 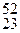 V. Составьте в полной и сокращенной формах уравнения протекающих ядерных реакций.
V. Составьте в полной и сокращенной формах уравнения протекающих ядерных реакций.
33. Электрон в атоме характеризуется набором квантовых чисел: n = 3, l = 1, m l = 0. Какая форма записи отражает энергетическое состояние электрона?
34. Какой энергетический подуровень заполняется электронами раньше: 5s или 4d; 6s или 5p и почему?
35. Составьте электронные формулы атомов элементов № 20 и № 53. На каких энергетических уровнях и подуровнях находятся валентные электроны?
36. Определите, каким элементам соответствуют приведенные электронные структуры:
а) …. 4s2 3d6,
б) …. 6s2 5d1 4f7,
в) …. 5s2 4d10 5p2?
37. Заряды ядер элементов в периодической системе непрерывно увеличиваются, а свойства простых веществ повторяются периодически. Как это объяснить?
38. Почему водород в периодической системе обычно помещают либо в первой группе и в то же время в скобках в седьмой, либо в седьмой группе и в то же время в скобках в первой. Приведите примеры реакций, доказывающих двойственную химическую природу водорода.
39. Чем обусловлена высокая химическая активность щелочных металлов? Составьте электронные схемы строения атомов натрия и цезия. У какого из этих элементов ярче выражены металлические свойства и почему?
40. Составить электронные формулы атомов элементов с порядковыми номерами 16 и 22. Показать распределение электронов этих атомов по атомным электронным орбиталям.
|
|
|
41. Составить электронную и электронно-графическую формулы атома кремния в нормальном и возбужденном состояниях.
42. Какой подуровень заполняется в атоме электронами после заполнения подуровня 4р? Ответ объяснить.
43. Какую высшую и низшую степени окисления проявляют мышьяк, селен и бром? Составить формулы соединений данных элементов, отвечающих этим степеням окисления.
44. У какого из элементов четвертого периода – марганца или брома сильнее выражены металлические свойства?
45. При бомбардировке нейтронами изотопов 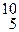 B и
B и 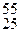 Mn выделяется a-частица и образуются изотопы
Mn выделяется a-частица и образуются изотопы 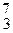 Li и
Li и 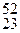 V. Составьте в полной и сокращенной формах уравнения протекающих ядерных реакций.
V. Составьте в полной и сокращенной формах уравнения протекающих ядерных реакций.
46. Электрон в атоме характеризуется набором квантовых чисел: n = 3, l = 1, m l = 0. Какая форма записи отражает энергетическое состояние электрона?
47. Какой энергетический подуровень заполняется электронами раньше: 5s или 4d; 6s или 5p и почему?
48. Составьте электронные формулы атомов элементов № 20 и № 53. На каких энергетических уровнях и подуровнях находятся валентные электроны?
49. Составить электронную формулу элемента с порядковым номером 82. По форме записи определить, в каком периоде и группе находится данный элемент, и какому семейству он принадлежит. Составить графическую схему заполнения электронами валентных орбиталей атома этого элемента в нормальном и возбужденном состояниях.
50. Напишите электронные формулы атомов углерода и серы и формулы соединений их с кислородом и водородом.
51. Изобразите электронные и электронно-графические формулы атомов 5В и 21Sc. Укажите валентные электроны. К какому семейству относятся атомы данных элементов?
52. Рассчитайте среднюю массу атома хлора.
53. Из какого числа атомов состоят 1г и 1 см3 магния?
54. Указать возможные степени окисления элемента 9F? Докажите на основании электронной конфигурации данного атома.
|
|
|
55. Указать возможные степени окисления элемента 32Ge? Докажите на основании электронной конфигурации данного атома.
56. Какой инертный газ и ионы каких элементов имеют одинаковую электронную конфигурацию с частицей, возникающей в результате удаления из атома кальция всех валентных электронов?
57. Могут ли электроны иона Аl3+ находиться на следующих орбиталях: а) 2р; б) 1р; в) 3d?
58. Напишите электронную конфигурацию атома неона в первом возбужденном состоянии.
59. Каков состав ядер изотопов 12C и 13C, 14N и 15N?
60. У какого из перечисленных ниже соединений наименее выражены кислотные свойства?
А) HNO3, б) H3PO4, в) H3AsO4, г) H3SbO4.
РАЗДЕЛ 3. ХИМИЧЕСКАЯ СВЯЗЬ
Знание природы взаимодействия атомов в веществе является основополагающим для выявления многообразия химических соединений, определения состава материалов, их строения и реакционной способности.
Причиной возникновения химической связи является такое состояние атома, при котором он всегда стремится восполнить свою оболочку до двух- или восьмиэлектронного облака. При взаимодействии атомов образуется устойчивая молекула, причем потенциальная энергия молекулы, всегда меньше энергии исходных атомов. Химическая связь образуется только тогда, когда потенциальная энергия при сближении атомов понижается.
В химической связи участвуют валентные электроны, расположенные на внешнем или предвнешнем энергетических уровнях, а, следовательно, менее прочно связанные с ядром. В табл. 3.1 и на рис.3.1. представлены примеры электронных формул атомов.
Таблица 3.1.
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 890; Нарушение авторских прав?; Мы поможем в написании вашей работы!