
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Восстановление железом
|
|
|
|
Восстановление железом проводят в среде электролитов и в водных растворах кислот. В некоторых случаях используют соли железа.
Железо в присутствии электролитов восстанавливает ароматические нитросоединения до соответствующих аминов (один из распространенных промышленных методов). При этом одновременно протекает четыре реакции:




Скорость процесса восстановления лимитируется первой стадией, которая аналогична процессу влажной коррозии железа. Поэтому восстановление ведут в среде электролита, как правило, в слабокислой среде. При повышении величины рН среды скорость реакции уменьшается. При рН > 12 процесс практически прекращается.
Электролиты вводят в реакционную массу в готовом виде (хлорид аммония) или получают в самом реакторе при протравливании чугунной стружки соляной кислотой. Наиболее активным электролитом является хлорид аммония, менее активным хлорид железа (II), сульфат аммония и т.д.
Для восстановления лучше всего использовать стружку серого чугуна, которая является отходом металлообрабатывающих производств. Активность серого чугуна объясняется возникновением в присутствии электролитов гальванической пары на границе раздела: железо–графит. Вследствие зернистого строения серый чугун в процессе восстановления распадается на мелкие частицы, что ведет к ускорению реакции.
Чугунная стружка должна быть специально подготовлена для реакции. После измельчения и просева, а также удаления пыли, чугунную стружку обезжиривают и протравливают небольшим количеством соляной кислоты, что увеличивает ее активность вследствие образования хлоридов.
Процесс восстановления чугунной стружкой ведут при температуре кипения реакционной массы. Обогрев чаще всего производят острым паром.
|
|
|
Обычно к нагретой до температуры кипения суспензии чугунной стружки в растворе электролита постепенно загружают нитропродукт. Каждую следующую порцию вводят лишь после того, как прореагирует предыдущая. В некоторых случаях порядок загрузки может быть изменен.
Если получающийся амин летуч с водяным паром, то часть его отгоняется во время процесса с водяным паром. Смесь паров воды и амина конденсируется в холодильнике, после чего поступает в отстойник для разделения. Остальную часть амина отгоняют с водяным паром после окончания процесса восстановления и подщелачивания реакционной массы. Иногда предварительно выделившийся амин сифонируют после отстаивания реакционной массы в редукторе. Амины, плохо перегоняющиеся с водяным паром, экстрагируют из реакционной массы органическими растворителями.
В производстве восстановление проводят в стальных или чугунных аппаратах (редукторах), футерованных диабазовой плиткой на кислотоупорной замазке и снабженных мешалкой (лопастной или сошниковой) и барботером для подачи острого пара.
Этот метод используют при производстве анестезина, новокаина и ряда других препаратов:

Метод отличается простотой, технологичностью, дешевизной сырья и высоким выходом целевого продукта реакции. В то же время, с развитием технологии металлообрабатывающей промышленности, отходами которой является чугунная стружка, сокращается сырьевая база этого метода, к тому же чугунная стружка с разных предприятий отличается по качеству. Однако основной проблемой метода являются трудности утилизации образующегося шлама. Фильтрация, транспортировка плохо фильтрующегося тяжелого и содержащего абразивные частицы осадка представляет серьезные трудности. Наконец, в некоторых случаях при экстрагировании продукта раствор плохо отстаивается от суспензии шлама, что вызывает большие потери растворителя.
|
|
|
Железныеопилки в среде соляной или уксусной кислот восстанавливают нитросоединения, азосоединения и альдегиды.

Процесс ведут при температуре кипения, медленно добавляя нитросоединение к суспензии железа в слабокислой водной или водно-спиртовой среде. Концентрация спирта может иметь большое значение. Наилучшие результаты получают при работе с железом, восстановленным водородом. Добавление небольшого количества хлорида никеля ускоряет реакцию.
Метод имеет промышленное значение. Положительными сторонами этого процесса являются дешевизна металла, небольшой расход кислоты, возможность использования образующихся оксидов железа в качестве красящих пигментов.
В синтезе парамиона восстановление осуществляют последовательным добавлением к раствору нитросоединения в уксусной кислоте чугунных стружек и соляной кислоты при 105—110 °С:

Сульфат железа (II) в присутствии аммиака восстанавливает нитрогруппу в молекулах соединений, содержащих и другие способные к восстановлению группы. Этот метод дает хорошие результаты при восстановлении ароматических нитрокарбоновых кислот и нитроальдегидов.

Восстановление алкоголятами алюминия
(метод Меервейна-Понндорфа-Верлея)
Алкоголяты алюминия восстанавливают ароматические и алифатические карбонильные соединения в соответствующие спирты, не затрагивая другие функциональные группы (С=С связи, в том числе и сопряженные с карбонильной группой, нитрогруппы и атомы галогенов).
В отличие от алкоголятов натрия связь между Аl и OR имеет выраженный ковалентный характер, поэтому алкоголяты алюминия являются слабыми основаниями и в незначительной степени катализируют альдольную конденсацию. Вследствие этого, а также из-за относительно большой способности к хелатообразованию алкоголяты алюминия особенно пригодны для восстановления по Меервейну-Понндорфу-Верлею.
Являясь кислотой Льюиса, алюминий в молекуле алкоголята образует комплекс с карбонильной группой и повышает ее электрофильную активность. Одновременно комплексно связанный атом алюминия вызывает сдвиг электронов в исходящих от него связях. Вследствие этого α-водородный атом алкоголята с электронной парой переносится к электронодефицитному карбонильному атому углерода:
|
|
|
Схема реакции:
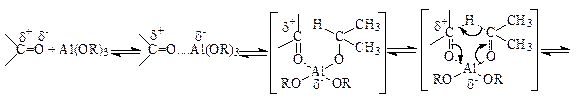
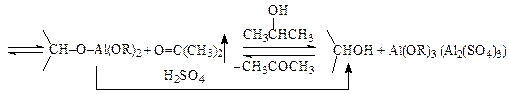
Восстановление идет за счет спиртового радикала алкоголята, который окисляется до карбонильного соединения. Образовавшийся новый алкоголят алюминия может подвергаться алкоголизу под действием растворителя, благодаря чему регенерируется изопропилат алюминия. Поэтому алкоголяты выполняют в основном роль катализатора. Однако лучшие результаты получаются при применении алкоголята в количествах 1 и более моль на моль субстрата.
Для восстановления обычно используют изопропилат алюминия в изопропиловом спирте; реже — этилат алюминия в этиловом спирте (для восстановления альдегидов). Восстановительные свойства у алкоголятов вторичных спиртов выражены значительно сильнее, чем у первичных. Кроме того, они менее склонны к побочным реакциям.
Альдегиды восстанавливаются значительно легче, чем кетоны из-за меньшего влияния пространственного фактора и большей электрофильности карбонильного атома углерода. Такие альдегиды как, например, фурфурол, восстанавливаются при комнатной температуре.
Процесс восстановления алкоголятами алюминия обратимый, поэтому обычно его проводят при нагревании с отгонкой образующегося карбонильного соединения, что способствует образованию целевого продукта. В связи с этим чаще всего в качестве восстановителя используют изопропиловый спирт, так как ацетон является самым летучим компонентом системы.
Полученный спирт выделяют, обрабатывая образовавшийся алкоголят алюминия разбавленной серной кислотой. Выходы продуктов обычно составляют 80—95 %.
Продолжительность реакции сильно зависит от природы субстрата. При слишком большой длительности процесса можно поднять температуру реакции, используя растворитель с более высокой температурой кипения (однако скорость побочных реакций увеличивается в большей степени, чем основной), добавить к реакционной смеси никель Ренея или хлорид алюминии, при этом через реакционную массу пропускают азот или водород.
|
|
|
Восстановление по Меервейну-Понндорфу-Верлею используется при синтезе левомицетина, мезатона, фетанола и ряда других препаратов:


|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 1292; Нарушение авторских прав?; Мы поможем в написании вашей работы!