
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Соединения алюминия
|
|
|
|
Алюминий и его соединения
Алюминий - один из наиболее распространенных элементов земной коры (кларк составляет 6,6 мол.%). Основные минералы: Al2O3 - корунд (окрашенные модификации - рубин, сапфир), Al2O3×nH2O - боксит, Na3AlF6 - криолит. Значительное количество алюминия находится в земной коре в виде алюмосиликатов.
Алюминий - серебристо-белый металл с высокой электро- и теплопроводностью, очень легкий (плотность 2,7 г/см3). Широко применяется в электротехнике, по электропроводности уступает только золоту, серебру и меди. Пластичен, хорошо обрабатывается прессованием и ковкой. Сплавы алюминия: силумины (11-14% кремния), дюралюмины (3,5-4% меди, 0,5-1% магния, кремния и марганца), магналий (3-30% магния) отличаются высокой прочностью и легкостью, что делает их основными конструкционными материалами в самолето- и ракетостроении.
В промышленности алюминий получают электролизом глинозема (технический оксид алюминия), растворенного в расплаве криолита Na3AlF6. В расплаве Al2O3 ведет себя как электролит.
Al2O3 = Al3+ + AlO33-
Катод: Al3+ + 3e- = Al
Анод: 4AlO33- - 12e- = 2Al2O3 + 3O2
Алюминий - очень активный металл, по активности уступает только щелочным и щелочноземельным металлам. Однако прочная оксидная пленка на поверхности алюминия придает ему повышенную устойчивость в обычных условиях. Если оксидную пленку удалить, алюминий активно реагирует с водой и кислородом воздуха:
4Al + 3O2 = 2Al2O3
2Al + 6H2O = 2Al(OH)3 + 3H2
При высоких температурах оксидная пленка не защищает алюминий и металл энергично взаимодействует с кислородом, серой, галогенами, азотом, фосфором, углеродом, образуя соответствующие бинарные соединения. Высокое сродство алюминия к кислороду позволяет использовать его для восстановления металлов из их оксидов (алюмотермия):
|
|
|
t
Fe2O3 + 2Al = 2Fe + Al2O3
Алюминий легко растворяется в водных растворах щелочей и кислот, не обладающих окислительными свойствами:
2Al + 6KOH + 6H2O = 2K3[Al(OH)6] + 3H2
2Al + 6HCl = 2AlCl3 + 3H2
Концентрированные кислоты-окислители и очень разбавленная азотная кислота пассивируют алюминий, взаимодействие возможно при нагревании:
t
8Al + 30HNO3 (разб) = 8Al(NO3)3 + 3NH4NO3 + 9H2O
В стабильных соединениях алюминий проявляет степень окисления +3, образуя оксид, гидроксид и соли.
Оксид алюминия существует в нескольких модификациях, основной из которых является a-Al2O3 (корунд) - твердое, тугоплавкое соединение (т.пл. 2050 °С). По твердости уступает только алмазу, эльбору и карборунду. Очень устойчивое соединение, не реагирующее с водными растворами кислот и щелочей. При сплавлении проявляет свойства амфотерного оксида:
t
Al2O3 + 2NaOH = 2NaAlO2 + H2O
t
Al2O3 + 3K2S2O7 = Al2(SO4)3 + 3K2SO4
Гидроксид алюминия выделяется при действии аммиака на водные растворы солей алюминия:
Al3+ + 3NH3×H2O = Al(OH)3¯ + 3NH4+
Свежеполученный Al(OH)3 реакционноспособное вещество, типичный амфотерный гидроксид, растворимый в растворах кислот и щелочей:
Al(OH)3 + 3HCl = AlCl3 + 3H2O
Al(OH)3 + 3KOH = K3[Al(OH)6]
Со временем гидроксид алюминия теряет активность за счет частичной потери воды и образования полимерных структур.
Фторид алюминия представляет собой полимерное вещество, нерастворимое в воде и органических растворителях. Хлорид, бромид и иодид алюминия - летучие кристаллические вещества, растворимые в органических растворителях, в парах и в инертных растворителях существуют в виде димерных молекул:
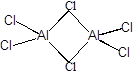
Галогениды алюминия - сильные кислоты Льюиса, энергично присоединяют электронодонорные молекулы, очень энергично растворяются в воде, иодид алюминия со взрывом.
Большинство солей алюминия хорошо растворимы в воде, сильно гидролизованы. Соли алюминия со слабыми кислотами гидролитически неустойчивы и существуют только в безводных условиях. Например:
|
|
|
Al2S3 + 6H2O = 2Al(OH)3¯ + 3H2S
Наибольшее применение находит сульфат алюминия и алюмокалиевые квасцы - K2SO4×Al2(SO4)3×24H2O.
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 674; Нарушение авторских прав?; Мы поможем в написании вашей работы!