
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
У навколишньому середовищі
|
|
|
|
ТЕРМОДИНАМІЧНІ ПРОЦЕСИ
Лабораторна робота №3.
КОНТРОЛЬНІ ПИТАННЯ
1. Що таке стерилізація? Які види стерилізації ви знаєте?
2. Класифікація живильних середовищ.
3. Які методи дослідження стану довкілля ви знаєте?
Мета роботи – навчитися розраховувати теплоємкість, експериментально визначати ентальпію хімічних реакцій і робити розрахунки, використовуючи термохімічні рівняння.
ТЕОРЕТИЧНА ЧАСТИНА
Перебіг багатьох хімічних реакцій супроводжується виділенням або поглинанням теплоти. У термохімії розрізняють два типи хімічних реакцій: екзотермічні, які супроводжуються виділенням теплоти, та ендотермічні, які супроводжуються поглинанням теплоти.
Сумарна величина енергетичних ефектів хімічної реакції називається тепловим ефектом хімічної реакції.
Під час ізохорного процесу, коли система не виконує зовнішньої роботи, пов'язаної зі зміною об'єму, вся теплота, що виділяється або поглинається, призводить до зміни внутрішньої енергії (U):

Для ізобарного процесу, при якому виконується певна робота, пов'язана зі зміною об'єму:
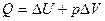 або
або 
де Q - теплота, що виділяється або поглинається; U - зміна внутрішньої енергії; р - тиск; Δ V- зміна об'єму; Δ Н- зміна ентальпії.
Додатне значення Δ Н відповідає поглинанню теплоти системою, від'ємне значення Δ Н- виділенню теплоти.
Значення Δ Н відноситься до того числа молів речовин, яке зазначено рівнянням реакції:
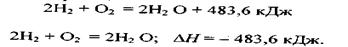
Ці рівняння показують, що при взаємодії двох молів водню з
одним молем кисню утворюються два молі води та виділяється
483,6 кДж теплоти.
Основним законом термохімії є закон Гесса: сумарний тепловий ефект ряду послідовних хімічних реакцій не залежіть від
кількості стадій процесу, а залежіть лише від початкового і
кінцевого станів системи. Отже, тепловий ефект хімічного процесу дорівнює сумі теплових ефектів окремих стадій.
|
|
|
Утворення СО2 можна проілюструвати схемою:

С+О2=СО2; ΔН=-393,5 кДж;
СО+1/2О2=СО2; ΔН1=-283,0 кДж;
С+1/2О2=СО; ΔН2=?
За законом Гесса: ΔН=ΔН1+ΔН2
Тому, ΔН2=ΔН-ΔН1=-393,5-(-283,0)=-110,5 кДж
|
|
|
|
|
Дата добавления: 2014-10-23; Просмотров: 366; Нарушение авторских прав?; Мы поможем в написании вашей работы!