
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Постулаты Бора. 1. Первый постулат заключается в следующем:
1. Первый постулат заключается в следующем:
Существуют только некоторые стационарные состояния атома, находясь в которых он не излучает энергию. Этим стационарным состояниям соответствуют вполне определенные (стационарные) орбиты, по которым движется электроны. При движении по стационарным орбитам электроны, несмотря на наличие у них ускорения, не излучают электромагнитных волн.
В стационарном состоянии атома электрон должен иметь дискретные (квантованные) значения момента импульса
Ln = mr v = n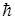 , n = 1, 2,... (2)
, n = 1, 2,... (2)
Здесь m,v– масса и скорость электрона, r – радиус его орбиты. С учетом (1) и (2) находим радиусы стационарных орбит электронов
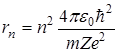 . (3)
. (3)
Для атома водорода (Z =1) радиус первой орбиты электрона при n = 1, называемый первым боровским радиусом (а), равен
r1 = a = 0,528 А. (4)
внутренняя энергия атома слагается из кинетической энергии электрона (Т = mv2 /2) и потенциальной энергии взаимодействия электрона с ядром (U =-Ze2/(4pe0r)),
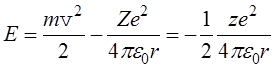 (5)
(5)
при выводе формулы (5) учли формулу (1). Подставляя в (5) квантовые радиусы орбит электронов (3), получим, что энергия атома (которая равна энергии электрона, так как ядро атома неподвижно) может принимать только следующие дозволенные дискретные (квантовые) значения
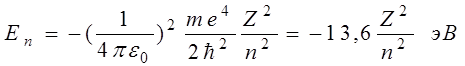 (6)
(6)
или
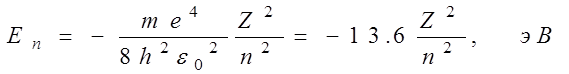
где знак минус означает, что электрон находится в связанном состоянии. (В атомной физике энергия измеряется в электронвольтах, 1 эВ = 1,6×10-19Дж).
2. Второй постулат устанавливает:
При переходе атома (электрона) из одного стационарного состояния в другое испускается или поглощается один фотон с энергией
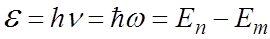 , (7)
, (7)
где Еn, Еm – энергии атома (электрона) в стационарных состояниях n и m, которые определяются согласно (6).
Исходя из своих постулатов Бор создал полуклассическую теорию простейшего водородоподобного атома и объяснил линейчатый спектр атом водорода. К водородоподобным атомам относятся атом водорода (z=1), ион гелия Не+ (z=2), ион лития Li++ (Z= 3) и др. Для них характерно, что вокруг ядра с зарядом = Ze вращается только один электрон.
|
|
Дата добавления: 2014-10-23; Просмотров: 507; Нарушение авторских прав?; Мы поможем в написании вашей работы!