
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термодинамические системы
|
|
|
|
Основные понятия химической термодинамики
Термодинамика
Термодинамика – наука о превращениях одних видов энергии и работы в другие.
Химическая термодинамика изучает превращения энергии и работы при химических процессах. Знание закономерностей химической термодинамики позволяет:
- предсказать, возможно ли в принципе химическое взаимодействие между данными веществами при определенных условиях;
- рассчитать количество энергии, которое выделится при проведении реакции или необходимо затратить для ее осуществления;
- предсказать, до какой степени будет протекать химическая реакция прежде, чем установиться химическое равновесие при данных условиях;
- выбрать оптимальные условия проведения процесса, обеспечивающие получение максимального выхода нужного продукта.
Термодинамической системой называется совокупность веществ, находящихся во взаимодействии и мысленно или физически выделенных из окружающей среды.
В зависимости от характера взаимодействия системы с окружающей средой различают открытые, закрытые и изолированные системы.
- открытые (незамкнутые) системы могут обмениваться с внешней средой энергией и массой. Например, в результате реакции взаимодействия соды с раствором хлороводородной кислоты улетучивается диоксид углерода и пары воды, то есть масса системы уменьшается, часть выделяющегося тепла идет на обогрев внешней среды: Na2CO3 + 2HCl = 2NaCl + CO2↑ + H2O
- закрытые (замкнутые) системы могутобмениваться с внешней средой только энергией. Например, рассмотренная выше система сода- кислота будет закрытой, если пробирку закрыть пробкой. В этом случае происходит только теплообмен с внешней средой через стенки пробирки;
- изолированные системы не обмениваются с окружающей средой ни массой ни энергией. На практике абсолютно изолированных систем не существует. Приближенно изолированной системой будет та же сода- кислота в закрытой пробкой пробирке, помещенная в термос.
Фазой называется часть системы, отделенная от других ее частей хотя бы одной поверхностью раздела. При переходе через поверхность раздела свойства системы меняются скачкообразно (плотность, вязкость, электропроводность, tкип., tплав.). Например, трехфазная система, приведенная на рис.1., включает три фазы и две поверхности раздела.
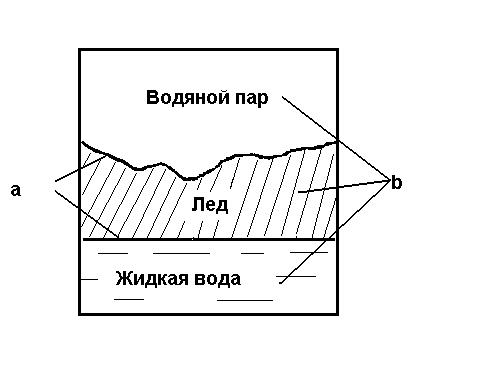 |
Рис.1.Пример трехфазной системы: a – поверхности раздела фаз;
b – фазы системы.
По агрегатному состоянию фазы разделяются на твердые (т), жидкие (ж) и газообразные (г). Твердые вещества образуют самостоятельные фазы. Жидкости могут смешиваться (серная кислота и вода или бензин и керосин), могут не смешиваться (вода и бензин). Любая смесь газов всегда однофазна.
Гомогенная система состоит из веществ, находящихся в одной фазе, в ней отсутствует поверхность раздела. Гомогенной системой является воздух-смесь азота, кислорода, водорода и других газов. К гомогенным системам относятся раствор серной кислоты, жидкая вода, лед, система 3H2(г)+ N2(г) = 2NH3 (г), состоящая только из газообразных веществ.
Гетерогенная система состоит из веществ, находящихся в разных фазах, разделенных поверхностью раздела. Гетерогенной системой является лед в воде, насыщенный раствор соли в воде, молоко, дым, туман. Система вода – лед - водяной пар – гетерогенная, трехфазная, состоит из жидкой, твердой и газообразной фаз. Система С(графит)+ СО2 (г) = 2СО (г) – гетерогенная, двухфазная, состоит из одной твердой и одной газообразной фаз.
Система MgO(к) + CO2(г) = MgCO3(к) – гетерогенная, трехфазная, состоит из двух твердых (к - кристаллы) и одной газообразной фаз.
|
|
|
|
|
Дата добавления: 2014-10-23; Просмотров: 2009; Нарушение авторских прав?; Мы поможем в написании вашей работы!