
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры составления задач и их решения
|
|
|
|
Гидролиз солей
Гидролиз солей относится к обменным реакциям, поскольку процесс идет без изменения степени окисления реагирующих веществ. Сущность реакций гидролиза состоит во взаимодействии ионов соли с ионами водыс образованием слабых электролитов. В процессе гидролиза один из ионов воды связывается в слабый электролит, а другой, как правило, накапливается в растворе. Тот ион, который накапливается в растворе, определяет реакцию среды. Если накапливаются ионы Н+, то среда будет кислой, если группы ОН – щелочной. При образовании одинаковых по силе электролитов среда может быть и нейтральной. Последний случай встречается редко.
Уравнения гидролиза пишутся аналогично другим ионным уравнениям: малодиссоциированные (в том числе и вода) и малорастворимые, а также газообразные вещества пишутся в виде молекул, сильные электролиты записываются в виде ионов. Уравнения гидролиза солей многоосновных кислот и многокислотных оснований записываются по ступеням, аналогично ступенчатой диссоциации.
Гидролиз солей, или их обменное взаимодействие с водой, происходит лишь в тех случаях, когда ионы, образующиеся в результате электролитической диссоциации соли–катион, анион или оба вместе, способны образовывать с ионами воды Н+ и ОН– – малодиссоциированные сочетания. Гидролизу подвергаются соли, образованные: слабыми кислотами и сильными основаниями; слабыми основаниями и сильными кислотами; слабыми кислотами и слабыми основаниями.
Если процесс гидролиза необходимо усилить, то следует разбавить раствор и повысить температуру.
Если необходимо уменьшить гидролиз солей, то к раствору добавляют кислоту или щелочь в зависимости от типа гидролизуемой соли.
|
|
|
Задача 893
Какие из перечисленных ниже солей подвергаются гидролизу: NH4I, Na2S, Al(CH3COO)3, CaCl2?
Решение:
Иодид аммония - соль, образованная сильной кислотой и слабым основанием. Гидролиз соли: гидролизу подвергается катион соли. Реакция раствора кислая: рН<7.
NH4I + HOH «NH4OH + HI.
Или в ионном виде:
NH4+ + HOH «NH4OH + H+.
Сульфид натрия – соль, образованная сильным основанием и слабой кислотой.
При растворении солей многоосновных кислот гидролиз протекает ступенчато:
Na2S + H2O «NaHS + NaOH.
Или в ионной форме:
S2– + H2O «HS– + OH–.
Гидролизу подвергается анион соли. Процесс отражает гидролиз по первой стадии.
Чтобы гидролиз соли многоосновной кислоты прошел полностью, как правило, увеличивают температуру процесса:
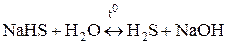 ,
,
или в ионной форме: 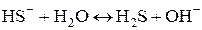 .
.
Раствор такой соли проявляет щелочную реакцию рН>7.
Ацетат алюминия – соль, образованная слабым основанием и слабой кислотой. Гидролизу подвергается как катион, так и анион соли:
Al(CH3COO)3 + H2O «AlOH(CH3COO)2 + CH3COOH.
Параллельно идут два процесса:
Al3+ + H2O «AlOH2+ + H+,
CH3COO– + H2O «CH3COOH + OH–.
В этом случае реакция раствора зависит от относительной силы кислоты и основания, образующих соль. Для гидролиза А1(СН3С00)3 реакция полученного раствора будет слабокислотной, поскольку константа диссоциации А1(OН)3 (К=1,38×10-9) меньше константы диссоциации уксусной кислоты (К=I,75×10-5).
Хлорид кальция - соль, образованная сильным основанием и сильной кислотой. Взаимодействие с водой можно представить таким образом:
CaCl2 + 2H2O «Ca(OH)2 + 2HCl,
H2O «H+ + OH–.
Однако единственным малодиссоциирующим соединением в реакции остается сама вода, следовательно, равновесие реакции полностью смещено влево - гидролиз не идет. Раствор соли проявляет нейтральную среду.
Реакция гидролиза представляет собой эндотермический процесс. Поскольку гидролиз является обычным равновесным процессом, то он зависит от всех тех факторов, которые влияют на равновесие реакций, и к нему применимо правило Ле-Шателье.
|
|
|
Задача 899
Вычислить константу гидролиза NН4Сl.
Решение:
Гидролиз соли, образованной слабым основанием и сильной кислотой, характеризуется константой гидролиза:
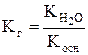 ,
,
где 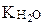 - ионное произведение воды; Косн – константа диссоциации основания.
- ионное произведение воды; Косн – константа диссоциации основания.
Из табл. 7 приложения находим 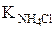 = 1,8 × 10-5.
= 1,8 × 10-5.
Отсюда 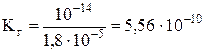 .
.
Задача 915
Вычислить степень гидролиза ZnCl2 по 1 ступени в 0,5 М растворе.
Решение:
Ионное уравнение гидролиза Zn2+ + H2O «ZnOH+ + H+,
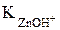 = 1,5×10-9.
= 1,5×10-9.
Степень гидролиза вычисляем по формуле:
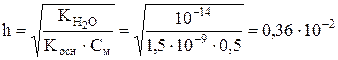 (0,36 %).
(0,36 %).
Степень гидролиза соли тем больше, чем меньше ее концентрация; иначе говоря, при разбавлении раствора гидролизующейся соли степень ее гидролиза возрастает.
При выполнении заданий рекомендуется использовать методические указания [2].
При решении задач по гидролизу использовать данные констант диссоциации некоторых электролитов, приведенные в табл. 9 приложения.
В задачах 860–893 указать, какие из перечисленных ниже солей подвергаются гидролизу. Для каждой из гидролизующихся солей написать в молекулярной и ионной форме уравнения гидролиза, указать реакцию водного раствора соли
| № Задачи | |
| 860. 861. 862. 863. 864. 865. 866. 867. 868. 869. 870. 871. 872. 873. 874. 875. 876. 877. 878. 879. 880. 881. 882. 883. 884. 885. 886. 887. 888. 889. 890. 891. 892. 893. | CrCI3, Na2S, AI2S3, KNO3 Zn(NO3)2, NaNO2, Ba(NO3)2, (NH4)2S MnSO4, CH3COONH4, KCI, NaHSO3 Na2SiO3, CuSO4, NaBr, Pb(CH3COO)2 NaH2PO4, AI2(SO4)3, NH4CN, BaCI2 Ca(HS2), Fe(CN)2, Ni(NO3)2, NaCI HCOONH4, FeCI3, KHCO3, Li2SO4 (CuOH)2SO4, (NH4)2CO3, K2SO4, Ba(NO3)2 Cr2(SO4)3, K2S, Na2SO4, Cr2S3 Na3AsO4, CoSO4, NaCIO4, Al2S3 CsNO3, K2HAsO4, NH4CIO4, Cu(CH3COO)2 Na2TeO3, ZnSO4, KJ, Fe(HCOO)3 K2HAsO4, NH4Br, RbNO3, Al(CH3COO)3 CaS, SrCl2, MgSO4, (NH4)2SO3 K2Se, BaJ2, Pb(CH3COO)2, SnSO4 NH4CN, Mg(ClO4)2, Ca(HS)2, RbCl Ca(NO2)2, Li2CrO4, Cr2S3, Zn(NO3)2 (ZnOH)2SO4, NaAsO2, Fe(CN)2, K2SO4 Zn(CN)2, Li2SO3, MnSO4, (NH4)2CO3 Bi(NO3)2, Li2SiO3, KJ, (NH4)2CO3 SbCl3, K2CrO4, Zn(CN)2, CdSO4 CH3COOK, Fe2(SO4)3, BaCl2, Al2S3 Al2S3, CsNO3, NH4ClO4, K2Te K2Te, SnSO4, Cu(CN)2, NaNO3 CuOHCl, NaH2PO4, NaBr, Cu(CH3COO)2 SrS, FeCl3, NH4CN, K2SO4 K2CO3, NaNO2, NH4HCOO, LiCl NaClO3, (NH4)2SO4, CH3COOK, KNO3 CuCl2, Ca(CH3COO)2, Pb(NO3)2, NaBr FeCl3, (NH4)2CO3, Na3PO4, K2CrO4 NaHS, Al2S3, MnCl2, Ba(NO3)2 NaHSO3, MnJ2, (NH4)2S, KSCN NaClO4, Mg(CH3COO)2, Ni3(PO4)2, RbCl NH4J, Na2S, Al(CH3COO)3, CaCl2 |
В задачах 894–903 вычислить константу гидролиза
| 894. 895. 896. 897. 898. | ацетата натрия формиата натрия ацетата калия карбоната калия ортофосфата калия | 899. 900. 901. 902. 903. | хлорида аммония гипохлорида натрия цианида натрия гидрокарбоната калия сульфита калия |
|
|
|
В задачах 904–915 вычислить степень гидролиза
| № задачи | |
| 904. 905. 906. 907. 908. 909. 910. 911. 912. 913. 914. 915. | Цианида калия в 0,1 Н растворе Ацетата калия в 0,1 М растворе 0,1 М раствора ортофосфата калия Карбоната натрия по I ступени в 0,2 М растворе Ортофосфата натрия по I ступени в 0,1 М растворе В 0,01 М растворе гидрокарбоната натрия Цианида аммония в 0,01Н растворе Хлорида аммония в 0,01 М растворе Гипохлорида калия в 0,001 М растворе В 0,06 М растворе нитрата свинца по I ступени Формиата лития в 0,001 н растворе Хлорида цинка по I ступени в 0,5 М растворе |
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 2252; Нарушение авторских прав?; Мы поможем в написании вашей работы!