
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Заряд белковой молекулы
Оптические свойства белковых растворов
Оптические свойства белков определяются размерами белковых молекул, структурой радикалов аминокислот в белках, а также наличием пептидных связей и альфа-спиральных участков в белках.
· Белковые растворы обладают эффектом светопреломления (рефракции) и светорассеивания. Данные свойства обусловлены большими размерами белковых молекул, соизмеримыми с длиной волны видимой части спектра.. При этом короткие синие лучи рассеиваются в большей степени, чем более длинноволновые красные лучи. Степень рефракции пропорциональна концентрации белкового раствора.
· Белковые растворы поглощают ультрафиолетовые лучи в диапазоне 190-230 нм за счёт присутствия пептидных связей и в диапазоне 260-280 нм за счёт присутствия в белках циклических аминокислот. Степень поглощения УФЛ пропорциональна концентрации белка в растворе.
· Белковые растворы способны вращать плоскость поляризованного света, что обусловлено оптической активностью содержащихся в белке аминокислот и наличием в нём альфа-спиральных участков. Изменение угла вращения поляризованного луча света изменяется при денатурационных воздействиях.
1.6.6. Свойства белков как истинных растворов
Белки, являясь молекулярными растворами, обладают свойствами истинных растворов. Будучи истинными растворами, белковые растворы отличаются высокой устойчивостью. Устойчивость белковым растворам придают два фактора: заряд белковой молекулы и гидратная оболочка.
Появление заряда на молекулах белков связано с их амфотерными свойствами (наличием кислотных и основных свойств). Группы, способные приобретать заряды, называются ионогенными. К ним относятся СООН - группы глютамата, аспартата, СООН - группы С-концевых аминокислот, NH2 - группы лизина, аргинина, α- NH2. - группы N-концевых аминокислот, азот имидазольного кольца гистидина. В очень незначительной степени ионизируются –SH группы цистеина и –OH группы тирозина. Ионизация различных функциональных групп белка групп определяется величиной рН среды.
Ионизация кислотных групп (СООН - группы – доноры Н+).
При рН = 2-4 половина карбоксильных групп в белках находится в ионизированном состоянии (–СОО-), половина – в неионизированном виде(–СООН). При физиологических значениях рН в интервале 7,35 – 7,45 (более щелочная среда) карбоксильные группы полностью ионизированы и определяют отрицательный заряд белковой молекулы.

Ионизация щелочных групп ( NH2 -группы - акцепторы Н+)
При рН около 10 половина аминогрупп белков ионизирована, а половина не ионизирована. При физиологических величинах рН =7.4 (более кислая среда) преобладает ионизированная форма аминогрупп (NH3+), придающая белковым молекулам положительный заряд.

Кислотно-основные свойства белков и аминокислот изучают методом потенциометрического титрования. Изменение ионизации белка при разных значениях рН имеет вид графика, приведенного ниже.
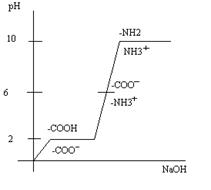
Из всех аминокислот только гистидин обладает буферными свойствами при рН = 6-7. Входя в состав белка гемоглобина, гистидин определяет его буферные свойства, необходимые для связывания кислорода.
Изменениями величины рН среды белок можно перевести в особое изоэлектрическое (электронейстральное) состояние, в котором сумма положительных зарядов равна сумме отрицательных зарядов, а молекула в целом электронейтральна
(+Н3N - белок - СОО-). Значение рН, при котором молекула белка электронейтральна, называется изоэлектрической точкой (ИЭТ). Для большинства белков изоэлектрическая точка находится в кислой среде (рН = 5-5,5). В то же время для гистонов ИЭТ находится в щелочной среде (рН= 9-11). В изоэлектрическом состоянии белки менее устойчивы, чем при наличии зарядов, поскольку одинаковый по знаку заряд белковой молекулы является фактором электростатического отталкивания белковых молекул, определяет ионные связи в белках и формирует наиболее стабильную конформацию белковой молекулы.
|
|
Дата добавления: 2014-10-31; Просмотров: 797; Нарушение авторских прав?; Мы поможем в написании вашей работы!