
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция 17. Окислительно-восстановительные иэлектрохимические процессы
|
|
|
|
- процессы взаимного превращения химической и электрической форм энергии: Е хим  Е эл
Е эл
особый вид окислительно – восстановительных реакций (ОВР Любая ОВР –
сумма сопряженных реакций окисления и восстановления
 4 е -
4 е -
2Но2 + Оо2 = 2Н+2О-2
восст- ль окисл - ль
Окисление – процесс отдачи е - частицей
Частица, отдающая е - - восстановитель (↑ ст. ок.)
Восстановление – процесс присоединения е - частицей
Частица, принимающая е - - окислитель (↓ ст. ок.)
Условие прохождения реакции:
столкновение частиц и переход е - от восстановителя к окислителю на малом расстоянии между ними
Особенности электрохимических ОВР -
- пространственное разделение процессов окисления и восстановления
- проводятся в электрохимических ячейках
Ячейка состоит из:
- двух электродов (1)
- внутренней цепи (2)
- внешней цепи (3) 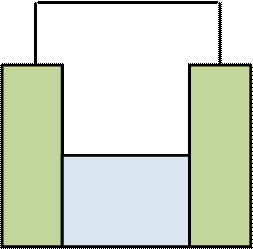

проводники II рода-
 растворы, расплавы электролитов
растворы, расплавы электролитов (ионнаяпроводимость)
(ионнаяпроводимость)
проводники I рода - металлические проводники (е - - проводимость)




В электрохимии:
процессы восстановления → катодные процессы
процессы окисления → анодные процессы
ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ
Электрод – проводник I рода, находящийся в контакте с проводником проводником II рода

 проводник I рода
проводник I рода  проводник II рода
проводник II рода
При погружении Ме в раствор собственных ионов происходит:
1) адсорбция полярных молекул растворителя (Н2О)
2) переход гидратированных катионов в раствор:
Ме + m Н2О ® Mеn+ × (Н2О)m + ne-

раствор Ме
В Ме остаются е -, нескомпенсированные (+) –ионами Þповерхность Ме
|
|
|
заряжается (-), приэлектродный слой раствора заряжается (+)
3) на границе Ме – раствор образуется двойной электрический слой (ДЭС),
который характеризуется определенной разностью потенциалов, называемой электродным потенциалом:
(Y2 - Y1) = Е Меn+/Ме – электродный потенциал

активный металл (Fe, Zn) Þ переход ионов в раствор Þ (- Е)
малоактивный металл (Cu, Ag) Þ адсорбция ионов из раствора Þ(+ Е)
4) При некотором значении Е устанавливается динамическое равновесие:
Ме + m Н2О  Меn+× (Н2О)m+ n e-
Меn+× (Н2О)m+ n e-
Упрощенно:
Ме  Меn+ + nе -
Меn+ + nе -
Потенциал, который устанавливается в условиях электродной реакции - равновесный электродный потенциал (Е равн)
Ионы металла Men+ - потенциалопределяющие ионы
Е равн зависит:
от природы Ме:
чем ¯ Е ионизации атома Ме
чем ¯ Е крист решетки Ме
чем Е гидратации ионов Ме, тем ↑ способность Ме посылать ионы Меn+ в раствори более отрицательным будет его 
от активности потенциалопределяющих ионов
от Т
У благородных Ме: Pt, (Pd, Au):
Е крист. реш. и Е иониз. Þ
нет разности потенциалов, обусловленной переходом ионов
Þ Pt, (Pd, Au) не принимают участия в электродных реакциях.
ü
Их используют в качестве подложки для адсорбции газов в газовых электродах.
ЗАКОНЫ ФАРАДЕЯ
1–й закон. Массы превращенных веществ на электродах при протекании постоянного тока пропорциональны количеству электричества Q, прошедшего через систему.
2-й закон. При прохождении через различные системы одного и того же количества электричества Q массы превращенных веществ m пропорциональны молярным массам их эквивалентов.
m (1) / M Э(1) = m (2) / M Э(2)
Объединенный закон:
При прохождении через любую электрохимическую систему 1F электричества на каждом из электродов превращается 1 моль-эквивалент вещества
F = 96484 Кл или F= 26,8 А×ч - число Фарадея
для массы вещества:

для объема газообразного 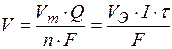
вещества
|
|
|
 n – число е-, участвующее в процессе
n – число е-, участвующее в процессе
МЭ – молярная масса эквивалента вещества, г/моль
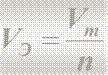
VЭ – объем моль эквивалента газа, л/моль
Q = I×τ - количество электричества [А×с]или [Кл];
I - сила постоянного тока [А];
τ – время процесса, [с]
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 352; Нарушение авторских прав?; Мы поможем в написании вашей работы!