
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кристаллизация сплавов
|
|
|
|
Фазовый состав твердого сплава, или система фаз, формируется в процессе охлаждения и кристаллизации из жидкой фазы, при этом фазовые превращения сопровождаются выделением тепловой энергии и уменьшением энергии Гиббса. Если система фаз приобретает минимальную энергию Гиббса, то изменения термодинамических параметров системы не вызывают фазовых изменений и она остается в равновесии. Такое фазовое равновесие сохраняется при определенном соответствии между числом фаз системы и числом внешних и внутренних параметров (температура, давление, концентрация компонентов), возможное изменение которых не меняет числа фаз, находящихся в равновесии. Число указанных параметров называется числом степеней свободы системы, а названное условие соответствия представляет правило фаз (Гиббса) и выражается уравнением:
С = К + П – Ф,
где С – число степеней свободы,
К – число компонентов системы,
П – число изменяемых внешних параметров,
Ф – число фаз, находящихся в равновесии.
Учитывая возможность присутствия в металлических сплавах жидкой и твердой фаз, принимается во внимание зависимость состояния сплавов от одного внешнего параметра – температуры (П =1), поскольку другой параметр – давление почти не влияет на равновесие жидкой и твердой фаз.
Чистый металл в процессе охлаждения и кристаллизации рассматривается как однокомпонентный сплав (К = 1), поэтому уравнение равновесия фаз принимает вид:
С = 1 + 1 – Ф.
Из полученного выражения следует, что при жидкофазном состоянии металла число степеней свободы составляет С = 1, т.е. система является моновариантной, и ее равновесие сохраняется при изменении температуры расплава соответственно кривой охлаждения (рис.13). С началом процесса кристаллизации появляется вторая фаза – кристаллы, и число степеней свободы соответствует равенству С = 0, при котором система называется нонвариантной. Здесь фазовое равновесие поддерживается при отсутствии степеней свободы, т.е. в условиях постоянной температуры до конца процесса кристаллизации металла.
|
|
|
У двухкомпонентного металлического сплава (К =2) правило равновесия фаз становится выражением:
С = 2 + 1 – Ф.
Оно показывает, что в процессе охлаждения жидкофазного расплава система является бивариантной (С =2) так, что ее равновесие сохраняется при произвольных изменениях температуры и концентрации (рис. 15, линия 1). При появлении второй, кристаллической фазы система становится моновариантной (С =1), допуская изменение температуры согласно кривой охлаждения (рис. 15, линия 2). Скорость охлаждения в это время замедляется из-за выделения скрытой теплоты кристаллизации, что проявляется как перегиб кривой при определенной температуре, называемой критической точкой. Если же в ходе фазовых превращений образуется третья фаза, то системе становится нонвариантной (С =0), и ее равновесие обеспечивается при постоянной температуре (рис. 15, линия 3).
После завершения фазовых превращений и кристаллизации сплава с образованием двух кристаллических фаз система становится моновариантной (С = 1), и ее охлаждение заканчивается при сохранении фазового равновесия (рис.15, линия 4).
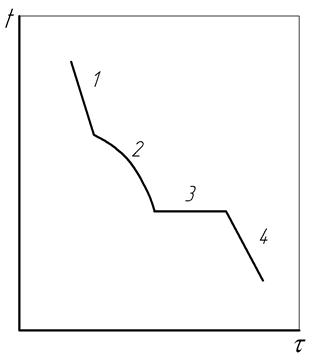
Рис. 15. Кривая охлаждения сплава: 1 – охлаждение жидкого сплава;
2 – кристаллизация с выделением одной твердой фазы; 3 – кристаллизация с выделением второй твердой фазы; 4 – охлаждение твердого кристаллического сплава
Кривая охлаждения сплава характеризует его фазовые и структурные превращения при определенных значениях концентрации компонентов и скорости охлаждения. Для других концентраций и скоростей превращения в сплаве протекают с иными закономерностями: возникают новые фазы, изменяются критические температуры и кинетика превращений, что отображается соответствующими кривыми.
|
|
|
Чтобы в системе данных компонентов определить изменения фазового состояния, соотношения фаз и их состава в зависимости от концентрации компонентов и температуры, используются диаграммы состояния или фазового равновесия сплавов. Они строятся в координатах температура – концентрация компонентов (в массовых процентах) по экспериментально полученным кривым медленного охлаждения либо нагревания серии образцов сплавов данной системы с различным содержанием компонентов, например, А и В (рис. 16, а). При этом происходит образование равновесных фаз и устанавливаются точки критических температур, которые затем переносятся на вертикали, соответствующие химическому составу сплавов. Последующим соединением точек, характеризующих однотипные фазовые превращения, получают линии диаграммы состояния (рис. 16, б).
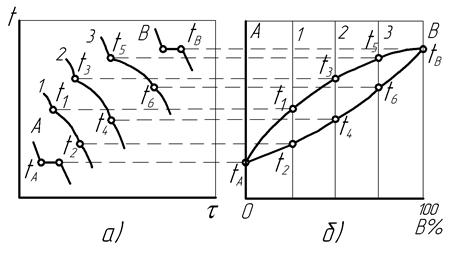
Рис. 16. Принцип построения диаграмм состояния сплавов: а – экспериментальные кривые охлаждения серии образцов; б – диаграмма состояния сплавов
Построенные экспериментально диаграммы состояния сплавов теоретически анализируются, что позволяет для сплава с определенной концентрацией компонентов и при заданной температуре выявить фазовое состояние сплава, соотношение фаз, их состав, а также характер основных свойств сплава. Это дает возможность в последующем разработать оптимальный технологический процесс обработки сплава для получения изделий с использованием методов литья, обработки давлением, процессов сварки, электрофизической обработки, напыления, термической обработки.
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 598; Нарушение авторских прав?; Мы поможем в написании вашей работы!