
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Закони газового стану
|
|
|
|
1.3.1. ЗАКОН ОБ’ЄМНИХ ВІДНОШЕНЬ ГЕЙ-ЛЮСАКА
Об’єми газів, що вступають до реакції відносяться один до іншого, а також до об’ємів одержуваних газоподібних продуктів як невеликі цілі числа. Наприклад: 1 л хлору сполучається з одним літром водню, у підсумку чого утворюється 2 л хлороводню.
1.3.2. ЗАКОН АВОГАДРО
Одним з основних газових законів є закон Авогадро: в однакових об’ємах газів за однакових умов (температура, тиск) містяться однакові кількості молекул.
Наслідки із закону Авогадро:
1. За нормальних умов (to = 0o C, p = 101,3 кПа) один моль будь-якого газу займає один і той самий об’єм, що дорівнює 22,4 л. Цей об’єм називається молярним об’ємом газу (VM). Молярний об’єм – це відношення об’єму газоподібної речовини до кількості цієї речовини: 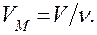
2. Відношення маси певного об’єму одного газу до маси такого ж об’єму другого газу називається відносною густиною першого газу за другим (позначається літерою D).
Враховуючи, що із закону Авогадро випливає, що m1: m2 = M1: M2, можна записати, що 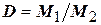 або
або 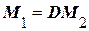 .
.
Звичайно густини визначають за найлегшим газом – воднем (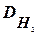 ). Молярна маса водню дорівнює 2 г/моль, звідси М = 2
). Молярна маса водню дорівнює 2 г/моль, звідси М = 2 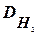 .
.
Молекулярна маса речовини у газоподібному стані дорівнює його подвоєній густині за воднем у а.о.м., а молярна маса цієї речовини стільки ж, тільки у г/моль.
Якщо відома густина за повітрям (Dпов.), то М = 29Dпов., бо середня молярна маса повітря дорівнює 29 г/моль.
1.3.3. ЗАКОН БОЙЛЯ – МАРІОТТА
Для порівняння тисків і об’ємів певної кількості того ж самого газу за різних умов (але сталій температурі) зручно користуватися закономБойля – Маріотта:
При сталій температурі тиск, який спричинює певна маса газу обернено пропорційний об’єму цієї маси газу: р2/р1 = V1/V2. або pV = const.
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 790; Нарушение авторских прав?; Мы поможем в написании вашей работы!