
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пищевые альгинаты
|
|
|
|
| Е- номер | Название | Природа катиона в мономерном остатке |
| Е400 | Альгиновая кислота | Н |
| Е401 | Альгинат натрия | Na |
| Е402 | Алъгинат калия | К |
| Е403 | Альгинат аммония | NH4 |
| Е404 | Альгинат кальция | 1/2Ca |
| Е405 | Пропиленгликольальгинат (ПГА) | -СН2-СН-СН3 | ОН |
Растворимость этих добавок в воде зависит от природы катиона в мономерных остатках, формирующих молекулы рассматриваемых гетерогликанов.
Свободные альгиновые кислоты плохо растворимы в холодной воде, но набухают в ней, связывая 200—300-кратное количество воды, однако растворимы в горячей воде и растворах щелочей, образуя при подкислении гели.
Натриевые и калиевые соли альгиновых кислот легко растворяются в воде с образованием высоковязких растворов. Соли с двухвалентными катионами образуют гели или нерастворимые альгинаты.
Вязкость растворов альгинатов связана с длиной полимерной молекулы альгината, в связи с чем коммерческие препараты имеют, как правило, определенную молекулярную массу. В этом случае вязкость растворов изменяется пропорционально концентрации добавки. При низких концентрациях повышение вязкости может быть достигнуто путем введения небольшого количества ионов кальция, которые, связывая молекулы, приводят фактически к повышению молекулярной массы и, как следствие, к повышению вязкости. Превышение дозировки ионов кальция может привести к гелеобразованию.
Образование гелевой структуры в растворах альгинатов происходит в результате взаимодействия их молекул между собой с участием ионов бивалентного кальция, причем зонами ассоциации служат участки полигулуроновой кислоты (зоны кристалличности). В связи с этим гелеобразующая способность и прочность гелей непосредственно связаны с количеством и длиной зон кристалличности. С химической точки зрения формирование геля при взаимодействии альгината с ионами кальция можно рассматривать как ионообменный процесс замены одновалентного катиона (например, натрия) в молекуле водорастворимой соли альгиновой кислоты с образованием стыковых зон через катион двухвалентного металла.
|
|
|
Применение альгинатов в пищевых продуктах основано на взаимодействии их водорастворимых солевых форм в присутствии ионов кальция, что приводит к модификации реологических свойств (повышению вязкости или образованию гелевой структуры). По своим технологическим функциям альгинаты являются загустителями, гелеобразователями и стабилизаторами. Альгинат кальция проявляет также функцию пеногасителя.
Одно из главных преимуществ альгинатов как гелеобразователей — их способность образовывать термостабильные гели, которые могут формироваться уже при комнатной температуре.
Пищевые добавки этой подгруппы широко применяют в пищевой промышленности для изготовления мармелада, фруктовых желе, конфет и осветления соков. Пропиленгликольалъгинат, не осаждающийся в кислых растворах, используется в качестве стабилизатора при производстве мороженого, концентратов апельсинового сока, приправы к салатам и сырам.
Концентрация альгинатов в пищевых продуктах составляет от 0,1 до 1,0%.
По официальным рекомендациям ФАО—ВОЗ суточное потребление человеком альгиновых кислот и их солей может достигать 25 мг/кг массы тела (в пересчете на свободную альгмновую кислоту).
Агар-агар (Е406). Смесь полисахаридов агарозы и агаропекгина. Агароза (содержание 50—80 %) — линейный полисахарид, построенный из строго чередующихся остатков β-D-галактопиранозы и 3,6-ангидро-α-L-галактопиранозы, связанных попеременно (1,4)-β и (1, 3)-α-связями:
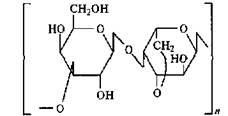
β,D-галактопираноза 3,6-α,L-галактопираноза
|
|
|
Агар-агар (агар) получают из морских красных водорослей родов Gracilaria, Gelidium, Ahnfeltia, произрастающих в Белом море и Тихом океане. В зависимости от вида водорослей состав выделенных полисахаридов может изменяться. Агар-агар незначительно растворяется в холодной воде и набухает в ней. В горячей воде образует коллоидный раствор, который при охлаждении дает хороший прочный гель, обладающий стекловидным изломом. У агара-агара этот процесс осуществляется за счет образования двойных спиралей и их ассоциации независимо от содержания катионов, сахара или кислоты. Гелеобразующая способность агара-агара в 10 раз выше, чем у желатина. При нагревании в присутствии кислоты способность к гелеобразованию снижается. Гели стабильны при рН выше 4, 5 и термообратимы. Агар используют в производстве кондитерских изделий (желейный мармелад, пастила, зефир), мясных и рыбных студней, различных желе и пудингов, а также для осветления соков. В составе мороженого агар-агар предотвращает образование кристаллов льда.
Агаропектин — смесь кислых полисахаридов сложного строения, аналогичного агарозе, с рядом отличий: заменой части остатков 3,6-ангидро-α, L-галактозы остатками 6-сульфата-α, L-галактозы, наличием остатков серной кислоты, связанных эфирными связями с различными группами ОН, и др.
Агароид (черноморский агар). Получают из водорослей филлофоры, растущих в Черном море. Плохо растворим в холодной воде, в горячей воде образует коллоидный раствор, при охлаждении которого образуется гель, имеющий вязко-тягучую консистенцию. Гелеобразующая способность этой добавки в два раза ниже, чем у агара.
Каррагинаны (Е407). Объединяют семейство полисахаридов, содержащихся наряду с агаром и фурцеллераном в красных морских водорослях. По химической природе каррагинаны близки к агарои-дам и представляют собой неразветвленные сульфатированные гетерогликаны, молекулы которых построены из остатков производных D-галактопиранозы со строгим чередованием α-(1-3) и β-(1-4)-связей между ними, т. е. из повторяющихся дисахаридных звеньев, включающих остатки β-D-галактопиранозы и 3,6-ангидро-α-D-галактопиранозы. В зависимости от особенностей строения дисахаридных повторяющихся звеньев, различают три основных типа каррагинанов, для обозначения которых используют буквы греческого алфавита: к-каппа, i-йота и Х-ламбда. Фрагменты формул этих типов каррагинанов представлены ниже.
|
|
|
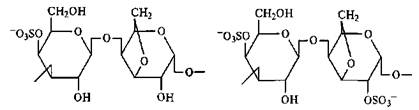
к-Каррагинан ι -Каррагинан
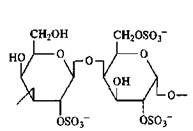
λ-Каррагинан
В к- и ι-каррагинанах левые галактозные остатки дисахаридных повторяющихся звеньев содержат сульфатированные гидроксильные группы при четвертом атоме углерода, а правый галактозный остаток находится в 3,6-ангидроидной форме и имеет сульфатированный гидроксил при втором атоме углерода в ι-каррагинане и несульфатированный — в к-типе.
В λ.-каррагинане в левом галактозном остатке дисахаридного звена сульфатирован гидроксил при втором атоме углерода, а в правом — при втором и шестом. Отличительные особенности строения каррагинанов различных типов приведены в табл. 3.14.
Таблица 3.14
|
|
|
|
|
Дата добавления: 2014-11-08; Просмотров: 2300; Нарушение авторских прав?; Мы поможем в написании вашей работы!