
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гибридизация атомных орбиталей. Типы гибридизации и геометрии молекул
|
|
|
|
Периодический закон и периодическая система химических элементов Менделеева в строении атома. Физический смысл периодического закона. Структура периодической системы. Период, группа, подгруппа
Основной закон химии - Периодический закон был открыт в 1869 году в то время, когда атом считался неделимым и о его внутреннем строении ничего не было известно. В основу Периодического закона Д.И. Менделеев положил атомные массы и химические свойства элементов.
Расположив 63 известных в то время элемента в порядке возрастания их атомных масс, Д.И. Менделеев получил естественный (природный) ряд химических элементов, в котором он обнаружил периодическую повторяемость химических свойств.
Периодический закон в формулировке Д.И. Менделеева: Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
Группы. В таблице семь горизонтальных рядов элементов, которые называются периодами, а также восемнадцать вертикальных столбцов — групп. Таким образом, каждый химический элемент имеет свой атомный (порядковый) номер, находится в определенном периоде и определенной группе.
В зависимости от того, какой энергетический подуровень заполняется электронами последним, различают четыре типа (семейства) элементов:
1. s -элементы – последним заполняется s -подуровень внешнего энергетического уровня;
2.p -элементы – p -подуровень внешнего энергетического уровня;
3. d -элементы – d -подуровень предпоследнего энергетического уровня;
4. f -элементы – f -подуровень третьего снаружи уровня.
Период — строка периодической системы химических элементов, последовательность атомов по возрастанию заряда ядра и заполнению электронами внешней электронной оболочки.
|
|
|
Периодическая система имеет семь периодов. Первый период, содержащий 2 элемента, а также второй и третий, насчитывающие по 8 элементов, называются малыми. Остальные периоды, имеющие 18 и более элементов — большими. Седьмой период не завершён. Номер периода, к которому относится химический элемент, определяется числом его электронных оболочек (энергетических уровней).
Каждый период (за исключением первого) начинается типичным металлом (Li, Nа, К, Rb, Cs, Fr) и заканчивается благородным газом (Не, Ne, Ar, Kr, Хе, Rn), которому предшествует типичный неметалл.
В первом периоде, кроме гелия, имеется только один элемент — водород, сочетающий свойства, типичные как для металлов, так и (в большей степени) для неметаллов. У этих элементов заполняется электронами 1 s -подоболочка.
У элементов второго и третьего периода происходит последовательное заполнение s - и р -подоболочек. Для элементов малых периодов характерно достаточно быстрое увеличение электроотрицательности с увеличением зарядов ядер, ослабление металлических свойств и усиление неметаллических.
Четвёртый и пятый периоды содержат декады переходных d -элементов (от скандия до цинка и от иттрия до кадмия), у которых после заполнения электронами внешней s -подоболочки заполняется, согласно правилу Клечковского, d -подоболочка предыдущего энергетического уровня.
Группа периодической системы химических элементов — последовательность атомов по возрастанию заряда ядра, обладающих однотипным электронным строением. Номер группы определяется количеством электронов на внешней оболочке атома (валентных электронов) и, как правило, соответствует высшей валентности атома.
В короткопериодном варианте периодической системы группы подразделяются на подгруппы (А), начинающиеся с элементов первого и второго периодов, и побочные (В), содержащие d -элементы. Подгруппы также имеют названия по элементу с наименьшим зарядом ядра (как правило, по элементу второго периода для главных подгрупп и элементу четвёртого периода для побочных подгрупп). Элементы одной подгруппы обладают сходными химическими свойствами.
|
|
|
С возрастанием заряда ядра у элементов одной группы из-за увеличения числа электронных оболочек увеличиваются атомные радиусы, вследствие чего происходит снижение электроотрицательности, усиление металлических и ослабление неметаллических свойств элементов, усиление восстановительных, ослабление окислительных свойств образуемых ими веществ.
7. Связь свойств элементов с их положением в периодической системе. Периодически имеющиеся свойства элементов: радиуса атома, энергиионизации, сродства к электрону и электроотрицательности
Д. И. Менделеев считал, что основной характеристикой элементов являются их атомные веса, и в 1869 г. впервые сформулировал периодический закон. Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
Весь ряд элементов, расположенных в порядке возрастания атомных масс, Менделеев разбил на периоды, внутри которых свойства элементов изменяются последовательно, разместив периоды так, чтобы выделить сходные элементы.
Итак, главной характеристикой атома является не атомная масса, а величина положительного заряда ядра. Это более общая точная характеристика атома, а значит, и элемента. От величины положительного заряда ядра атома зависят все свойства Элемента и его положение в периодической системе. Таким образом, порядковый номер химического элемента численно совпадает с зарядом ядра его атома. Периодическая система элементов является графическим изображением периодического закона и отражает строение атомов элементов.
Теория строения атома объясняет периодическое изменение свойств элементов. Возрастание положительного заряда атомных ядер от 1-до 110 приводит к периодическому повторению у атомов элементов строения внешнего энергетического уровня. А поскольку от числа электронов на внешнем уровне в основном зависят свойства элементов; то и они периодически повторяются. В этом физический смысл периодического закона.
|
|
|
В каждом периоде с возрастанием порядкового номера элементов металлические свойства постепенно ослабевают и возрастают неметаллические, заканчивается период инертным газом. В каждом периоде с возрастанием порядкового номера элементов металлические свойства постепенно ослабевают и возрастают неметаллические, заканчивается период инертным газом.
В свете учения о строении атома становится понятным разделение всех элементов на семь периодов, сделанное Д. И. Менделеевым. Номер периода соответствует числу энергетических уровней атома, то есть положение элементов в периодической системе обусловлено строением их атомов. В зависимости от того, какой подуровень заполняется электронами, все элементы делят на четыре типа.
1. s-элементы. Заполняется s-подуровень внешнего уровня (s1 — s2). Сюда относятся первые два элемента каждого периода.
2. р-элементы. Заполняется р-подуровень внешнего уровня (р1 -- p6)- Сюда относятся последние шесть элементов каждого периода, начиная со второго.
3. d-элементы. Заполняется d-подуровень последнего уровня (d1 — d10), а на последнем (внешнем) уровне остается 1 или 2 электрона. К ним относятся элементы вставных декад (10) больших периодов, начиная с 4-го, расположенные между s- и p-элементами (их также называют переходными элементами).
4. f-элементы. Заполняется f-подуровень глубинного (треть его снаружи) уровня (f1 —f14), а строение внешнего электронного уровня остается неизменным. Это лантаноиды и актиноиды, находящиеся в шестом и седьмом периодах. Таким образом, число элементов в периодах (2-8-18-32) соответствует максимально возможному числу электронов на соответствующих энергетических уровнях: на первом — два, на втором — восемь, на третьем — восемнадцать, а на четвертом — тридцать два электрона. Деление групп на подгруппы (главную и побочную) основано на различии в заполнении электронами энергетических уровней. Главную подгруппу составляют s- и p-элементы, а побочную подгруппу — d-элементы. В каждой группе объединены элементы, атомы которых имеют сходное строение внешнего энергетического уровня. При этом атомы элементов главных подгрупп содержат на внешних (последних) уровнях число электронов, равное номеру группы. Это так называемые - валентные электроны.
|
|
|
У элементов побочных подгрупп валентными являются электроны не только внешних, но и предпоследних (вторых снаружи) уровней, в чем и состоит основное различие в свойствах элементов главных и побочных подгрупп.
Отсюда следует, что номер группы, как правило, указывает число электронов, которые могут участвовать в образовании химических связей. В этом заключается физический смысл номера группы.
Свойства элементов, зависящие от строения электронной оболочки атома, изменяются по периодам и группам периодической системы. Поскольку в ряду элементов-аналогов электронные структуры лишь сходны, но не тождественны, то при переходе от одного элемента в группе к другому для них наблюдается не простое повторение свойств, а их более или менее отчетливо выраженное закономерное изменение.
Химическая природа элемента обусловлена способностью его атома терять или приобретать электроны. Эта способность количественно оценивается величинами энергий ионизации и сродства к электрону.
Энергией ионизации (Eи) называется минимальное количество энергии, необходимое для отрыва и полного удаления электрона из атома в газовой фазе при T = 0 K без передачи освобожденному электрону кинетической энергии с превращением атома в положительно заряженный ион:
Э + Eи = Э+ + e-
Энергия ионизации является положительной величиной и имеет наименьшие значения у атомов щелочных металлов и наибольшие у атомов благородных (инертных) газов.
Сродством к электрону (Ee) называется энергия, выделяемая или поглощаемая при присоединении электрона атому в газовой фазе при T = 0
K с превращением атома в отрицательно заряженный ион без передачи частице кинетической энергии: Э + e- = Э- + Ee. Максимальным сродством к электрону обладают галогены, особенно фтор (Ee = -328 кДж/моль). Способность связанного атома смещать к себе электроны химических связей, повышая около себя электронную плотность называется электроотрицательностью. Это понятие в науку введено Л.Полингом. Электроотрицательность обозначается символом ÷ и характеризует стремление данного атома к присоединению электронов при образовании им химической связи. Для количественной оценки ÷ предложено несколько различных методов.
По Р.Маликену электротрицательность атома оценивается полусуммой энергий ионизации и сродства к электрону свободных атом ÷ = (Ee + Eи)/2. В периодах наблюдается общая тенденция роста энергии ионизации и электроотрицательности с ростом заряда ядра атома, в группах эти величины с увеличением порядкового номера элемента убывают.
Атомные и ионные радиусы. Размеры атомов и ионов определяются размерами электронной оболочки. Согласно квантово-механическим представления электронная оболочка не имеет строго определенных границ. Поэтому за радиус свободного атома или иона можно принять теоретически рассчитанное расстояние от ядра до положения главного максимума плотности внешних электронных облаков. Это расстояние называется орбитальным радиусом. На практике обычно используют значения радиусов атомов и ионов, находящихся в соединениях, вычисленные исходя из экспериментальных данных. При этом различают ковалентные и металлические радиусы атомов.
Зависимость атомных и ионных радиусов от заряда ядра атома элемента и носит периодический характер. В периодах по мере увеличения атомного номера радиусы имеют тенденцию к уменьшению. Наибольшее уменьшение характерно для элементов малых периодов, поскольку у них заполняется внешний электронный уровень. В больших периодах в семействах d- и f- элементов это изменение менее резкое, так как у них заполнение электронов происходит в предвнешнем слое. В подгруппах радиусы атомов и однотипных ионов в общем увеличиваются.
8. Химическая связь. Основные характеристики химической связи: энергия, длинна связи, валентные углы
Химическая связь - взаимное притяжение атомов, приводящее к образованию молекул и кристаллов. Принято говорить, что в молекуле или в кристалле между соседними атомами существуют Х. с. Валентность атома показывает число связей, образуемых данным атомом с соседними атомами Э.Франкленд в 1852 предложил концепцию, согласно которой каждый элемент образует соединения, связываясь с определённым числом эквивалентов др. элементов, при этом один эквивалент соответствует количеству, требуемому одной валентностью.
Энергия химической связи, равна работе, которую необходимо затратить, чтобы разделить молекулу на две части (атомы, группы атомов) и удалить их друг от друга на бесконечное расстояние. Для молекулы, содержащей две (или более) одинаковых связей, различают энергию каждой связи (энергию разрыва связи) и среднюю энергию связи, равную усредненной величине энергии разрыва этих связей. Различие между величинами энергий разрыва и средней энергией химической связи обусловлено тем, что при частичной диссоциации молекулы (разрыве одной связи) изменяется электронная конфигурация и взаимное расположение оставшихся в молекуле атомов, в результате чего изменяется их энергия взаимодействия. Величина энергии химической связи зависит от начальной энергии молекулы, об этом факте иногда говорят как о зависимости энергии химической связи от температуры. Энергия химической связи — важная характеристика, определяющая реакционную способность вещества и использующаяся при термодинамических и кинетических расчетах реакций химических. Энергия химической связи может быть косвенно определена по данным калориметрических измерений, расчетным способом (см. Квантовая химия), а также с помощью масс-спектроскопии испектрального анализа.
Длина химической связи — расстояние между ядрами химически связанных атомов. Длина химической связи — важная физическая величина, определяющая геометрические размеры химической связи, её протяжённость в пространстве. Для определения длины химической связи используют различные методы. Газовую электронографию, микроволновуюспектроскопию, спектры комбинационного рассеяния и ИК спектры высокого разрешения применяют для оценки длины химических связей изолированных молекул в паровой (газовой) фазе.Межъядерные расстояния в кристаллах определяют с помощью рентгеноструктурного анализа, нейтронографии иэлектронографии.
Считается, что длина химической связи является аддитивной величиной, определяемой суммой ковалентных радиусов атомов, составляющих химическую связь. Л.Полинг в своей книге привёл значения ковалентных радиусов большого числа элементов. Однако, длина химической связи (dAB) между электроотрицательным и электроположительным атомами несколько короче, чем длина, полученная сложением ковалентных радиусов элементов (rA и rB), составляющих молекулу. Поправка на отклонение от принципа аддитивности ковалентных радиусов учитывается уравнением Шомакера-Стивенсона: dAB = rA + rB — 0,09 (χA — χB) и составляет величину k = 0,09 Δχ, где Δχ — разность значений электроотрицательностей атомов χA и χB.
Валентный угол – угол, образованный двумя направлениями химических связей, исходящими из одного атома. Знание В. у. необходимо для определения геометрии молекул. В. у. зависят как от индивидуальных особенностей присоединённых атомов, так и от гибридизации атомных орбиталей центрального атома. Для простых молекул В. у., как и др. геом. параметры молекулы, можно рассчитать методами квантовой химии. Экспериментально их определяют из значений моментов инерции молекул, полученных путём анализа их вращат. спектров
9. Ковалентная связь. Свойства ковалентной связи: насыщаемость, направленность, виды ковалентной связи
Ковалентная связь (атомная связь, гомеополярная связь) — химическая связь, образованная перекрытием (обобществлением) пары валентных электронных облаков. Обеспечивающие связь электронные облака (электроны) называютсяобщей электронной парой.
Термин ковалентная связь был впервые введён лауреатом Нобелевской премииИрвингом Ленгмюром в 1919 году. Этот термин относился к химической связи, обусловленной совместным обладанием электронами, в отличие от металлической связи, в которой электроны были свободными, или от ионной связи, в которой один из атомов отдавал электрон и становился катионом, а другой атом принимал электрон и становился анионом.
Позднее (1927 год) Ф.Лондон и В.Гайтлер на примере молекулы водорода дали первое описание ковалентной связи с точки зрения квантовой механики. С учётом статистической интерпретации волновой функции М.Борна плотность вероятности нахождения связывающих электронов концентрируется в пространстве между ядрами молекулы. В теории отталкивания электронных паррассматриваются геометрические размеры этих пар. Так, для элементов каждого периода существует некоторый средний радиус электронной пары (Å):
0,6 для элементов вплоть до неона; 0,75 для элементов вплоть до аргона; 0,75 для элементов вплоть до криптона и 0,8 для элементов вплоть до ксенона.
НАСЫЩАЕМОСТЬ — характерное свойство ковалентной связи. Она проявляется в способности атомов образовывать ограниченное число ковалентных связей. Это связано с тем, что одна орбиталь атома может принимать участие в образовании только одной ковалентной химической связи. Данное свойство определяет состав молекулярных химических соединений. Так, при взаимодействии атомов водорода образуется молекула Н2, а не Н3. С точки зрения МВС третий атом водорода не может присоединиться, так как спин его электрона окажется параллельным спину одного из спаренных электронов в молекуле. Способность к образованию того или иного числа ковалентных связей у атомов различных элементов ограничивается получением максимального числа неспаренных валентных электронов. НАПРАВЛЕННОСТЬ — свойство ковалентной связи, определяющее геометрическую структуру молекулы. Причина направленности связи заключается в том, что перекрывание электронных орбиталей возможно только при их определенной взаимной ориентации, обеспечивающей наибольшую электронную плотность в области их перекрывания. В этом случае образуется наиболее прочная химическая связь.
Гибридизация атомных орбиталей - способ описания перестройки орбиталей атома в молекуле по сравнению со своб. атомом. Являясь формальным мат. приемом, Г. а. о. позволяет отразить нарушение сферич. симметрии распределения электронной плотности атома при образовании хим. связи. Сущность Г. а. о. состоит в том, что электрон молекулы вблизи выделенного атомного ядра характеризуется не отдельной атомной орбиталью (АО), а линейной комбинацией атомных орбита-лей с разл. значениями азимутального и магнитного квантовых чисел. Такая линейная комбинация наз. гибридной (гибридизированной) орбиталью (ГО). Как правило, гибридизация затрагивает лишь высшие и близкие по энергии занятые АО своб. атома. Напр., для атомов элементов второго периода периодич. системы типичная форма ГО 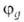 -линейная комбинация 2s-орбитали
-линейная комбинация 2s-орбитали 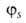 и 2р-орбиталей
и 2р-орбиталей
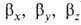
 ,
, 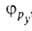
 ,
, 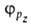
с численными коэффициентами 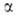 и ГО обладают более низкой симметрией, чем составляющие их АО. Так, распределение электронной плотности, отвечающее указанной ГО
и ГО обладают более низкой симметрией, чем составляющие их АО. Так, распределение электронной плотности, отвечающее указанной ГО  , смещено от атомного ядра в направлении вектора п с координатами
, смещено от атомного ядра в направлении вектора п с координатами 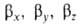 ; вектор пявляется осью симметрии ГО (рис. 1). При изменении ориентации в пространстве осей координат коэффициенты линейной комбинации могут изменяться, однако остается постоянным отношение сумм квадратов коэффициентов для данного значения азимутального квантового числа. Это отношение определяет тип ГО.
; вектор пявляется осью симметрии ГО (рис. 1). При изменении ориентации в пространстве осей координат коэффициенты линейной комбинации могут изменяться, однако остается постоянным отношение сумм квадратов коэффициентов для данного значения азимутального квантового числа. Это отношение определяет тип ГО.
Геометрия молекул. В 1957 г. канадский физикохимик Роналд Джеймс Гиллеспи создал простую, но красивую теорию, которая позволяет с хорошей точностью по структуре Льюиса предсказывать геометрическую форму молекул.Согласно этой теории, во многих простых молекулах химические связи расположены таким образом, что электронные пары, принадлежащие одному атому, максимально удалены друг от друга. Например, в молекуле ВеН2 атом бериллия делит с атомами водорода две пары электронов. Одна пара максимально удалена от другой, когда угол между связями составляет 180°. Это означает, что молекула линейна.
Теория даёт возможность установить геометрическое строение молекул типа AXnEm, где к центральному атому А присоединены n атомов X и имеется также т неподелённых электронных пар (что обозначено символом Еm). Общее число электронных пар m+n составляет от двух до восьми.
В оптимальной конфигурации ядер два заряда находятся на концах диаметра, три заряда образуют правильный треугольник, четыре — тетраэдр, шесть — октаэдр.
Если рассматривать молекулы с четырьмя электронными парами, находящимися в вершинах тетраэдра, то: в молекуле CF4(тип АХ4) все пары принадлежат химическим связям, поэтому атомы фтора также расположены в вершинах тетраэдра. В молекуле NF3 (тип АХ3Е) одна пара электронов азота не участвует в образовании связи, так что молекула имеет форму треугольной пирамиды. Наконец, молекула F2O (тип АХ2Е2) с двумя неподеленными электронными парами имеет угловую форму.
11. Ионная связь. Свойства ионной связи: ненасыщаемость, ненаправленность. Свойства веществ с ионным типом связи
Ионная связь - связь, возникшая между атомами с резко выраженными противоположными свойствами (типичным металлом и типичным неметаллом), между которыми возникают силы электростатического притяжения, называется электровалентной, или ионной связью. Соединения, образовавшиеся путем притяжения ионов, называются гетерополярными, или ионными. (FrF – самое типичное ионное соединение, NaCl). Образование таких соединений получается из атомов, резко отличающихся по значению электроотрицательности, в результате перехода электронов от атомов одних элементов к другим. Ионные соединения возникают между элементами I и II групп с элементами главных подгрупп VI и VII групп. Типичные металлы имеют на внешнем энергетическом уровне не более 3-х электронов, которые они отдают, превращаясь в положительно заряженные катионы, а типичные неметаллы, имеющие 6–7 электронов на внешнем валентном уровне, принимают недостающие электроны, превращаясь в отрицательно заряженные катионы, т. е. электронные оболочки соединяющихся элементов превращаются в электронную оболочку (завершенный уровень) благородных газов. Вещества с ионной связью имеют кристаллическую решетку, твердые, являются электролитами, с высокими температурами кипения и плавления, при растворении в воде или плавлении проявляют свойства сильных электролитов. Ионная связь – производная ковалентной связи в результате односторонней поляризации общей электронной пары, переходящей во владение одного из соединяющихся атомов.
Одностороннюю поляризацию осуществляет атом хлора, обладающего ярко выраженными неметаллическими свойствами. Электроны переходят от атома натрия, имеющего типичные металлические свойства, к атому хлора. В результате к атому хлора смещается общее электронное облако. Ионная связь – высшая степень ковалентной неполярной связи. Ко-валентная полярная связь является промежуточной формой между ионной и ковалентной неполярной связью.
Природа образования ко-валентной и ионной связи едина, принципиальных отличий не существует. Различие состоит в степени поляризации. Ионной связи характерны ненасыщаемость – каждый ион, взаимодействуя с противоположным во всех направлениях, не компенсирует силовые поля, и ненаправленность – любой ион в любом направлении способен притягивать к себе ион противоположного заряда. В результате этих свойств ионные соединения представляют собой твердые тела с ионной кристаллической решеткой. 100 %-ной ионной связи не существует. Существует степень или доля ионности связи – в соединении СsF ионная связь имеет долю 89 %. Так как ион может притягивать к себе ионы противоположного знака в любом направлении, ионная связь в отличие от ковалентной отличается ненаправленностью.
Взаимодействие друг с другом двух ионов противоположного знака не может привести к полной взаимной компенсации их силовых полей. Поэтому они могут притягивать и другие ионы противоположного знака, то есть ионная связь отличается ненасыщенностью.
Растворимость – свойство веществ с ионным видом, это -способность вещества образовывать с другим веществом (или веществами) гомогенные смеси с дисперсным распределением компонентов (см. Растворы). Обычно растворителем считают вещество, которое в чистом виде существует в том же агрегатном состоянии, что и образовавшийся раствор. Если до растворения оба вещества находились в одном и том же агрегатном состоянии, растворителем считается вещество, присутствующее в смеси в существенно большем кол-ве.
Растворимость определяется физическим и химическим сродством молекул растворителя и растворяемого вещества, соотношением энергий взаимодействием однородных и разнородных компонентов раствора. Как правило, хорошо растворимы друг в друге подобные по физ. и хим. свойствам вещества (эмпирич. правило "подобное растворяется в подобном"). В частности, вещества, состоящие из полярных молекул и вещества с ионным типом связи хорошо раств. в полярных растворителях (воде, этаноле, жидком аммиаке), а неполярные вещества хорошо раств. в неполярных растворителях (бензоле, сероуглероде).
Согласно теории, предложенной Дж. Гильдебрандом (1935), взаимная растворимость неэлектролитов возрастает с уменьшением разности их параметров растворимости d=(Е/V)1/2, где Е-теплота испарения, V-полярный объем. Параметр растворимости - одно из осн. понятий, определяющих когезионные свойства веществ в конденсир. состояниях; важная технол. характеристика полимеров и растворителей, лакокрасочных материалов и т.п.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 2046; Нарушение авторских прав?; Мы поможем в написании вашей работы!