
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Для бинарного раствора, состоящего из компонентов А и В, неограниченно растворимых друг в друге, общее давление пара, согласно первому закону Рауля, равно
|
|
|
|
Таким образом, осмотическое давление в разбавленных растворах численно равно тому давлению, которое производило бы то же число молекул растворенного вещества, если бы оно в виде идеального газа занимало бы при данной температуре объем, равный объему раствора.
Или
πV = nRT, (14)
где с – концентрация растворенного вещества (моль∙л-1),
n – число молей растворенного вещества,
V - объем раствора.
Осмотические эффекты чрезвычайно важны в биологических системах, поскольку большинство биологических мембран – стенки кишечника, стенки клеток – полупроницаемы. Осмос обусловливает поднятие воды по стеблю растений, рост клетки и многие другие явления. Слишком большой градиент концентрации приводит к разрыву или высушиванию клетки. Животные клетки имеют систему защиты, основанную на осморегуляции: организм животного стремится поддерживать осмотическое давление всех тканевых жидкостей на постоянном уровне. Например, осмотическое давление крови человека – 800 000 Н∙м-2. Такое же осмотическое давление имеет 0,9 %-ный раствор хлорида натрия - изотоничный крови физиологический раствор, широко применяется в медицине.
Давление пара растворителя и растворенного вещества. Закон Рауля. Закон Генри.
Если компоненты бинарного (состоящего из двух компонентов) раствора летучи, то пар над раствором будет содержать оба компонента.
Согласно закону Рауля парциальное давление насыщенного пара растворителя над раствором (рi) прямо пропорционально его мольной доле в растворе
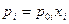 , (15)
, (15)
причем коэффициент пропорциональности (р0i) равен давлению насыщенного пара над чистым растворителем при данной температуре.
Поскольку сумма мольных долей всех компонентов раствора равна единице, для бинарного раствора легко получить следующее соотношение, также являющееся формулировкой первого закона Рауля:
|
|
|
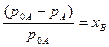 (16)
(16)
(относительное понижение давления пара растворителя над раствором равно мольной доле растворенного вещества и не зависит от природы растворенного вещества).
Закон Рауля выполняется для идеальных растворов. Идеальными при любых концентрациях можно считать растворы, компоненты которых близки по физическим и химическим свойствам (оптические изомеры, гомологи и т.п.), образование которых не сопровождается объёмными и тепловыми эффектами. Растворы, компоненты которых существенно различаются по физическим и химическим свойствам, подчиняются закону Рауля лишь в области бесконечно малых концентраций (предельно разбавленные растворы, в которых молярная доля растворенного вещества не превышает 0,005).
Для предельно разбавленного раствора давление пара растворенного вещества подчиняется закону Генри: парциальное давление (рi ) насыщенного пара растворенного вещества пропорционально его мольной доле в растворе:
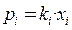 , (17)
, (17)
где ki – константа Генри, имеющаяразмерность давления и определяемая природой газа.
Таким образом, в предельно разбавленных реальных растворах растворитель подчиняется закону Рауля, а растворенное вещество – закону Генри.
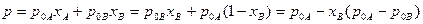 (18)
(18)
Т.е. для идеальных растворов зависимость общего и парциальных давлений насыщенного пара от состава раствора является линейной при любых концентрациях (рис.6.).
 |
Рис. 6. Зависимость парциальных и общего давлений пара идеального раствора от концентрации. (р0А, р0В – давление насыщенного пара над чистыми жидкими компонентами А и В при данной температуре.)
Неидеальные раcтворы не подчиняются закону Рауля в форме pi = p0i×xi. Для них отношение pi / p0i равно уже не мольной доле xi, а некоторой функции ai - термодинамической активности i -ого компонента в растворе, которая зависит как от температуры, так и от состава раствора. По физическому смыслу активность – это такая концентрация данного компонента в идеальном растворе, при которой он в последнем имеет такой же химический потенциал, что и в реальном растворе
|
|
|
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 611; Нарушение авторских прав?; Мы поможем в написании вашей работы!