
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Атом состоит из компактного и массивного положительно заряженного ядра и отрицательно заряженных легких электронов, обращающихся вокруг него
|
|
|
|
Раздел физики, изучающий строение и состояние атомов, называют атомной физикой. Реальные сомнения в том, что атом является неделимой материальной частицей, появились в конце 19-го века, когда английский физик Дж. Томсон открыл электрон, входящий в состав электронейтрального атома. Из экспериментов следовало, что масса электрона примерно в 2000 раз меньше массы самого лёгкого атома, а значит, основная часть массы атома заряжена положительно. В 1903 г. Томсон предложил модель строения атома, согласно которой атом имеет форму шара диаметром около 10-10 м (расстояние между узлами кристаллической решётки твёрдых тел), внутри которого равномерно распределён положительный заряд, а отрицательно заряженные электроны находятся внутри этого шара, как изюминки в кексе (рис. 33а).
В 1909–1911 годах английский физик Э. Резерфорд и его сотрудники Х. Гейгер и Э. Марсден исследовали структуру атома с помощью быстрых положительно заряженных частиц. В качестве таких частиц были использованы так называемые a-частицы, возникающие при распаде радия и некоторых других радиоактивных элементов. Заряд a-частиц равен двум элементарным, а масса - примерно 4 а.е.м. Установка, использованная Резерфордом в этих опытах (рис. 33б), состояла из свинцового контейнера 1, содержащего крупицу радия, из которого вдоль узкого канала вылетал пучок a-частиц 2, падающий на лист тонкой металлической фольги 3. За фольгой был помещен полупрозрачный цилиндрический экран 4, покрытый кристаллами сульфида цинка, свечение которых под ударами a-частиц наблюдали с помощью микроскопа 5.
В опытах Резерфорда a-частицы сталкиваются с атомами фольги, и при каждом таком столкновении a-частица, пролетая через электрическое поле атома, изменяет направление движения (испытывает рассеяние). Электроны, имеющие гораздо меньшую массу, чем a-частица, не могут изменять направление движения a-частиц. Поэтому, изучая рассеяние a-частиц можно оценить размеры положительно заряженной части атома. Оказалось, что бóльшая часть a-частиц, несущихся со скоростью около 1/15 скорости света, проходит через тонкую фольгу почти не рассеиваясь, что соответствовало модели атома Томсона, в которой положительный заряд был равномерно распределён по объёму всего атома (рис. 33а). Однако очень малая доля a-частиц отклонялась на углы более 90°(см. рис. 33б), что было невозможно объяснить, пользуясь моделью Томсона, т.к. электрическое поле однородно заряженного шара недостаточно велико на его поверхности и убывает до нуля по мере приближения к центру шара.
|
|
|
Чтобы объяснить, почему некоторые a-частицы могут быть отброшены назад атомом, Резерфорд предложил принципиально новую модель атома, в которой весь положительный заряд атома и почти вся его масса сконцентрированы в теле очень малых размеров атомном ядре. Такую модель атома называют ядерной. Согласно оценкам Резерфорда диаметр атомных ядер должен составлять 10-14 – 10-15 м. Таким образом, размеры атома в 104-105 раз превышают размеры его ядра, а максимальная напряжённость электрического поля в ядерной модели атома превышает его напряжённость в модели Томсона в 108-1010 раз, что и делает возможным рассеяние быстрых a-частиц на большие углы.
Основываясь основе ядерной модели атома, Резерфорд предположил, что атом устроен подобно солнечной системе – вокруг ядра, как вокруг Солнца, обращаются электроны, как планеты (рис. 33в). При этом в нейтральном атоме суммарный отрицательный заряд электронов должен компенсировать положительный заряд ядра. Такая модель строения атома была названа планетарной. В планетарной модели электроны должны обращаться вокруг ядра, чтобы не упасть на него под действием кулоновских сил притяжения.
|
|
|
Вопросы для повторения:
· Какую модель строения атома предложил Томсон?
· Какие результаты были получены в опытах Резерфорда?
· Какую модель строения атома и почему предложил Резерфорд?
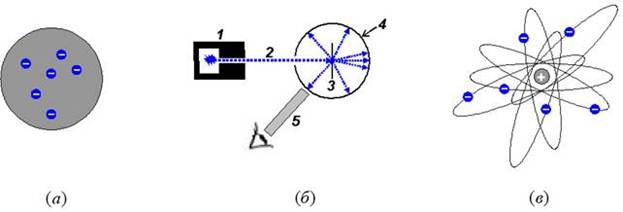
Рис. 33. (а) –модель строения атома, предложенная Томсоном; (б) – схема опытов Резерфорда; (в) – планетарная модель строения атома.
|
|
|
|
|
Дата добавления: 2014-11-08; Просмотров: 981; Нарушение авторских прав?; Мы поможем в написании вашей работы!