
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методические указания. 1. При решении задач на первое начало термодинамики прежде всего необходимо установить характер процесса
|
|
|
|
1. При решении задач на первое начало термодинамики прежде всего необходимо установить характер процесса, протекающего в газе.
2. В изохорном и изобарном процессе 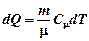 , где Сm = СVm - в изохорном процессе, Сm = СРm - в изобарном процессе. Так как обе молярные теплоемкости больше нуля, то знак dQ совпадает со знаком dT. Значит, при нагревании (dT > 0) газ тепло получает (dQ > 0), при охлаждении - отдает тепло (dQ < 0).
, где Сm = СVm - в изохорном процессе, Сm = СРm - в изобарном процессе. Так как обе молярные теплоемкости больше нуля, то знак dQ совпадает со знаком dT. Значит, при нагревании (dT > 0) газ тепло получает (dQ > 0), при охлаждении - отдает тепло (dQ < 0).
3. При изотермическом процессе dT = 0, dQ может быть больше и меньше нуля. При адиабатическом процессе dQ = 0, хотя газ может нагреваться (dT > 0), если над ним совершают работу внешние силы, или охлаждаться (dT < 0), если он сам совершает работу за счет своей внутренней энергии.
4. При решении задач на расчет изменения энтропии следует помнить, что:
а) энтропия является функцией состояния;
б) энтропия системы равна сумме энтропий ее частей (свойство аддитивности).
5. Если переход тела из начального состояния в конечное осуществляется несколькими последовательными процессами, то полное изменение энтропии равно алгебраической сумме изменений энтропии в каждом процессе. Формула 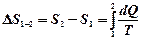 дает изменение энтропии при переходе тела из состояния 1 в состояние 2. Расчет изменения энтропии в различных процессах будет ясен после решения задач 23-29.
дает изменение энтропии при переходе тела из состояния 1 в состояние 2. Расчет изменения энтропии в различных процессах будет ясен после решения задач 23-29.
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 330; Нарушение авторских прав?; Мы поможем в написании вашей работы!