
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Общие химические свойства оксидов
Амфотерные оксиды
Амфотерность (от греч. amphoteros — и тот и другой) — способность химических соединений (оксидов, гидроксидов, аминокислот) проявлять как кислотные, так и основные свойства, в зависимости от свойств второго реагента, участвующего в реакции.
Одно и то же вещество (например, ZnO), реагируя с сильной кислотой или кислотным оксидом, проявляет свойства основного оксида:
ZnO + 2 HCl = ZnCl2 + H2O
ZnO + SO3 = ZnSO4.
а при взаимодействии с сильным основанием или основным оксидом – свойства кислотного оксида:
ZnO + 2 NaOH + H2O = Na2[Zn(OH)4] (в водном растворе)
ZnO + CaO 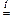 CaZnO2 (при сплавлении).
CaZnO2 (при сплавлении).
Амфотерные оксиды способны вытеснять летучие оксиды из солей:
K2CO3 + ZnO 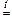 K2ZnO2 + CO2.
K2ZnO2 + CO2.
Оксиды могут участвовать в окислительно-восстановительных реакциях приводящих к изменению степени окисления данного элемента:
1°. Восстановление оксидов. Восстановители (C, CO, H2, CH4, и др., активные металлы, такие как Mg, Al) при нагревании восстанавливают многие элементы из оксидов до простых веществ:
ZnO + C 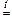 Zn + CO
Zn + CO
WO3 + 3 H2 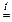 W + 3 H2O
W + 3 H2O
3 CuO + 2 NH3 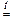 3 Cu + N2 + 3 H2O
3 Cu + N2 + 3 H2O
P4O10 + 10 C 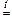 P4 + 10 CO
P4 + 10 CO
9 CuO + 2 CH3NH2 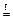 9 Cu + N2 + 2 CO2+ 5 H2O
9 Cu + N2 + 2 CO2+ 5 H2O
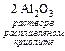
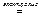 4 Al + 3 O2
4 Al + 3 O2
CuO + CO 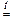 Cu + CO2
Cu + CO2
Cr2O3 + 2 Al 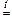 2 Cr + Al2O3
2 Cr + Al2O3
SiO2 + 2 Mg 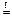 Si + 2 MgO
Si + 2 MgO
2 NO2 + 4 Cu 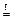 2 N2 + 4 CuO
2 N2 + 4 CuO
CO2 + 2 Mg 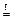 C + 2 MgO.
C + 2 MgO.
2°. Окисление оксидов. Оксиды элементов, проявляющих переменные степени окисления, могут участвовать в реакциях, приводящих к повышению степени окисления данного элемента:
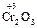 + 4 NaOH + 3 NaNO3
+ 4 NaOH + 3 NaNO3 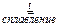 2
2 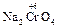 + 3 NaNO2 + 2 H2O
+ 3 NaNO2 + 2 H2O
3 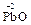 + KClO3
+ KClO3 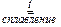 3
3 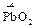 + KCl
+ KCl
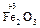 + 4 KOH + 3 KNO3
+ 4 KOH + 3 KNO3  3 KNO2 + 2
3 KNO2 + 2 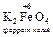 + 2 H2O
+ 2 H2O
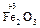 + 3 Cl2 + 10 KOHконц.
+ 3 Cl2 + 10 KOHконц. 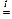 2
2 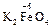 + 6 KCl + 5 H2O
+ 6 KCl + 5 H2O
2 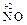 + O2 = 2
+ O2 = 2 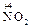
2 NO2 + O3 = 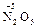 + O2.
+ O2.
3°. Пассивация оксидов. Термическое разложение гидроксидов при высоких температурах (> 1000°C) приводит к получению оксидов в химически малоактивной форме. Оксиды полученные таким путем не растворяются ни в кислотах, ни в щелочах. Перевести их в растворимое состояние можно только лишь сплавлением с кислыми солями или щелочами. Примером могут служить оксиды алюминия, хрома, титана.
Глава 2
|
|
Дата добавления: 2014-11-16; Просмотров: 530; Нарушение авторских прав?; Мы поможем в написании вашей работы!