
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
НЛ .Ефименко
|
|
|
|
Лечение огнестрельных ранений живота
Частота огнестрельной травмы сохраняет тенденцию к увеличению, как в локальных войнах и вооруженных конфликтах, так и в практике гражданского здравоохранения. В период проведения боевых действий доля огнестрельных ранений живота составляет 4,7-8,8 %, а в группе умерших достигает
80 %. Увеличение огнестрельных ранений живота в структуре санитарных потерь можно объяснить, наряду с совершенствованием стрелкового оружия, сокращением сроков доставки раненых в лечебные учреждения и возросшим уровнем анестезиологического и реаниматологического обеспечения.
Классификация огнестрельных ранений живота представлена на схеме 1.
Диагностика
Одним из сложных разделов экстренной хирургии является своевременная диагностика повреждений органов при огнестрельных ранениях живота. Тяжесть их поражения нередко маскируется шоком, отсутствием сознания. Поэтому патологические изменения в брюшной полости можно выявить только с помощью комплекса обследований (диагностического алгоритма), включающих как неинвазивные (ультразвуковое исследование, полипозиционное рентгенологическое обследование органов грудной клетки и брюшной полости), так и инвазивные (лапароцентез, лапароскопию) методы исследования (схема.2).
При ранениях живота выделяют три группы преобладающих синдромов: перитонита (при повреждении полых органов), встречающегося в 15-18 % случаях, внутрибрюшной кровопотери (при ранении паренхиматозных органов, большого сальника, брыжейки тонкой кишки) - в 50—55 %, а также сочетания кровотечения и развивающегося перитонита.
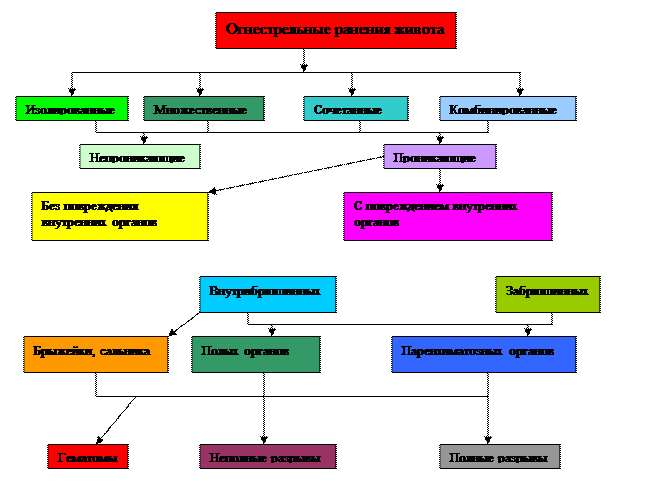
Схема 1. Классификация огнестрельных ранений живота
|
|
|
Последний синдром возникает обычно при одновременном повреждении полых и паренхиматозных органов - в 30-35 % наблюдений.
Обзорная рентгенография (при тяжелом состоянии пострадавшего в латеропозиции) преследует обнаружение свободного газа в брюшной полости и косвенных признаков наличия в ней жидкости. К косвенным признакам наличия свободной жидкости в брюшной полости относят: высокое положение и ограничение подвижности купола диафрагмы; реактивный выпот в плевральной полости; дисковидные ателектазы в нижних отделах легких; «потерю» нормальной толщины мышц и неровность линий предбрюшинного жира; увеличение расстояния между боковой стенкой брюшной полости и восходящей ободочной кишкой; прогрессирующее вздутие кишечных петель и «всплытие» их на поверхность; расширение межпетлевых промежутков (картина звездчатых тканей в центральных областях и лентовидных - в проекции боковых каналов). Кроме того, в области поврежденного полого органа обнаруживается вздутие какой-либо одной петли тонкой кишки (симптом «дежурной петли»), а скопление отдельных пузырьков газа встречаются при разрывах забрюшинно расположенных органов (двенадцатиперстная кишка, восходящая и нисходящая ободочная). Обнаружение инородных тел внутри брюшной полости облегчает постановку диагноза и воссоздание хода раневого канала.
При ранениях живота применяют специальные методы рентгенологического исследования. К их числу относится контрастная ангиография, которая информативна при повреждениях печени, почек, селезенки, поджелудочной железы и двенадцатиперстной кишки. Артериографическим подтверждением нарушения целости внутренних органов и магистральных сосудов живота служит экстравазация контрастирующего вещества в местах гематом либо выявление артериовенозного шунтирования сразу после его введения.
|
|
|
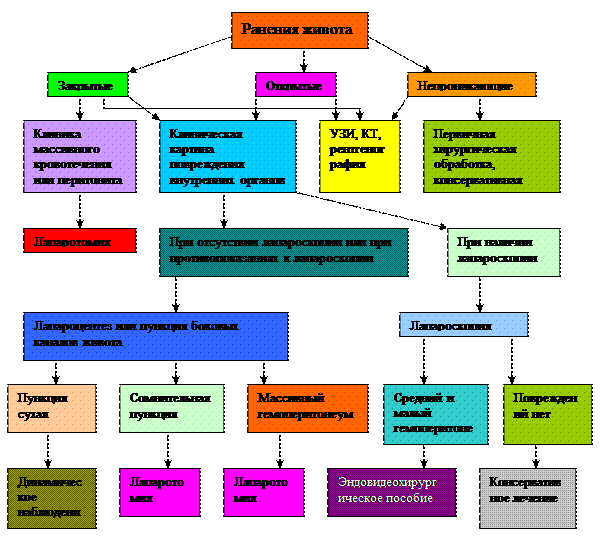
Схема. 2. Диагностический алгоритм при ранениях органов живота
Другую специальную рентгенологическую методику - контрастирование раневого канала (вульнерографию) - применяют для идентификации проникающего характера ранения. Через катетер в раневой канал вводят до 10 мл водорастворимого контрастирующего вещества, и производят рентгенографию в двух основных проекциях. Растекание рентгеноконтрастного вещества в полости брюшины свидетельствует о проникающем характере ранения, а скопление в подкожной клетчатке, мышечной ткани - о целости париетальной брюшины.
Высокоинформативным неинвазивным методом диагностики является ультразвуковое исследование. Сокращая время обследования пострадавших, обеспечивая возможность динамического наблюдения, метод позволяет обнаружить наличие свободной жидкости до 200,0 мл с точностью 94-95 %, от 200,0 до 500,0 мл - 98-99 %. По изменению размеров и конфигурации (неровности контуров и деформации), нарушений однородности структуры, отсутствие характерной УЗИ-картины в этой области, наличии ан- или гипоэхогенных образований характерных для подкапсульных гематом, зон повышенной эхогенности можно судить о характере повреждений паренхиматозных органов. УЗИ-диагностика внутрибрюшного кровотечения основана на симптоме»разобщения» париетального и висцерального листков брюшины в латеральных каналах брюшной полости, где наиболее часто скапливается свободная жидкость. Наиболее достоверным является УЗИ-картина трех анатомических областей: правого подпеченочного пространства, правой подвздошной ямки, полости малого таза. Определение во всех трех зонах свободной жидкости свидетельствует, о том, что ее объем составляет не менее 250 мл.
Ценность метода заключается в том, что с его помощью удается визуализировать те повреждения органов, которые еще не привели к возникновению внутрибрюшного кровотечения. Речь идет о диагностике подкапсульных и внутрипаренхиматозных гематом. Внутрипаренхиматозные гематомы чаще всего определяются в виде звездчатого или овоидного эхонегативного образования с нечеткими, неровными контурами. Подкапсульные гематомы печени и селезенки на эхограммах определяются как линейные или серповидные образования.
|
|
|
В то же время и этот метод не лишен недостатков (во всяком случае - на современном уровне развития техники). Он малоинформативен в диагностике ранений полых органов. Выраженное вздутие кишечника или наличие эмфиземы мягких тканей экранирует практически всю картину со стороны брюшной полости и делает УЗИ недостаточно эффективным.
Рентгеновская компьютерная томография является наиболее информативным методом, однако ее применение бывает ограничено сложностью, длительностью и дороговизной исследования, наличием ряда противопоказаний (нестабильная гемодинамика). Тем не менее, у раненых с компенсированным состоянием применение этого метода оправдано. Он позволяет получить высокую диагностическую информацию во всех случаях использования: либо устанавливается факт повреждения внутреннего (чаще паренхиматозного) органа, либо выявляется другая патология (например, забрюшинная гематома).
Диффузные изменения печени и селезенки при КТ выражаются равномерным увеличением органов, округлостью контуров, неоднородностью их структуры, незначительным снижением их плотности. Подкапсульно расположенные гематомы характеризуются наличием в периферических отделах органа серповидных или линзовидных зон с четкими ровными контурами, чаще однородной структуры. Для центральных гематом характерно наличие множественных зон округлой формы с нечеткими неровными контурами, повышенной плотностью патологического образования в органе.
Лапароцентез, выполняемый по методике Н.К. Голобородько, является простым, быстрым и щадящим методом диагностики с достоверностью обнаружения патологического содержимого в брюшной полости 90-91 %.
Для определения возможного поступления крови из забрюшинного пространства используют методику сравнительного определения гематокрита в кровянистом содержимом брюшной полости и на периферии, основанную на том, что при забрюшинных гематомах в брюшную полость в основном поступает плазма, а форменные элементы крови задерживаются в забрюшинной клетчатке. Обнаружение в промывных водах из брюшной полости числа эритроцитов менее 100 х 106/мл служит показанием к консервативному лечению, при результатах лаважа с числом эритроцитов в диапазоне от 100 х 10б/мл до 750 х 106/мл, прибегают к видеолапароскопии, а число эритроцитов при лаваже, превышающее 750 х 106/мл, требует выполнения неотложной лапаротомии.
|
|
|
Обнаружение продолжающегося внутрибрюшного кровотечения основывается на положительной пробе Рувилуа - Грегуара. Время, затраченное на это инструментальное исследование, составляет в среднем 5-10 минут. Однако отрицательные результаты однократного исследования, выполненного в ближайший час после ранения, не дают основания полностью исключить возможность двухмоментного разрыва паренхиматозных, а также забрюшинно расположенных полых органов, в том числе и при промывании брюшной полости. Ложноположительные результаты бывают обусловлены поздним выполнением (через 3 часа после ранения) лапароцентеза, когда кровь (при огнестрельных переломах костей таза) из забрюшинной гематомы начинает просачиваться через брюшину в полость живота. Ложноотрицательные результаты бывают получены при повреждении забрюшинно расположенных полых органов живота.
Эндовидеоскопические методы исследования как принципиально новое направление в диагностике ранений живота настолько «очаровали» хирургов своей кажущейся простотой и почти 100 % информативностью (разрешающая способность метода составляет 98-99 %), что они стали повсеместно вытеснять все другие. Наряду с этим видеолапароскопия может быть использована не только как диагностический метод, но в некоторых случаях как лечебный.
Ургентная видеолапароскопия при ранениях органов живота позволяет: 1) в кратчайшие сроки диагностировать повреждения; 2) сократить время предоперационного обследования; 3) избежать диагностических лапаротомий; 4) избрать правильную лечебную тактику; 5) выбрать адекватный конкретной ситуации способ лечения и оптимальный доступ; 6) в 6,5-17 % случаев решить вопрос о возможности завершения диагностического вмешательства лечебной видеолапароскопией.
Время проведения диагностической видеолапароскопии составляет в среднем 27-30 минут.
Хирургическая тактика
Современная хирургия ранений органов живота требует в первую очередь изучения вопросов временного и окончательного гемостаза.
Способы временного и окончательного гемостаза и частота их использования при огнестрельных ранениях и травмах органов живота представлены в таблице 1.
Таблица 1. Частота использования временных и окончательных методов гемостаза на паренхиматозных органах живота
| Способы гемостаза | Частота применения, % |
| Сдавление печеночной ткани руками | 37,8 |
| Сдавление селезеночной ткани руками | 45,5 |
| Сдавление печеночной ткани зажимом | 26,7 |
| Методика «забытых» тампонов по I.Shelle | 6,7 |
| Сдавление печени кетгутовой сеткой | 8,9 |
| Исключение воротных и кавальных сосудистых структур из системы печеночного кровотока | 75,6 |
| Временный портокавальный шунт | |
| Шов печени | 44,4 |
| Шов селезенки | 36,4 |
| Физические методы окончательного гемостаза | 36,9 |
| Фармакологические методы окончательного гемостаза | 69,8 |
| Гепатопексия по Киари-Алферову или Шапкину | 11.1 |
Эффективным средством гемостаза является методика «окутывания» печени или селезенки кетгутовой сеткой или сеткой из полиглактина 910
(Vicryl). Операция выполняется быстро, при этом максимально сохраняется функционирующая часть паренхимы органа, исключается развитие вторичного послеоперационного кровотечения, функция органа восстанавливается в течение 1-3 суток с момента операции. Применение рассасывающейся сетки позволяет сохранить орган у многих пострадавших, при этом отмечена эффективность, безопасность метода при использование его при обширных глубоких повреждениях селезенки, в том числе в области ворот.
Значительно реже используют методику «забытых» тампонов, разработанную I.Shelle и заключающуюся в плотном окутывании поврежденной печени несколькими слоями марлевых салфеток. Рану передней брюшной стенки зашивают по типу лапаростомии. Салфетки удаляют на 5-7 сутки после образования вокруг раны печени плотных фибринозных сращений.
Исключение воротных и кавальных сосудистых структур из системы печеночного кровотока используют также для остановки кровотечения. Среди них временное пережатие печеночно-двенадцатиперстной связки (ПДС) является эффективным приемом борьбы с профузным кровотечением при травмах печени. Пережатие ПДС осуществляют иногда с полным выключением печени из кровотока (пережатие над- и подпеченочного отделов нижней полой вены). Однако длительные окклюзии связки всегда в той или иной мере повреждают печень и несут в себе угрозу развития печеночной недостаточности. С целью уменьшения негативных последствий ПДС следует придерживаться следующих требований: 1) осуществлять пережатие ПДС не более 30 мин. с 5 мин. восстановлением кровотока в печени через 15 минут окклюзии, а при полном выключении не более 10 мин.; 2) переливание в момент устранения окклюзии ПДС перфторана (20 мл/кг массы) снижает выраженность повреждения ткани печени. В случаях отсутствия последнего, может быть использована комбинация препаратов из изотонического раствора хлорида натрия (30 мл/кг) и реополиглюкина (15 мл/кг); 3) осуществлять медленное восстановление кровотока после ПДС.
Существенным недостатком этого способа является быстрое скопление крови в бассейне воротной вены на фоне исходного дефицита ОЦК. Клинически это выражается падением АД, тахикардией, и остановкой сердечной деятельности.
С целью предотвращения депонирования крови в бассейне воротной вены при прекращении афферентного кровотока печени, используют временный портокавальный шунт А.Е.Борисова: берут систему для забора крови и иглой пунктируют любую крупную ветвь воротной вены (чаще всего правую желудочно-сальниковую вену). После заполнения кровью системы иглу на противоположном конце системы вводят в нижнюю диафрагмальную либо внутреннюю подвздошную вену. После окончательного гемостаза печени и миновании надобности в шунте, последний удаляют, и вены перевязывают. Преимущество данного способа заключается в быстроте, простоте исполнения и хорошей эффективности.
В настоящее время имеется значительное число различных механических и физических методов (аппаратов), позволяющих достичь полной остановки паренхиматозного крово- и желчеистечения с поверхности поврежденной печени.
Своим развитием хирургия печени обязана исследованиям М.М. Кузнецова и Ю.Р. Пенского (1894), которые предложили швы для ушивания ран печени.
В настоящее время предложено большое количество разнообразных швов печени: от простого узловатого до сложных швов с применением различных алло- и аутоматериалов, препятствующих прорезыванию швов. Основными требованиями к шву печени являлся хороший гемо- и желчестаз, а также минимальное нарушение кровоснабжения паренхимы печени в сопредельных областях.
Наиболее приемлемы для выполнения этих задач являются узловые и блоковидные швы Замошина и шов через пластинки ткани или фасции, брюшину. После «резекции-обработки» ран печени применяют также шов с использованием в качестве шовного материала полосок аутокожи.
Большинство из физических методов применяют для хирургических вмешательств с использованием как традиционных, так и мини-инвазивных подходов.
В нашей стране для этих целей наиболее часто пользуется моно- или биполярная электокоагуляция, электрокоагуляция усиленная аргоном (аргоновый коагулятор), плазменные потоки, излучения лазера (чаще всего гранатового -Nd:YAG), спрэй-коагуляция. Из этих методов наибольшим гемостатическим эффектом обладает излучение Nd:YAG лазера (длина волны излучения 1,06 мкм), а также плазменные потоки (аргоновая плазма).
Для окончательного гемостаза используют также фармакологические средства. Из всех фармакологические средств, используемых с этой целью, наиболее эффективными являются фибриновый клей («Тиссукол», Австрия) и комбинация фибринового клея с коллагеновой волокнистой пластиной («Та-хоКомб», Норвегия).
Если при повреждении печени IV ст. не удается устранить дефект паренхимы, прибегают к гепатопексии - подшиванию свободного края печени к пристеночной брюшине по Киари-Алферову (верхняя гепатопексия) или выполняют заднюю гепатопексию по Шапкину.
Среди методов окончательного гемостаза используют с успехом также тампонаду раны селезенки сальником на ножке. Такую же методику используют и при повреждениях печени.
Показаниями к тампонаде раны печени или селезенки сальником на «ножке» являются: 1) невозможность захвата дна раны при ее ушивании и отсутствии сильного кровотечения, 2) дефект в ткани печени после иссечения сегмента, субсегмента, когда стянуть края раны путем гепатизации не представлялось возможным из-за опасности натяжения и прорезывания швов, а также развития ишемии сопредельных участков; 3) центральные разрывы с формированием полости, которая через узкий канал сообщалась с брюшной полостью. После обработки такой раны ушивание полости невозможно и опасно, поэтому тампонада её сальником позволяет закончить операцию без стягивания «стенок» полости.
Ранения печени
Хирургическая тактика при повреждениях печени в первую очередь зависит от тяжести ранения органа. Мы используем четырехстепенную классификацию тяжести повреждений печени: I степень (гематомы, разрывы глубиной до 3 см встречаются в 45 % случаев, II степень (центральные разрывы более 3 см глубиной - 36 %, III степень (размозжение доли или множественные разрывы обеих долей - 14 %, IV степень (размозжение паренхимы и повреждение печеночных вен и /или воротной вены - 5 %.
В зависимости от характера и тяжести повреждений печени выполняются как «традиционные» так и эндоваскулярные вмешательства, а также операции с использованием видеолапароскопической техники, частота использования которых составляет соответственно 75,6 %, 4,4 % и 20 %.
При «традиционных» операциях и внутрипеченочных разрывах с образованием полости производится ее вскрытие, ревизия раны с обязательной перевязкой кровоточащих сосудов, тампонада сальником на ножке и ушивание. При глубоких ранах печени обычно необходим доступ к дну ее, который выполняют путем разъединения паренхимы по малососудистым участкам по ходу внутри-органных фиссур с последующей перевязкой сосудов и желчных ходов. Поскольку раны имеют форму желоба, то прибегают к сближению их краев атравматическим швами поверх уложенной на ее дно дренажной трубки.
При 3 ст. тяжести, как правило, выполняют резекции печени (атипичные сегмент - или лобэктомии), а для достижения гемостаза используют физические методы или производят герметизацию раневой поверхности с помощью «ТахоКомба» или «Тиссукола».
При 4 ст. удаляют нежизнеспособные участки печени и производят в зависимости от локализации раны верхнюю (по Киари) или нижнюю (по В.С.Шапкину) гепатопексию после укрытия раны пластинкой «ТахоКомб». При неэффективности гемостаза печень плотно укутывают кетгутовой сетью или гемостаз достигают за счет использования методики оставления «забытых» тампонов. Кроме того, всем пострадавшим обеспечивают адекватное дренирование области повреждения путем активной аспирации.
Операции с использованием видеолапароскопической техники возможны у пострадавших без выполнения конверсии при гемоперитонеуме до 1000 мл без признаков продолжающегося внутрибрюшного кровотечения и повреждениях печени I— II ст. тяжести. Среди них выполняют герметизацию ран пластинкой «ТахоКомб», лазерную или ультразвуковую коагуляцию.
С использованием видеолапароскопической техники выполняют также ушивание с герметизацией линии швов пластинкой «ТахоКомб» и производят пункцию и эвакуацию крови из подкапсульной гематомы.
В последние годы в связи с развитием эндоваскулярной хирургии для гемостаза с успехом применяют методику рентгеноэндоваскулярной окклюзии ветвей печеночной артерии. Трансфеморальным или трансаксиллярным доступом по Сельдингеру проводят селективную катетеризацию артериального русла и определяют состояние кровотока. Затем катетер суперселективно подводят к источнику кровотечения и осуществляют эндоваскулярную редукцию печеночного артериального кровотока введением в просвет сосуда различных окклюзирующих устройств. Чаще всего с этой целью применяют спирали Гиантурко.
Ранения селезенки
При выборе объема хирургического вмешательства основное значение имеет характер и тяжесть повреждения. Выделяем четыре степени тяжести травмы селезенки: I степень - повреждение капсулы и (или) паренхимы глубиной менее 1 см отмечается в 31 % случаев, II степень - разрыв глубиной от 1 до 3 см - 24 %, III степень - разрыв глубиной выше 3 см - 33,3 %, IV степень - полное разрушение органа - 11,2 %.
Современная хирургическая тактика при ранениях селезенки предполагает изучение возможности выполнения органосохраняющих операций (ОСО), в том числе, выявления факторов, влияющих на отказ от их выполнения.
Накопленный клинический опыт убеждает в том, что абсолютные показания к органосберегающей операции на селезенке имеют место у 39,4 % оперированных раненых, относительные - у 32 %, к спленэктомии с аутотрансплантацией селезеночной ткани - 20 %, к спленэктомии - у 9 %. В зависимости от тяжести травмы селезенки в 81,5% случаев используем «традиционные» вмешательства (спленэктомия, спленорафия, резекция органа, тампонады раны сальником на ножке), в 17 % применяем видеолапароскопическую технику, а в 1,5 % - также чрескожную пункцию и аспирацию гематомы под контролем УЗИ.
При повреждениях селезенки 1 ст. тяжести операции путем чревосечения («традиционные») в настоящее время не выполняем. При 2 ст. тяжести повреждения они выполняются у 25 %больных, при 3 ст. - в 62 % и 4 ст. - во всех случаях. Среди них спленэктомию выполняем в 24 % случаев. Альтернативой полного удаления селезенки считаем аутотрансплантацию ее ткани, которая была выполнена в 62 % наблюдений. Не преуменьшая роли аутотрансплантации, ее нельзя противопоставлять ОСО, как с точки зрения сохранения морфологической структуры, как и функциональных качеств органа.
При 2 ст. тяжести повреждения селезенки ОСО удается выполнить в 53 % случаев: спленорафию - в 62 % наблюдений, резекцию - в 38 %. Спленорафию выполняют наложением одного или нескольких швов (чаще П - или 8-образных) рассасывающимися нитями (викрил 3/0-4/0) на атравматической колющей игле. В качестве «опоры» для швов используют прядь большого сальника на ножке или отдельные его фрагменты размерами 2x3 см. Важным моментом спленорафии считают расположение швов поперечно к ходу внутриорганных сосудов, избегают также надавливания иглодержателем на легко травмируемую капсулу селезенки.
При резекции селезенки временный гемостаз осуществляют путем наложения на ножку селезенки мягкого сосудистого зажима, после чего производят мобилизацию ее. С учетом резекции поврежденного участка паренхимы для уменьшения кровотечения из раны предварительно часть селезеночной ножки, соответствующая повреждению и превышающая ее длину на 1,5-2,0 см, лигируют. После обескровливания выбранного сегмента его удаляют, стараясь разделять капсулу и паренхиму в пределах обескровленных сегментов. Встречающиеся кровоточащие сосуды перевязывают викрилом А/0-5/0. Раневую поверхность обрабатывают плазменным потоком или лазерной коагуляцией, затем производят пластику культи сальником на ножке, который подшивают по окружности непрерывным викриловым швом или сквозным 8-образным. Резекцию селезенки, как правило, заканчивалась спленорафией с тампонадой раны каким-либо гемостатическим материалом. «Укрепление» швов как в случаях спленорафии, так и резекции селезенки осуществляют пластинкой «Тахокомб».
Операции с использованием видеолапароскопической техники удается выполнить при 1 и 2 ст. повреждений селезенки в 39,5 % случаев. Среди них производят пункционную аспирацию обширной подкапсульной гематомы селезенки с последующей пластикой пункционного отверстия клеевой композицией, коагуляцию ран лазерным излучением, клеевую пластику раны «Кано-конлитом», гемостаз пластинкой «Тахокомб», спленорафию, которую осуществляют по типу оментолиенопексии.
Внедрение в клиническую практику таких методов визуального контроля как УЗИ, дает возможность точно диагностировать характер повреждения селезенки и проводить лечение, не прибегая к лапаротомии или видеолапароскопии - путем пункции гематомы органа.
Ранения поджелудочной железы
Несмотря на использование комплексных методов обследования, ранения поджелудочной железы до операции выявляется редко, вот почему оперативное вмешательство часто проводится на фоне выраженных воспалительных изменений. Поэтому каждого поступившего с ранением поджелудочной железы следует рассматривать как пострадавшего, страдающего травматическим панкреатитом, так как ранения поджелудочной железы является пусковым механизмом, активирующим протеолитические ферменты.
В повседневной практике используют классификацию, в которой повреждения поджелудочной железы разделены на 4 степени тяжести. Первая степень тяжести - ушиб органа, подкапсульная гематома без повреждения капсулы встречается в 35 % случаев. Вторая степень тяжести - повреждение железы без разрыва главного панкреатического протока выявляется в 24 % наблюдений. Повреждения поджелудочной железы третьей степени тяжести -травма железы с разрывом главного панкреатического протока - в 32 %. Повреждения поджелудочной железы четвертной степени тяжести - панкреатодуоденальная травма обнаруживаются у 9 % пострадавших.
Выделение 4 групп повреждений поджелудочной железы имеет непосредственное практическое значение, поскольку раненым каждой группы выполняется свой специфический объем оперативного вмешательства. Объем хирургических вмешательств по поводу огнестрельных ранений и повреждений поджелудочной железы до конца не определен, так как при указанной патологии выполняется до 18 различных видов оперативных пособий (табл.2).
Тем не менее, лучшие результаты получают при выполнении следующих операций: при 1 степени тяжести - этапной санационной видеооменто-панкреатоскопии, при 2 степени - герметизации железы пластинкой «ТахоКомб», этапной оментопанкреатоскопии с использованием видеолапароскопической техники или «абдомизация» железы, плазменной или лазерной коагуляции сосудов, герметизации пластинкой «ТахоКомб» с использованием этапной видеооментопанкреатоскопии; при 3 степени - окклюзии протоковой системы железы, этапной оментопанкреатоскопии с использованием видеолапароскопической техники или видеоассистированной дистальной резекции железы, этапной видеооментопанкреатоскопии; при 4 степени - пилоросохраняющей панкреатодуоденальной резекции.
Таблица 2. Характер операций в зависимости от тяжести ранений поджелудочной железы (%)
| Тяжесть травмы железы | Частота выполнения | Характер операций |
| 1ст. | 6,9 | Вскрытие гематомы, дренирование, тампонада |
| 16,3 | Оментопанкреатопексия, дренирование, тампонада | |
| 6,3 | Этапная санационная видеооментопанкреатоскопия | |
| 5,1 | Санационная видеолапароскопия, дренирование сальниковой сумки | |
| 2 ст. | 7,5 | Шов железы, дренирование, тампонада |
| 3,8 | «Абдоминизация» железы, дренирование, тампонада | |
| 5,7 | Герметизация железы пластинкой «ТахоКомб» этапная оментопанкреатоскопия с использованием видеолапароскопической техники | |
| 7,5 | «Абдоминизация» железы, плазменная или лазерная коагуляция сосудов, герметизация пластинкой «ТахоКомб» с использованием видеолапароскопии, этапная видеооментопанкреатоскопия | |
| Ill ст. | 13,8 | Дистальная резекция |
| 1,9 | «Абдоминизация» железы, дренирование, тампонада | |
| 3,8 | Сшивание главного панкреатического протока на дренаже | |
| 3,1 | Вшивание дистальной части железы в тонкую кишку | |
| 1,3 | Сшивание каудальной и дистальной культей железы «конец в конец» с отключенной по Ру петлей тонкой кишки | |
| 4,4 | Окклюзия протоковой системы железы, этапная оментопанкреатоскопия с использованием видеолапароскопической техники | |
| 3,8 | Видеоассистированная дистальная резекция железы, этапная видеооментопанкреатоскопия | |
| IVст. | 2,5 | Классическая панкреатодуоденальная резекция |
| 3,8 | Пилоросохраняющая панкреатодуоденальная резекция | |
| 2,5 | Продольная панкреатоеюностомия с дистальной резекцией поджелудочной железы |
Существенную роль в исходах при ранениях и травмах поджелудочной железы имеет поэтапная санация сальниковой сумки, для чего выполняют оментобурсопанкреатостомию. Техника оментобурсопанкреатостомии с использованием видеолапароскопической техники заключалась в следующем. После выполнения основных этапов операции, связанных с травмой поджелудочной железы, через контрапертурные отверстия в сальниковую сумку вводят фистулу, которую швами и шайбами фиксируют к передней брюшной стенке вместе с большим сальником.
Фистула фирмы «VIRA» (NEW TECHNOLOGYS) ПКП «ВИРА» г.Красноярск), выполнена из прозрачного биоинертного материала с диаметром внутреннего просвета 10-11 мм, что позволяет установить визуальный контроль за состоянием брюшной полости. Две шарнирные втулки, встроенные в корпус устройства, дают возможность использовать эндоскопическую технику для систематической санации брюшной полости. После операции при необходимости выполняют этапную панкреатоскопию через установленную фистулу.
Ранения полых органов
Ранения желудка относительно чаще сопровождают случаи проникающих ранений и реже встречаются при закрытых травмах живота. Следует отметить анатомические особенности, имеющие отношение к повреждениям этого органа,- большую подвижность и относительную защищенность. При ранениях в '/3 всех случаев одновременно повреждаются обе стенки желудка. Эта статистика важна для хирурга, идущего на лапаротомию по поводу проникающего ранения живота; при повреждении передней стенки строго обязательно рассечение желудочно-поперечно-ободочной связки с целью ревизии задней стенки. Тщательному осмотру должны подвергаться стенки желудка в местах прикрепления сальника вдоль малой и большой кривизны, где жировая ткань способна маскировать небольшие проникающие дефекты стенки. Повреждение желудка, проникающее в его просвет, подлежит ушиванию двухрядными швами.
В случаях огнестрельных ранений, особенно высокоскоростными пулями, следует иссечь ткани в границах видимых изменений. При этом 1-й ряд швов носит гемостатический характер и накладывается через все слои (непрерывный рассасывающимися нитями); 2-й ряд состоит из отдельных серозно-мышечных швов (нерассасывающиеся материалы). При обширных повреждениях органа, когда возникает необходимость в удалении очень больших участков, лишенных жизнеспособности, показана типовая резекция желудка в масштабах, определяемых границами повреждения.
Сквозные дефекты стенки двенадцатиперстной кишки относительно чаще возникают в результате проникающих ранений живота. При закрытых травмах этот отдел желудочно-кишечного тракта повреждается при весьма значительной силе прямых ударов. Тогда, как правило, нарушается целость забрюшинно расположенной части кишки.
Для полноценного осмотра и хирургического лечения повреждений двенадцатиперстной кишки валено провести ее мобилизицию: рассечь брюшину по обоим краям кишки; пересечь брюшину у латерального края правой половины толстой кишки; пересечь связку Трейтца. Правый фланг поперечной ободочной кишки следует мобилизовать в медиальном направлении. Обнаружению небольших перфораций двенадцатиперстной кишки способствует интраоперационное введение красителя (метиленовый синий) через назогастральный зонд. Нельзя оставлять без внимания более или менее значительные гематомы в стенке кишки, так как в последующем они вызывают вторичную перфорацию, стеноз или обструкцию.
Небольшие травматические дефекты всех отделов двенадцатиперстной кишки подлежат ушиванию отдельными вворачивающими (1-й этаж) и серо-серозными (2-й этаж) швами в поперечном направлении. При больших дефектах, когда ушивание приводит к стенозированию просвета кишки, необходимо наложить гастроеюноанастомоз, который уменьшает нагрузку на поврежденную кишку и предупреждает развитие непроходимости. Однако более целесообразно в подобной ситуации полностью пересечь поврежденную двенадцатиперстную кишку на уровне дефекта; наглухо ушить оба ее конца и наложить гастроеюноанастомоз.
На выбор типа операции при повреждениях двенадцатиперстной кишки влияет локализация травматического дефекта. Так, при значительном повреждении верхнего (проксимального) отдела кишки ее резецируют в направлении к пилорическому отделу, т. е., по сути дела, идут на дистальную резекцию желудка (антрумэктомия). Культю двенадцатиперстной кишки следует ушивать наглухо, а непрерывность ЖКТ восстанавливать путем наложения гастроеюноанастомоза, как и при обычной резекции желудка по типу Биль-рот-П. При ненадежном ушивании культи двенадцатиперстной кишки в ее просвет вставляют трубку диаметром 3 мм для послеоперационной декомпрессии, отведения желчи и кишечного содержимого. Область оперативного вмешательства дополнительно дренируют широкопросветными трубками, подключенными к источнику вакуума. В желудок вводят постоянный зонд. Выполнение такой же операции рекомендуется и при больших разрывах дистального отдела двенадцатиперстной кишки. Однако при этой локализации больших разрывов возможна резекция участка кишки с наложением первичного анастомоза.
Тонкая кишка повреждается в местах относительно прочной анатомической фиксации. Поэтому чаще дефекты возникают в проксимальном отделе тощей, дистальном отделе подвздошной кишки и в местах прикрепления спаек. По этой причине более рациональным признается ушивание дефектов, начиная с дистальных отделов кишки.
Резекцию поврежденного сегмента тонкой кишки предпринимают по следующим основным показаниям: выраженное сужение просвета кишки, возникающее после ушивания травматического дефекта; большие размеры и неправильная форма раневого дефекта; продольные разрывы и раны большой протяженности; множественные ранения на протяжении ограниченного участка кишки; локализация дефектов и обширных гематом у брыжеечного края кишки; обширные интрамуральные гематомы; отрывы брыжейки от края кишки и разрывы брыжейки в поперечном направлении. Восстановление просвета тонкой кишки после ее резекции производят наложением анастомоза «конец в конец» или «бок в бок».
При резекции тонкой кишки позднее 6 часов с момента травмы с наличием трех и более «факторов риска» (шок, острая массивная кровопотеря, гиповолемия, эндотоксикоз, вторичный иммунодефицит, респираторный дистресс-синдром, ДВС-синдром.) производят дополнительное формирование Y-образной декомпрессионной стомы.
Ранения и разрывы толстой кишки требуют особой тщательности в определении хирургической тактики из-за повышенного риска несостоятельности накладываемых швов и анастомозов. Для хирургического лечения используют несколько типов операций. Первый тактический вариант состоит в первичном ушивании дефекта толстой кишки с дополнительным наложением разгрузочной колостомы в приводящем отделе; второй вариант включает резекцию поврежденного участка с наложением первичного анастомоза; третий вариант предусматривает экстраперитонизацию ушитых ран и наложенных анастомозов с выведением и фиксацией их за пределами полости брюшины; четвертый и наиболее распространенный вид операции подразумевает после резекции поврежденного участка выведение одного или обоих концов толстой кишки на переднюю стенку живота в виде двух колостом; при этом отводящий отдел можно заглушить и оставить в свободной брюшной полости (по типу операции Гартмана). Выбор оперативной методики определяется рядом факторов, главными из которых являются этиология и характер повреждения (рана огнестрельная, нанесенная холодным оружием, подкожный разрыв); масштабы и локализация разрыва; загрязнение брюшной полости; время, прошедшее с момента ранения, и степень развития перитонита; сопутствующие травмы. Кроме того, должны учитываться описанные выше факторы риска. Ответственное решение о первичном зашивании раны толстой кишки с оставлением поврежденного участка в брюшной полости принимается только при наличии следующих благоприятных условий: изолированный характер колото-резаного ранения, небольшая протяженность дефекта (не более 2 см), малые сроки с момента ранения (не позже 2 ч), отсутствие признаков перитонита. При наличии тех же благоприятных условий огнестрельные раны небольших размеров (не менее 2 см) и не сопровождающиеся большой зоной контузии и некроза тканей также допустимо закрыть первичным швом, предварительно проведя иссечение некротических тканей.
На выбор оперативной тактики также влияет локализация повреждения. Так, раны слепой кишки в сомнительных случаях рекомендуется превращать в цекостому.
При ушивании небольших разрывов в восходящем отделе толстой кишки также следует без колебаний наложить разгрузочную цекостому. Обширные разрывы, разрушения восходящего отдела толстой кишки требуют его резекции с наложением первичного илеотрансверзоанастомоза. Признаки возникшего перитонита диктуют необходимость выводить после резекции как приводящую (подвздошную), так и отводящую (поперечную ободочную) кишку на переднюю стенку живота в виде стом. Значительная загрязненность полости брюшины, массивная кровопотеря, шок и сочетанный характер травмы -все это должно склонять хирурга к наиболее безопасному виду вмешательства - выведению обоих концов резецированной кишки на переднюю стенку живота в виде одноствольных колостом. Выведение за пределы брюшной полости поперечной ободочной и левой половины толстой кишки технически трудновыполнимо. В такой ситуации целесообразнее после резекции поврежденного участка приводящий отдел вывести наружу в виде одноствольной колостомы, а отводящий «заглушить» и погрузить в брюшную полость.
При отсутствии уверенности в необходимости первичной резекции участка кишки, а также при ненадежном ушивании ран, наложенных анастомозов их выводят за пределы брюшины на срок 10 дней. Для этого под кишку в поперечном направлении подкладывают пластмассовую или резиновую трубку либо выкраивают участок фасции. Выведенный участок кишки укрывают влажной повязкой.
При ранениях и травмах левой половины толстой кишки, как и внутри-брюшинного отдела прямой кишки, рекомендуется резекция поврежденного отдела; приводящий отдел используют для формирования одноствольной колостомы; отводящий - заглушают и погружают в брюшную полость. Подобная тактика продиктована высоким риском несостоятельности швов при первичном ушивании дефектов и значительными трудностями экстраперитонизации левой половины толстой кишки; она признается наиболее безопасной и рекомендуется для большинства повреждений, включая случаи огнестрельных ранений.
При обширных повреждениях толстой кишки разрушенный участок выводится из брюшной полости и фиксируется к брюшине.
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 581; Нарушение авторских прав?; Мы поможем в написании вашей работы!