
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пример 5
|
|
|
|
Пример 4
Пример 3
В какую сторону сместится равновесие реакции N2O4 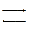 2NO2 – 56,98 кДж
2NO2 – 56,98 кДж
1) при повышении температуры
2) при понижении давления
3) при увеличении концентрации NO2
Данная задача решается по принципу Ле-Шателье:
1) прямая реакция эндотермическая Þ при Т химическое равновесие будет смещаться вправо (в сторону эндотермической реакции).
2) прямая реакция идёт с увеличением числа моль вещества, поэтому при понижении Р равновесие сместиться вправо.
3) при увеличении [NO2], равновесие будет смещаться в сторону той реакции, которая идёт на расходование этого вещества, то есть влево.
Изменением каких факторов можно осуществить сдвиг равновесия вправо у реакции
СО2 + Ств 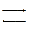 2СО – 160,5 кДж.
2СО – 160,5 кДж.
Прямая реакция эндотермическая, идёт с увеличением числа моль газообразных веществ (СО2 и СО) Þ необходимо:
1) повысить Т
2) понизить давление
3) увеличить концентрацию исходных веществ СО2 и С, уменьшить продукта СО.
Для реакции СН3СООН + С2Н5ОН 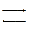 СН3СООС2Н5 + Н2О при 25°С КС = 4. В каком направлении протекает реакция, если массы веществ равны: уксусной кислоты 50 кг, 27 кг спирта, 37 кг эфира и 54 кг воды.
СН3СООС2Н5 + Н2О при 25°С КС = 4. В каком направлении протекает реакция, если массы веществ равны: уксусной кислоты 50 кг, 27 кг спирта, 37 кг эфира и 54 кг воды.
| DF -? | Задача на уравнение изотермы Вант Гоффа. |
| T = 298 K KC = 4 m k = 50кг m СН = 27 кг m эф = 37 кг m в = 54 кг R = 8,314 Дж/моль×К | Так как объём в системе не меняется, то вместо молярной концентрации можно использовать количество вещества (моль).
 
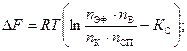
|
пэф = mэф/Mэф Мэф = 10-3(12 × 4 + 16 × 2 + 8) = 88 ×10-3 кг/моль
пв = mв/Mв Мв = 10-3(2 + 16) = 18×10-3 кг/моль
пк = mк/Mк Мк = 10-3(12×2 + 16×2 + 4) = 60×10-3 кг/моль
пв = mв/Mв Мсп = 10-3(12×2 + 16 + 6) = 46 × 10-3 кг/моль
пк = 50/60×10-3 = 0,83×103 моль
пв = 54/18×10-3 = 3×103 моль
пэф = 37/88×10-3 = 0,42×103 моль
псп = 27/46 × 10-3 = 0,59 моль
|
|
|
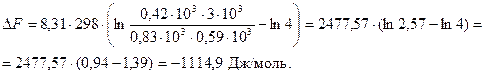
DF < 0 Þ реакция протекает в прямом направлении.
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 1519; Нарушение авторских прав?; Мы поможем в написании вашей работы!