
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основное уравнение МКТ идеального газа
|
|
|
|
Молекулярно – кинетическая теория газов
Вещество находится в газообразном состоянии, если средняя кинетическая энергия хаотического движения его молекул превышает среднюю потенциальную энергию их взаимодействия.
Вмолекулярно – кинетической теории рассматривается физическая модель – идеальный газ.
Идеальный газ – это модель реального газа, согласно которой:
- между молекулами отсутствуют силы взаимодействия;
- размеры молекул газа пренебрежительно малы по сравнению с расстоянием между ними;
- столкновения молекул газа между собой и стенками сосуда абсолютно упругие.
У молекул идеального газа есть только кинетическая энергия, и нет потенциальной энергии.
В элементарном курсе физики в теории рассматривается одноатомный идеальный газ – газ, молекула которого состоит из одного атома.
Реальные газы при не слишком низких температурах и достаточно малых давлениях (разреженные газы) по своим свойствам близки к идеальному газу. Например, гелий при комнатной температуре и атмосферном давлении с хорошим приближением подчиняется законам идеального газа.
позволяет найти давление газа и понять от чего оно зависит
1. 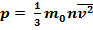 2.
2. 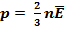 3.
3. 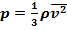 4.
4. 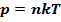
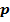 – давление газа – результат ударов о стенки сосуда большого числа молекул вследствие их хаотического движения. Измеряется как средняя сила большого числа молекул, действующая на единицу площади
– давление газа – результат ударов о стенки сосуда большого числа молекул вследствие их хаотического движения. Измеряется как средняя сила большого числа молекул, действующая на единицу площади 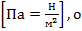 дна молекула давления не создаёт.
дна молекула давления не создаёт.
Хаотическое поступательное движение молекул газа называется тепловым движением, для одной молекулы понятие не существует, хаотичным движение молекул становится тогда, когда их много за счёт столкновений друг с другом. Движение одной молекулы механическое.
|
|
|
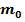 - масса молекулы газа.
- масса молекулы газа.
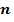 - концентрация молекул газа – число молекул в единице объёма:
- концентрация молекул газа – число молекул в единице объёма: 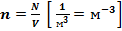
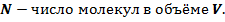
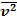 - средний квадрат скорости – квадрат скорости, в среднем приходящийся на одну молекулу:
- средний квадрат скорости – квадрат скорости, в среднем приходящийся на одну молекулу: 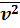 =
= 
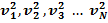 - квадраты скоростей молекул.
- квадраты скоростей молекул.
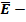 средняя кинетическая энергия хаотического (теплового) движения молекул – кинетическая энергия, в среднем приходящаяся на одну молекулу:
средняя кинетическая энергия хаотического (теплового) движения молекул – кинетическая энергия, в среднем приходящаяся на одну молекулу: 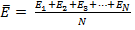 ,
, 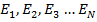 – кинетические энергии молекул,
– кинетические энергии молекул, 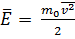
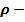 плотность газа – масса молекул в единице объёма:
плотность газа – масса молекул в единице объёма: 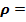
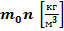
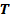 - абсолютная температура (температура по шкале Кельвина)
- абсолютная температура (температура по шкале Кельвина) 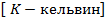
Температура – степень нагретости тела, величина, характеризующая тепловое движение молекул: чем быстрее движутся молекулы, тем выше температура. Температура – главная характеристика состояния теплового равновесия, для всех тел в тепловом равновесии она одинакова, разность температур тел указывает направление теплообмена: энергия от более нагретого тела передаётся к менее нагретому телу, пока не уравняются их температуры и не наступит тепловое равновесие.
Температура – мера средней кинетической энергии теплового движения молекул: 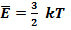 – средняя кинетическая энергия теплового движения молекул газа пропорциональна абсолютной температуре.
– средняя кинетическая энергия теплового движения молекул газа пропорциональна абсолютной температуре.
Понятие температуры для одной молекулы не существует
 - постоянная Больцмана, коэффициент перехода от средней кинетической энергии к абсолютной температуре:
- постоянная Больцмана, коэффициент перехода от средней кинетической энергии к абсолютной температуре: 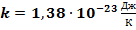
Абсолютный нуль – ноль на шкале Кельвина – температура, при которой средняя кинетическая энергия молекул равна нулю, т.е. температура, при которой должно прекратиться движение молекул. Так как молекулы не двигаться не могут, абсолютный нуль не достижим.
Температура по шкале Кельвина не может быть отрицательной. Термодинамическая шкала абсолютных температур – шкала положительных температур.
На практике для измерения температуры используется шкала Цельсия:
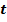 – температура по шкале Цельсия
– температура по шкале Цельсия 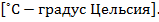
В основе шкалы Цельсия опорные точки: 0˚С – температура таяния льда при нормальном атмосферном давлении; 100˚С – температура кипения воды при нормальном атмосферном давлении.
|
|
|
Связь температуры по шкале Кельвина с температурой по шкале Цельсия
Устанавливается на основе того, что шаг обеих шкал одинаков (Δt =ΔT) и 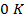 соответствует
соответствует 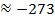 ˚. ˚С
˚. ˚С 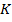
100 373
0 273
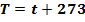
-273 0
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 881; Нарушение авторских прав?; Мы поможем в написании вашей работы!