
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Відновлення оксидів заліза
Вище 570°С
1. 3Fe2O3 + H2 = 2Fe3O4 + H2O + Q
2. Fe3O4 + H2 = 3FeO + H2O - Q
3. FeO + H2 = FeO + H2O - Q
Нижче 570 0С
1. 3Fe2O3 + H2 = 2Fe3O4 + H2O + Q
4. 1/4Fe3O4 + H2 = 3/4Fe + H2O - Q
Константа рівноваги цих реакцій, у разі коли тверді або рідкі фази не утворюють між собою розчинів і не розчинені в інших речовинах, записується в наступним вигляді
Kp = 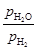 =
=  ; %H2O + %H2 = 100; %H2O =
; %H2O + %H2 = 100; %H2O =  .
.
Зміна рівноважного складу газу з температурою для даних реакцій представлена на рис. 4.7.
При 570°С оксиди FeO і Fe3O4 рівноміцні, тому рівноважні газові суміші в реакціях (2), (3) і (4) мають однаковий склад і відповідні криві перетинаються при 570°С (точка m). В області нижчих температур закисна фаза нестійка і реакції (2) і (3) втрачають значення. При температурі вище 570°С відпадає перетворення (4). По графіку можна встановити області існування різних фаз в системі Fe – О. Так, поле між кривими 2 і 3 належить газовим сумішам з недоліком Н2 по відношенню до рівноважного змісту для реакції (3) і з лишком – для реакції (2). Отже, дані суміші окислювальні для заліза і відновні для Fe3O4. Вони обумовлюють переходи Fe ® FeO і Fe3О4 ® FeO і забезпечують стабільність закисної фази. Так само можна встановити, що в областях вище за криві 3 і 4 стійке залізо, а нижче за лінії 4 і 2 – Fe3О4. Поле стабільності Fe2О3 вельми обмежено і розташовується під кривою 1.
|
|
Дата добавления: 2014-11-20; Просмотров: 479; Нарушение авторских прав?; Мы поможем в написании вашей работы!