
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методика решения задач
|
|
|
|
Алгоритм решения, например, задачи: «Определить рН и степень диссоциации уксусной кислоты в растворе 0,2М по СН3СООН и 0,1М по СН3СООNa»:
1. Написать уравнения процессов, протекающих при образовании данного раствора, в нашем примере это:
а) 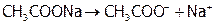 (необратимо),
(необратимо),
б) 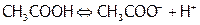 (обратимо).
(обратимо).
2. Выбрать расчетные формулы для определения искомых величин. Для нашего примера:
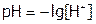 и
и 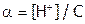 (ибо концентрация диссоциированных молекул уксусной кислоты по уравнению (б) равна
(ибо концентрация диссоциированных молекул уксусной кислоты по уравнению (б) равна 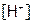 ).
).
3. Обозначить через Х концентрацию частиц, которую нужно определить для решения задачи: 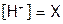 моль/л.
моль/л.
4. Установить, равновесие какой реакции определяет концентрацию данных ионов, и использовать выражение константы равновесия этой реакции для расчета их концентрации. В нашей задаче Н+ образуются при диссоциации СН3СООН [30], поэтому находим 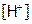 из выражения константы равновесия этого процесса:
из выражения константы равновесия этого процесса:
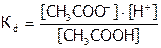 .
.
5. Определить величины, входящие в полученное выражение константы из справочника или по условию задачи, или выразив через Х.
В нашем случае 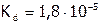 (по справочным данным). Концентрация молекул СН3СООН равна исходной ее концентрации (0,2 моль/л) за вычетом того количества кислоты, которое диссоциировано на ионы
(по справочным данным). Концентрация молекул СН3СООН равна исходной ее концентрации (0,2 моль/л) за вычетом того количества кислоты, которое диссоциировано на ионы 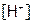 и
и 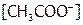 . Поскольку
. Поскольку 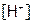 обозначили за Х моль/л, то, очевидно, количество диссоциированных молекул уксусной кислоты тоже будет равно Х моль/л (по уравнению (4)). Значит:
обозначили за Х моль/л, то, очевидно, количество диссоциированных молекул уксусной кислоты тоже будет равно Х моль/л (по уравнению (4)). Значит:
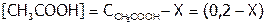 моль/л.
моль/л.
Концентрация ацетат-ионов складывается из 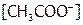 , образующейся при диссоциации уксусной кислоты, то есть Х моль/л (уравнение (б)) и из концентрации ацетат-ионов, полученных при диссоциации ацетата натрия (уравнение (а)). А поскольку последний является сильным электролитом (
, образующейся при диссоциации уксусной кислоты, то есть Х моль/л (уравнение (б)) и из концентрации ацетат-ионов, полученных при диссоциации ацетата натрия (уравнение (а)). А поскольку последний является сильным электролитом (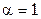 ), то при диссоциации 0,1 моль этой соли образуется 0,1 моль
), то при диссоциации 0,1 моль этой соли образуется 0,1 моль 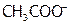 . Итак, суммарно[31]:
. Итак, суммарно[31]:
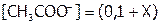 моль/л.
моль/л.
|
|
|
6. Подставить найденные значения и обозначения в выражение константы и найти Х. Для нашей задачи получим:
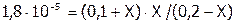 .
.
Значениями Х в качестве слагаемых пренебрегаем[32], как величинами, небольшими по сравнению с числами 0,1 и 0,2, и получаем:
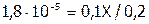 , откуда
, откуда 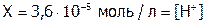 .
.
7. Подставляем найденные значения в формулы расчета искомых величин:
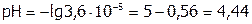 ,
,
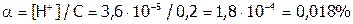 .
.
Используя указанную методику, можно решать задачи и для других равновесных состояний, в частности, для системы «осадок-раствор». Например, пусть требуется определить рН раствора над осадком Zn(OH)2 и растворимость последнего.
1. В данной системе имеет место равновесие:
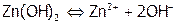 .
.
2. Поскольку при растворении осадка образуются ионы ОН-, то рН находим по формуле: 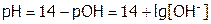 .
.
Растворимость же осадка (s), т.е. число его молей в 1 л насыщенного раствора (в соответствии с уравнением (6)) будет равно 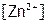 .
.
3. Обозначим 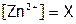 моль/л, тогда, судя по уравнению:
моль/л, тогда, судя по уравнению:
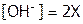 моль/л. [33]
моль/л. [33]
4. Не только ионы 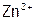 , но и
, но и 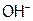 образуются (в основном) при растворении осадка, значит, находим их концентрацию из выражения ПР:
образуются (в основном) при растворении осадка, значит, находим их концентрацию из выражения ПР:
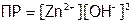
5. Значение ПР берем из справочника.
6. Подставляем ПР и принятые обозначения:
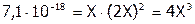 , откуда:
, откуда: 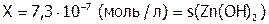 ,
,
а 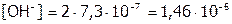 и
и 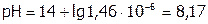 .
.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 399; Нарушение авторских прав?; Мы поможем в написании вашей работы!