
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Властивості тугоплавких сполук
|
|
|
|
Тугоплавких сполук
Властивості та застосування безкисневих
ТУГОПЛАВКИХ СПОЛУК
ОТРИМАННЯ ПОРОШКІВ БЕЗКИСНЕВИХ
Розвиток нової техніки потребує створення матеріалів, що мають високі температури плавлення, твердість, зносостійкість, пластичність за високих температур, специфічні магнітні й електричні властивості.
Ці властивості мають тугоплавкі сполуки або матеріали, до складу яких вони входять. До тугоплавких сполук передусім належать карбіди, бориди, нітриди та силіциди перехідних металів IVа — VIа підгруп періодичної системи елементів Д. І. Менделєєва.
Особливістю перехідних металів є те, що вони, окрім зовнішніх валентних електронів, мають також внутрішні недобудовані енергетичні рівні. Їх участь в утворенні хімічних зв’язків з неметалами (С, N, В, Si) сприяє утворенню міцних сполук, що мають високі температури плавлення, твердість, стійкість проти агресивних середовищ. Крім того, тугоплавкі сполуки мають чітко виражені металеві властивості та високі тепло- й електропровідність. З підвищенням температури їх електричний опір зростає, як і всіх металевих провідників. Поблизу абсолютного нуля багато сполук виявляють властивості надпровідності, а за високих температур випускають з поверхні електрони. Деякі властивості тугоплавких сполук наведено в табл.7.1.
Властивості тугоплавких сполук зумовлені також і їх структурними особливостями. Залежно від положення металу в періодичній системі елементів спостерігається неперервна і систематична зміна структури і властивостей їх сполук. Часто вони утворюють фази впровадження або близькі до них фази з ізольованими атомами неметалу. Характер структури сполук перехідних металів з неметалами залежить від співвідношення розмірів радіусів атомів металу R Меі неметалу Rх.
|
|
|
Згідно з правилом Хегга за співвідношення Rx / R Ме< 0,59 утворюються фази упровадження, а за Rx/R Ме > 0,59—фази зі складними гратками. Проте є і винятки з цього правила. Так, карбіди вольфраму і молібдену, для яких Rх / R Ме<0,59, не є фазами упровадження. Найбільш близькі за структурою карбіди і нітриди, з одного боку, і бориди та силіциди – з другого.
Метали IVа і Vа підгруп утворюють найбільш тугоплавкі карбіди і нітриди з кубічною або гексагональною щільноупакованою граткою.
Таблиця 7.1
| Сполука | Темпера-тура плавлення, °С | Густина, г/см3 | Мікро-твер-дість, ГПа | Модуль пруж-ності, ГПа | Коефіцієнт термічного розширення
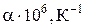
| Питомий
електроопір

|
Тепло-провід-ність, 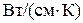
|
| TiC | 4,92 | 32,0 | 7,47 | 61,0 | 0,068 | ||
| ZrC | 6,66 | 26,0 | 6,73 | 49,0 | 0,116 | ||
| HfC | 12,67 | 29,1 | 6,30 | 39,0 | 0,163 | ||
| VC | 5,48 | 28,0 | 7,20 | 78,0 | 0,098 | ||
| NbC | 7,82 | 24,0 | 6,65 | 51,1 | 0,150 | ||
| ТаС | 14,40 | 18,0 | 6,30 | 42,1 | 0,219 | ||
| Cr3C2 | 18,95 | 6,74 | 13,0 | 11.70 | 75,5 | 0,190 | |
| Mo2C | 9,16 | 15,0 | 7,80 | 71,0 | 0,318 | ||
| WC | 15,77 | 24,0 | 3,84 | 19,2 | 0,293 | ||
| TiN | 5,21 | 19,9 | 9,35 | 40,0 | 0,418 | ||
| ZrN | 7,28 | 15,2 | 10,2 | 28,0 | 0,282 | ||
| HfN | 13,84 | 16,0 | 6,9 | 32,0 | 0,190 | ||
| VN | 6,04 | 15,2 | 8,35 | 85,0 | 0,029 | ||
| NbN | 7,98 | 14,0 | 10,10 | 78,0 | 0,042 | ||
| ТаN | 13,80 | 16,6 | 3,6 | 180,0 | 0,055 | ||
| TiB2 | 4,52 | 33,7 | 4,5 | 29,0 | 0,645 | ||
| ZгВ2 | 6,09 | 22,5 | 5,9 | 13,0 | 0,230 | ||
| HfB2 | 11,20 | 29,0 | 6,3 | 10,6 | 0,213 | ||
| VB2 | 5,10 | 28,0 | 7,9 | 22,7 | 0,422 | ||
| NЬВ2 | 7,00 | 26,0 | 7,7 | 25,7 | 0,240 | ||
| ТаВ2 | 12,62 | 25,0 | 7,9 | 32,5 | 0,167 | ||
| СгВ2 | 5,60 | 16,0 | 10,5 | 30,0 | 0,318 | ||
| Мo2В5 | 7,48 | 23,5 | 8,6 | 26,0 | 0,268 | ||
| WB5 | 13,10 | 26,6 | 7,8 | 22,0 | |||
| TiSi2 | 4,39 | 8,53 | 12,5 | 16,9 | 0,415 | ||
| ZгSi2 | 4,88 | 10,63 | 8,3 | 75,8 | — | ||
| НfSi2 | 7,20 | 9,12 | — | — | — | — | |
| VSi2 | 4,66 | 9,6 | — | 11,2 | 66,5 | — |
|
|
|
Продовження таблиці 7.1
| NbSi2 | 5,45 | 10,5 | 8,4 | 50,4 | — | ||
| ТаSi2 | 8,83 | 15,6 | – | 8,9 | 46,1 | — | |
| СгSi2 | 4,91 | 11,3 | 10,4 | 914,0 | — | ||
| МоSi2 | 6,12 | 11,5 | 8,25 | 21,6 | 0,485 | ||
| WSi2 | 9,8 | 10,9 | 6,25 | 12,5 | 0,466 |
За ними слідують менш стійкі сполуки металів VIа підгрупи, з яких карбіди і нітриди молібдену і вольфраму ще зберігають простих структур, а карбіди хрому мають складніші структури з великими елементарними осередками.
Метали IVа підгрупи утворюють тільки карбіди і нітриди типу МеС, МеN, склад яких може значно відхилятися від стехіометричного з відповідною зміною властивостей. Метали Va підгрупи, разом з указаними сполуками, утворюють нижчі карбіди і нітриди Ме2Сі Мe2Nз гексагональними щільноупакованими гратками. Зони гомогенності для цих сполук металів Vа підгрупи звужуються. Тенденція до різноманіття форм і звуження зон гомогенності зберігається і для сполук металів VIa підгрупи. У цьому разі розміри металевих атомів стають відносно настільки малими, що з утворенням карбідів або сильно спотворюються кристалічні гратки металу (Сг), або змінюються послідовності упаковки (Мо, W), хоча це стосується тільки монокарбідів і не поширюється на нижчі карбіди.
За структурою бориди перехідних металів IVa – VIaпідгруп значно складніші від карбідів і нітридів. Це проміжні сполуки між інтерметалевими сполуками типу берилідів і фазами упровадження. Для бору, що має порівняно великий атомний радіус (0,087 нм), умови Хегга задовольняють тільки його сполуки з цирконієм (R в/ R Zr = 0,54), а для сполук з титаном це співвідношення безпосередньо дорівнює 0,59. Завдяки цьому бориди мають різноманітні й складні структури, у яких важливим є хімічний зв’язок між атомами металів і бору. Цей зв’язок створюється за рахунок загальних електронів і переходу атома бору в стан позитивно зарядженого іона або атомного остова. Сила хімічного зв’язку зростає зі збільшенням кількості атомів бору в боридних фазах.
|
|
|
Атоми бору в структурах бориду з малим їх умістом ізольовані один від одного, а з великим — валентно зв’язані, при цьому вони в міру збільшення вмісту бору утворюють складніші структурні конфігурації. Тому бориди класифікують таким чином:
1) бориди з ізольованими атомами бору: Ме4В, Ме3В;
2 ) бориди з ізольованими парами атомів бору: Ме3В2;
3) бориди з одинарними ланцюжками з атомів бору: МеВ;
4) бориди з здвоєними ланцюжками з атомів бору: Мe3B4
5) бориди із сітками з атомів бору: МеВ2, Мe2В5
6) бориди з каркасами з атомів бору: МеВ4, МеВ6.
Усі дібориди перехідних металів, а також борид вольфраму W2B5 ― це структурні типи із сітками з атомів бору.
Структурні особливості боридів і прагнення атомів бору в них до утворення sр3 – sр2 - електронних конфігурацій визначають їх достатньо високі твердість і крихкість. Для боридів також характерні високі електропровідність, тугоплавкість, помірний коефіцієнт термічного розширення.
Багато спільного в структурах з боридами мають силіциди перехідних металів IVa – VIа підгруп. Силіциди характеризуються поєднанням металевих зв’язків між атомами металів і силіцію з ковалентними зв’язками між атомами силіцію, а також значною часткою ковалентних зв’язків між атомами металу, яка зростає із зменшенням електронно-донорної здатності металів. Зі збільшенням вмісту силіцію в силіцидах утворюються складніші структури. Нижчі силіциди утворюють металеві структури з ізольованими атомами силіцію (Me3Si) внаслідок заміщення атомами силіцію атомів металу за умови, що R Si / R Me £ 84...0,85. Із підвищенням відносного вмісту силіцію з’являються структури з ізольованими парами атомів силіцію типу Ме3, Sі2, МeSi2,з ланцюгами з атомів силіцію типу Ме5Si3, із шарами і просторовими каркасами з атомів силіцію типу МeSi2
|
|
|
Особливості структур силіцидів і хімічного зв’язку між їх атомами визначаються тим, що їх температури плавлення зазвичай нижчі, ніж відповідних металів (табл. 7.1). Твердість силіцидів відносно невелика і не перевищує 10...15 ГПа. Вони також мають невисокі механічі властивості і здатність до повзучості за відносно низьких температур. Деякі вищі силіциди є напівпровідниками (Сг3Si2). Багато силіцидів перехідних металів парамагнітні, при цьому парамагнетизм у них виражений набагато слабкіше, ніж у відповідних металів. Важливою властивістю силіцидів є їх висока хімічна стійкість і стійкість проти окиснення на повітрі.
Застосування тугоплавких сполук. Оскільки тугоплавкі сполуки мають високу твердість, міцність і хімічну стійкість, їх широко застосовують в інструментальній промисловості для виготовлення за їх участю лезоподібного інструмента, а також вільних і зв’язаних абразивних матеріалів. Головне місце серед лезоподібнихінструментів займають вироби з порошкових твердих сплавів. Для їх виготовлення використовують карбіди, бориди, нітриди та їх сплави. Застосовують тугоплавкі сполуки також для виготовлення абразивного інструмента для шліфування та полірування, магнітно-абразивних порошків для фінішної магнітно-абразивної обробки деталей машин. Широкого застосування набувають карбіди і бориди у складі наплавних матеріалів і матеріалів для нанесення жароміцних і зносостійких композиційних покриттів газотеремічними методами.
Останнім часом тугоплавкі сполуки застосовуються для нанесення покриттів малої товщини з газової фази на поверхню інструмента для підвищення його експлуатаційних характеристик. Найчастіше з цією метою застосовують покриття з карбіду і нітриду титану, карбідів молібдену і гафнію, а також двошарові і навіть тришарові покриття ТiС, Ті(СN), ТіN. Нанесений на твердий сплав шар карбіду має високу адгезію до основного матеріалу, зносостійкість і коефіцієнт лінійного розширення, які сумірні з коефіцієнтом лінійного розширення твердого сплаву, а подальші шари збільшують в’язкість різальної кромки, що підвищує стійкість інструментів у 2—5 разів.
Багато тугоплавких сполук використовують як конструкційні матеріали в апаратах, що експлуатуються в хімічних виробництвах. Це, перш за все, твердосплавна арматура насосів з перекачування агресивних розчинів і пульп та компресорів для стиснення газів. Деталі з тугоплавких сполук знаходять застосування у вузлах різних машин, що працюють в умовах високих температур, підвищеного газоабразивного зносу і т. ін.
Тугоплавкі сполуки мають високі вогнетривкі властивості — стійкість у контакті з розплавленими металами, задовільні міцність і ерозійну стійкість. Ширше за вогнетривкий матеріал застосовують карбід силіцію, що є основою вогнетривів, які мають високі теплопровідність, механічну міцність і абразивну стійкість.
Використання тугоплавких сполук як випарників дозволило значно розширити можливості вакуумної металізації, яка дала змогу наносити металеві покриття на метали, скло, кераміку, пластмасу, шкіру і тканини.Як посудина для випаровування алюмінію, міді, нікелю застосовують диборид, карбід та нітрид титану. Вогнетривкі матеріали на основі диборидів, дисиліцидів молібдену і карбіду силіцію застосовують як захисні чохли термопар для неперервного контролю температури сталі, чавуну, кріолітоглиноземного розплаву, алюмінію, міді, сплавів на основі кольорових металів.
Тугоплавкі сполуки входять також до складу матеріалів електротехнічного призначення. Так, наприклад, дисиліцид молібдену, карбід силіцію використовують як нагрівники високотемпературних печей з робочою температурою до 1650 °С. Дисиліцид молібдену — основний резистивний матеріал печей сучасної електроніки. Як нагрівники для печей з нейтральним середовищем або вакуумних з робочою температурою до 2800 °С можна використовувати карбід ніобію. Застосування таких нагрівників дозволяє забезпечити найважливіші технологічні процеси вирощування монокристалів, термообробку спецсплавів. Перспективним є використання тугоплавких сполук як матеріалів зі спеціальними електрофізичними властивостями. Високі термоелектричні властивості в поєднанні з високою вогнетривкістю дозволяють виготовляти з них термоелектроди високотемпературних термопар. Так, для вимірювання температури в окиснювальних середовищах використовують термоелектроди з дисиліцидів молібдену і вольфраму (MoSi2/WSi2). Вимірювати температуру нейтральних і активних газових средовищ (наприклад вуглецевмісних) до 2000...2500 °С можна термопарами з термоелектродами з графіту і дибориду цирконію (С/ZгВ2), графіту і карбіду титану (С/ТiС).
Багато тугоплавких карбідів і боридів мають високі термоемісійні властивості і використовуються для виготовлення з них катодів потужних пристроїв катодної електроніки для плавлення тугоплавких металів і сплавів, а також виготовлення установок з термоелектронного перетворення теплової енергії в електричну.
Із тугоплавких сполук виготовляють електроди, що не витрачаються для контактного зварювання вуглецевих і неіржавійних сталей, напрямлені втулки зварювальних напівавтоматів зі збільшеним вильотом електрода.
У зв’язку зі зростанням експлуатаційних параметрів технологічних процесів і машин нової техніки використання тугоплавких сполук неперервно збільшуватиметься.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 1502; Нарушение авторских прав?; Мы поможем в написании вашей работы!