
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Очистка коллоидных растворов
|
|
|
|
После того, как коллоидные растворы получены, они почти всегда загрязнены примесями – избытком исходного электролита или стабилизатора. Для получения устойчивых коллоидных растворов, способных к длительному хранению, пригодных для медицинского использования вакцин и сывороток, их очищают. Для этого используют фильтрацию, диализ, электродиализ и ультрафильтрацию.
Фильтрация через бумажные фильтры – это очистка от грубодисперсных примесей.
Диализ - это процесс очистки золя от низкомолекулярных примесей, которые легко проходят через полупроницаемую мембрану в чистый растворитель, а более крупные коллоидные частицы не проходят и остаются в диализном мешке (Рис 2.3а). Мембраны бывают естественные и искусственные – из целлофана, бычьего или рыбьего пузыря, коллодия и т.д. Процесс диализа длительный, поэтому его ускоряют, используют элекродиализ.
Электродиализ – диализ с применением электрического тока, с помощью которого создаётся направленное движение низкомолекулярных ионов через полупроницаемую мембрану, что ускоряет очистку от низкомолекулярных электролитов и примесей (Рис. 2.3б).
Ультрафильтрация (отделение дисперсной фазы от среды) – это фильтрование через полупроницаемую мембрану под давлением или с помощью вакуума, в результате чего создается разность давлений по обе стороны мембраны, что ускоряет диализ. Ультрафильтрация и электродиализ применяются в аппарате «искусственная почка». В организме по принципу ультрафильтрации в почечных нефронах происходит постоянная очистка крови от низкомолекулярных продуктов метаболизма (аммиака, фосфатов, хлоридов, ксенобиотиков).
Рис. 2.3 Очистка коллоидных растворов
|
|
|
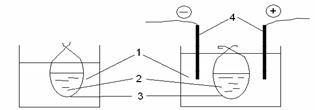 1 - растворитель (вода)
1 - растворитель (вода)
2 –коллоидный раствор
3 - мембрана
а. Диализ б. Электродиализ 4 – электроды
2.4. Строение коллоидных частиц – мицелл.
Отдельные частицы коллоидных растворов называют мицеллами. Мицеллы имеют сложное строение. Основой мицеллярной теории является наличие у мицелл двойного электрического слоя. Он может образоваться:
– либо за счёт избирательной адсорбции ионов на поверхности;
– либо в результате ионизации молекул твёрдой фазы.
Рассмотрим образование мицелл в коллоидном растворе иодида серебра, полученном методом химической конденсации по реакции обмена: AgNO3 + KJ = AgJ↓ + KNO3
В зависимости от соотношения исходных веществ может быть три случая:
а) при эквивалентом соотношении реагентов коллоидный раствор образоваться не может, стабилизация системы происходит за счет уменьшения площади поверхности, т.е. роста кристаллов AgJ и выпадения осадка.
б) рассмотрим образование мицеллы при небольшом избытке KJ. В этом случае уменьшение поверхностной энергии может идти за счёт адсорбции ионов из раствора. Согласно правилу Панета – Фаянса из раствора электролита на поверхности микрокристаллов адсорбируется тот ион, который входит в состав твёрдого тела и способен достраивать его кристаллическую решётку. В нашем случае в растворе имеются ионы К+ и J-. Достраивание кристаллической решётки агрегата идет за счёт ионов J–, входящих в состав кристалла. Иодид-ионы в количестве «n» адсорбируются на поверхности микрокристаллов (агрегате мицеллы), и поверхность приобретает отрицательный заряд: m[AgJ] · nJ-, поэтому их называют потенциалоообразующими. Образуется ядро мицеллы. К поверхности ядра притягиваются из раствора оставшиеся противоионы калия, К+ (но не все, а в количестве «n - x»).
Потенциалообразующие ионы J- и связанные противоионы К+ образуют вокруг ядра плотный адсорбционный слой. Он имеет заряд. Его потенциал называют дзета-потенциалом. Агрегат с адсорбционным слоем составляют гранулу: { m[AgJ] nJ- (n-х) К+ }х-
|
|
|
Поскольку в адсорбционном слое потенциалообразующих ионов больше, чем противоионов, то гранула имеет заряд, совпадающий по знаку с зарядом потенциалообразующих ионов.
В адсорбционный слой гранулы входят не все противоионы К+, а только часть, (n-x), а оставшиеся противоионы К+ (х) находятся дальше – в рыхлом диффузном слое. Почему? Противоионы испытывают действие двух противоположных сил:
1. притяжения к заряженной поверхности ядра;
2. теплового движения, стремящегося равномерно распределить их в объёме.
Поэтому плотность слоя противоионов убывает по мере удаления от заряженной поверхности гранулы.
двойной электрический слой, ДЭС
 агрегат
агрегат
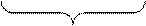 { m[AgJ] nJ- (n-х) К+ } х- хК+ ∙ l H2O
{ m[AgJ] nJ- (n-х) К+ } х- хК+ ∙ l H2O
ядро потенциало противоионы рыхлый гидратная
образующие диффузный оболочка
 ионы слой
ионы слой
плотный адсорбционный слой
 гранула
гранула
мицелла
Гранула с диффузным слоем образует мицеллу. Мицелла электронейтральна. В зависимости от исходных концентраций растворов, условий и других факторов числа m, n и х могут меняться. Снаружи мицелла окружена гидратной оболочкой. Избыток KJ адсорбировался на поверхности микрокристаллов нерастворимого иодида серебра и образовал двойной электрический слой (ДЭС). Этот защитный слой препятствует росту кристаллов и выпадению осадка. Поэтому избыток электролита, из которого формируется двойной электрический слой, является стабилизатором.
в) если имеется небольшой избыток другого электролита, AgNO3, то состав коллоидной мицеллы будет другим. Агрегат по-прежнему будут составлять молекулы иодида серебра, AgJ. Но после образования мелких кристалликов осадка AgJ – зародышей, в растворе остались лишь ионы Ag+ и NO3-. По правилу Панета-Фаянса адсорбироваться на поверхности могут только ионы Ag+, достраивающие ее кристаллическую решётку.
Ag+ - потенциалообразующие ионы. Образуется ядро - m[AgJ]nAg+. Значит, противоионами будут ионы NO3-. Вместе с ионами Ag+ они образуют адсорбционный слой, а с агрегатом – положительно заряженную гранулу:
{ m[AgJ] nAg+ (n-х) NO3- }х+
 Оставшиеся х ионов NO3- входят в диффузный слой мицеллы. Они сольватированы
Оставшиеся х ионов NO3- входят в диффузный слой мицеллы. Они сольватированы
|
|
|
{ m[AgJ] nAg+ (n-х) NO3- }х+ хNO3- l H2O
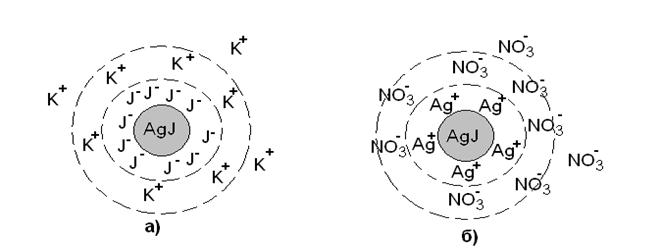
Рис.2.4 Схема строения коллоидной мицеллы золя иодида серебра
а) полученного при избытке KJ
б) полученного при избытке AgNO3
2.5. Электрокинетические явления в золях – электрофорез и электроосмос
Хотя мицелла и не заряжена, но если её поместить в электрическое поле, то ионы рыхлого диффузного слоя будут отрываться и перемещаться к электроду с противоположным знаком, а заряженная гранула – к другому электроду.
Движение твёрдой дисперсной фазы относительно неподвижной дисперсионной среды в электрическом поле называется электрофорезом.
Так, при электрофорезе золя иодида серебра, стабилизированного KJ, катионы рыхлого диффузного слоя отрываются и мигируют к катоду («–» электроду), а отрицательно заряженная гранула перемещается к аноду («+» электроду).
Перемещение жидкой среды относительно твердой дисперсной фазы под действием электрического поля называется электроосмосом. Впервые эти явлениия наблюдал в 1808 г. Ф.Ф. Рейс.
Эти электрокинетические явления не могли бы наблюдаться, если бы не было двойного электрического слоя в составе мицеллы.
Если все ионы диффузного слоя перейдут в адсорбционный слой, тогда в плотном адсорбционном слое заряд противоионов будет равен заряду потенциалообразующих ионов, и гранула не будет иметь заряда. Такое состояние коллоидного раствора называется изоэлектрическим – ИЭС. Это состояние коллоидной системы наименее устойчивое.
Электрофорез и электроосмос широко используют на практике для:
– разделения белков, α- аминокислот, нуклеиновых кислот, антибиотиков;
– нанесения коллоидных частиц каучука или красок на металлические поверхности;
– обезвоживания пористых материалов;
– диагностики многих заболеваний;
- лечения.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 2053; Нарушение авторских прав?; Мы поможем в написании вашей работы!