
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Требования, предъявляемые к природным и полусинтетическим оптически активным веществам
|
|
|
|
Химическое разделение энантиомеров через диастереомеры
Это наиболее хорошо исследованный и потому часто используемый метод. Наибольшее количество расщеплений сделано именно этим методом. Первое такое расщепление было выполнено Пастером в 1853 г. Для разделения рацемической винной кислоты им был использованы природные оптически активные алкалоиды: (+)-цинхотоксин и (+)-хинотоксин.
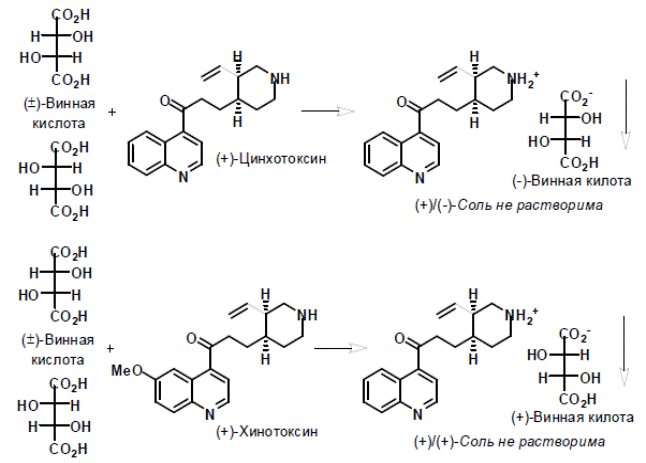
Суть метода заключается в действии на рацемат оптически активным реагентом, в результате чего образуется новая пара веществ − диастереомеров. Последние могут быть разделены вследствие различия в их физических свойствах. Хиральный реагент после разделения диастереомеров отщепляют.
Общая схема:
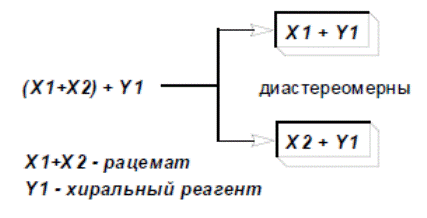
На расщепляемый рацемат X1+X2 действуют оптическим активным, обычно природного происхождения, реагентом Y1: при этом получается новая пара веществ X1Y1 и X2Y1, уже не находящиеся друг с другом в отношениях антиподов − эти вещества диастереомерны, а, значит, различаются по физическим свойствам. Разницы в растворимости, давлении пара, коэффициентах адсорбции во многих случаях оказывается достаточно, чтобы разделить диастереомеры кристаллизацией, перегонкой или хроматографически.
На практике расщепление рацематов через диастереомеры включает четыре последовательные операции: образование пары диастереомеров, их отделение друг от друга, разрушение каждого из диастереомеров, причем выделяются антиподы разделяемого вещества. Последняя стадия – регенерация оптически-активного реагента.
Пример: рацемический (R,S)-1-фенилэтиламин образует с природной (2R,3R)-винной кислотой две диастереомерные соли: [(R)-1-фенилэтиламин]·[(2R,3R)-винная кислота] и [(S)-1-фенилэтиламин]·[(2R,3R)-винная кислота], которые обладают различной растворимостью в этаноле и могут быть разделены кристаллизацией. Свободный амин выделяют затем экстракцией диэтиловым эфиром из водного щелочного раствора соли.
|
|
|
Очевидно, что образование диастереомеров возможно только в том случае, если разделяемое вещество имеет химически активную группу, способную взаимодействовать с подходящим асимметрическим реагентом (он также должен обладать химически активной функцией). Природа этой группы, вообще говоря, безразлична. Важно лишь, чтобы при реакции не затрагивались связи асимметрического центра, а образование и расщепление диастереомеров происходило легко. Практически чаще всего используют диастереомерные соли, все остальные реакции имеют несравненно меньшее значение. Для расщепления рацемических кислот необходимы оптически активные основания, для расщепления рацемических оснований − оптически активные кислоты.
Большинство асимметрических реактивов − вещества дорогие, поэтому большое значение имеет возможность регенерации реактивов после окончания расщепления. Пожалуй, единственный реагент, в отношении которого проблема регенерации не стоит из-за его дешевизны, винная кислота.
Природа предоставляет широкий набор хиральных агентов. Здесь можно встретить карбоновые кислоты, алкалоиды (амины − азотистые основания), аминокислоты, терпены (алканы, алкены, спирты, кетоны). Некоторые природные оптически активные вещества модифицируют, добавляя новые высоко реакционно-способные группировки (например, камфорсульфокислота и камфорная кислота из камфоры). Такие хиральные реагенты назовём полусинтетическими. Основные, наиболее дешёвые реагенты сведены в таблицу и разбиты по классам.
1. Доступность (низкая стоимость, лёгкость получения)
2. Стабильность источника поступления
|
|
|
3. Устойчивость при использовании и хранении (не рацемизуется в присутствии кислот и
оснований). Амины, например, на воздухе дают карбонаты.
4. Наличие активной функциональной группы (кислотная или аминная функции),
5. Высокая энантиомерная чистота
6. Возможность регенерации после разделения рацемата
7. Низкая токсичность
8. Доступность в виде обоих антиподов
9. Низкий молекулярный вес
10. Низкая растворимость
Примеры: α-метил-β-фенилэтиламин отвечает всем требованиям, но, к сожалению, он известен как амфетамин. В этой связи, как мощный стимулятор ЦНС подлежит особому учёту и фактически не доступен для обычного химика. Иногда, при высокой стоимости оптически активного реагента на первую роль выходит молекулярная масса, т.к. оплата проводится за граммы, а не за моли.
Для разделения антиподов аминов применяют природные карбоновые кислоты (винная, яблочная, миндальная, молочная) или полусинтетические кислоты (камфорная кислота, β-камфорсульфокислота). Здесь лидирующую позицию занимает правовращающая D-(R,R)-винная кислота − самое доступное и дешевое оптически активное вещество, получаемое в промышленных масштабах из “винного камня” (кислый тартрат калия), осаждающегося на стенках бочек винодельческих заводов. Кроме этого она доступна в обеих оптически активных формах. Применяют также более кислые чем исходная кислота, её производные по гидроксильным группам: ацетаты, дибензоильное производное, и пр. Часто получают малаты и манделаты. Лактаты аминов синтезируют реже из-за высокой гигроскопичности, как самой молочной кислоты, так и её солей. Широко используются производные камфоры и пирроглутаминовая кислота (легко получается из природной глутаминовой кислоты при нагревании).
Пример: рацемат (R,S)-1-фенилэтиламина образует с природной (2R,3R)-винной кислотой две диастереомерные соли: [(R)-1-фенилэтиламин]·[(2R,3R)-винная кислота] и [(S)-1-фенилэтиламин]·[(2R,3R)-винная кислота], которые обладают различной растворимостью в этаноле и могут быть разделены кристаллизацией. Свободный энантиомер амина выделяют экстракцией эфиром из щелочного раствора.
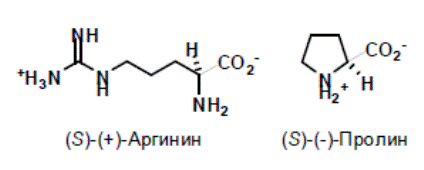
Для расщепления рацемических кислот используют их способность образовывать соли с хиральными природными (алкалоиды хинин, хинидин, бруцин, стрихнин, морфин, аминокислоты: (S)-(−)-пролин, (S)-(+)-аргинин) или синтетическими основаниями (1-фенилэтиламином, альфа-(нафтил-1)-этиламином). Учитывая чрезвычайную ядовитость природных алкалоидов, на практике предпочитают использовать синтетические основания.
|
|
|
Рацемические спирты (тиолы, диолы, фенолы) расщепляют путем превращения их в кислые эфиры дикарбоновых кислот, как правило, фталаты или сукцинаты с последующей нейтрализацией второй карбоксильной группы хиральным амином и перекристаллизацией образующейся смеси диастереоизомерных солей. Фталатную группу удаляют метилмагнийиодидом или, реже, гидролизом. Пример: реакция фталевого ангидрида с октанолом-2. Такой способ называют “ метод соединительных звеньев ”. Есть и другой старый метод, по которому спирт этерифицируют подходящей оптически активной кислотой (часто миндальной). Продукты разделяют колоночной хроматографией или перекристаллизацией. Но образующиеся диастереоизомерные сложные эфиры часто плохо кристаллизуются, что сильно ограничивает метод. Гидролиз сложноэфирной группы иногда тоже представляет сложности. Пример: бутанол-2 + миндальная кислота.
Широко применяются природные L - аминокислоты: пролин (2-карбоксипирролидин) и фенилаланин. В свободном виде, эти цвиттер-ионы мало пригодны для солеобразования с рацематами. Но N-ацилированные аминокилоты или их сложные эфиры находят применение в асимметрическом синтезе. Гораздо чаще встречается обратная задача: разделение рацемата искусственно полученной аминокислоты. В этом случае разомкнуть внутреннюю соль могут лишь сильные кислоты, для этого пригодна, например, β-камфорсульфокислота или β-пиненсульфокислота. Однако на практике выгоднее превратить рацемат аминокислоты в амид или сложный эфир и разделять соли, как это было описано выше для аминов или кислот. Чаще получают производные по аминогруппе (Boc, Ac, формил, бензоил, тозил, и др.) и разделяют их в виде солей с алкалоидами. Также широко используется и разделение эфиров аминокислот при помощи природных алкалоидов.
Карбонильные соединения могут быть разделены на энантиомеры несколькими способами. Здесь так же применяется метод соединительных звеньев. Так природные карбоновые кислоты вводят в реакцию с гидразином и конденсируют получающийся гидразид с карбонильным соединением (пример: гидразид (+)-миндальной кислоты + 3-метилциклогексанон). Второй метод: реакция конденсации с эфирами природных аминокислот, делят диастереомерные основания Шиффа ((S)-(-)-амфетамин + кетон). Третий метод – синтез полуацеталей с применением диолов: например, диэтилового эфира (2R,3R)-(+)-винной кислоты.
|
|
|
|
|
Дата добавления: 2014-12-08; Просмотров: 975; Нарушение авторских прав?; Мы поможем в написании вашей работы!